名校
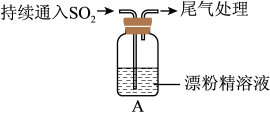
1 . 某学生对 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:
(1) 和
和 制取漂粉精的化学方程式是
制取漂粉精的化学方程式是_______ 。
(2) 试纸颜色的变化说明漂粉精溶液具有的性质是
试纸颜色的变化说明漂粉精溶液具有的性质是_______ 。
(3)向水中持续通入 ,未观察到白雾。推测现象i的白雾由
,未观察到白雾。推测现象i的白雾由 小液滴形成,进行如下实验:
小液滴形成,进行如下实验:
a.用酸化的 溶液检验白雾,产生白色沉淀;
溶液检验白雾,产生白色沉淀;
b.用湿润的碘化钾淀粉试纸检验白雾,无变化。
①实验b的目的是_______ 。
②由实验 不能判断白雾中含有
不能判断白雾中含有 ,理由是
,理由是_______ 。
(4)现象ⅱ中溶液变为黄绿色的向能原因是_______ 。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀 ,无明显变化。取上层清液,加入
,无明显变化。取上层清液,加入 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是_______ 。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:_______ 。
 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:| 操作 | 现象 |
取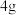 漂粉精固体,加入 漂粉精固体,加入 水 水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的 |  试纸先变蓝(约为12),后褪色 试纸先变蓝(约为12),后褪色 |
| i、液面上方出现白雾; ⅱ、稍后,出现浑浊,溶液变为黄绿色; ⅱi、稍后,产生大量白色沉淀,黄绿色褪去 |
(1)
 和
和 制取漂粉精的化学方程式是
制取漂粉精的化学方程式是(2)
 试纸颜色的变化说明漂粉精溶液具有的性质是
试纸颜色的变化说明漂粉精溶液具有的性质是(3)向水中持续通入
 ,未观察到白雾。推测现象i的白雾由
,未观察到白雾。推测现象i的白雾由 小液滴形成,进行如下实验:
小液滴形成,进行如下实验:a.用酸化的
 溶液检验白雾,产生白色沉淀;
溶液检验白雾,产生白色沉淀;b.用湿润的碘化钾淀粉试纸检验白雾,无变化。
①实验b的目的是
②由实验
 不能判断白雾中含有
不能判断白雾中含有 ,理由是
,理由是(4)现象ⅱ中溶液变为黄绿色的向能原因是
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀
 ,无明显变化。取上层清液,加入
,无明显变化。取上层清液,加入 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是②用离子方程式解释现象ⅲ中黄绿色褪去的原因:
您最近一年使用:0次
名校
解题方法
2 . 下列各组实验中,实验操作、现象及结论或解释均正确的是
| 选项 | 实验操作 | 实验现象 | 结论或解释 |
| A | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| B | 在干冰中央挖一个小穴,撒一些镁粉,用红热的铁棒把镁引燃,盖上另一块干冰 | 镁粉在干冰中继续燃烧,发出耀眼的白光 | CO2不能扑灭金属镁引起的火灾 |
| C | 向K2S溶液中通入足量的CO2,然后将产生的气体导入CuSO4溶液中 | CuSO4溶液中产生黑色沉淀 | Ka1(H2S)>Ka1(H2CO3) |
| D | 向蔗糖中加入适量浓硫酸,搅拌 | 产生黑色“面包” | 浓硫酸具有酸性和吸水性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 某小组用如下装置(夹持装置已略去)制备并探究 的性质。
的性质。 的化学方程式是
的化学方程式是___________ 。
(2)a中控制生成 多少的操作是
多少的操作是___________ ;反应后a中若溶液颜色无色,试管底部有灰白色固体,确定产物中有 的操作是
的操作是___________ 。
(3)b用于探究 的性质。
的性质。
①b中为___________ 溶液时,可证明 有漂白性。
有漂白性。
②b中为 和淀粉混合溶液时,溶液蓝色褪去,可证明
和淀粉混合溶液时,溶液蓝色褪去,可证明 有还原性,反应的化学方程式为
有还原性,反应的化学方程式为___________ 。
③b中为 溶液时,反应后在溶液中可检验出
溶液时,反应后在溶液中可检验出 ,说明检验
,说明检验 的方法是
的方法是___________ 。
④b中为 溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子
溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子 的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为
的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为___________ 。随着反应进行,又出现淡黄色沉淀,溶液黄色消失,这是由于溶液中的 与过量
与过量 又继续反应了,写出反应的离子方程式
又继续反应了,写出反应的离子方程式___________ 。
(资料: 能与S反应生成
能与S反应生成 ,
, 与酸反应生成S和
与酸反应生成S和 )。
)。
(4)c用于吸收 尾气,可选用的试剂是
尾气,可选用的试剂是___________ 。
A.NaOH溶液 B.澄清石灰水 C. 溶液
溶液
 的性质。
的性质。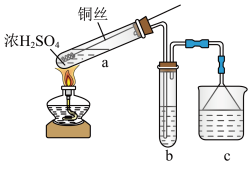
 的化学方程式是
的化学方程式是(2)a中控制生成
 多少的操作是
多少的操作是 的操作是
的操作是(3)b用于探究
 的性质。
的性质。①b中为
 有漂白性。
有漂白性。②b中为
 和淀粉混合溶液时,溶液蓝色褪去,可证明
和淀粉混合溶液时,溶液蓝色褪去,可证明 有还原性,反应的化学方程式为
有还原性,反应的化学方程式为③b中为
 溶液时,反应后在溶液中可检验出
溶液时,反应后在溶液中可检验出 ,说明检验
,说明检验 的方法是
的方法是④b中为
 溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子
溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子 的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为
的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为 与过量
与过量 又继续反应了,写出反应的离子方程式
又继续反应了,写出反应的离子方程式(资料:
 能与S反应生成
能与S反应生成 ,
, 与酸反应生成S和
与酸反应生成S和 )。
)。(4)c用于吸收
 尾气,可选用的试剂是
尾气,可选用的试剂是A.NaOH溶液 B.澄清石灰水 C.
 溶液
溶液
您最近一年使用:0次
4 . 在探究铜与硝酸反应时,发现在室温下,溶液A与铜片立即产生气泡,而相同条件下,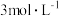 稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。
稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。 与浓
与浓 反应的化学方程式为
反应的化学方程式为___________ 。
(2)己知 与浓
与浓 反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因
反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因___________ 。
(3)查阅资料:
①二氧化氮溶于水的过程产生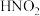 。
。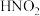 中氮元素的化合价为
中氮元素的化合价为___________ 。
②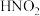 (亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。
(亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。
(4)分析溶液A与铜片立即产生气泡,而相同条件下,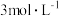 稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设:
稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设: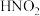 对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中
对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中___________ 。
(5)催化剂能够加快化学反应速率的原因是:改变反应历程,先参加反应,后又生成,所以反应前后催化剂的量和性质不发生改变。由此同学们推测 与稀硝酸反应中
与稀硝酸反应中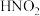 起催化作用的过程如下:
起催化作用的过程如下:
i.___________ (用离子方程式表示)
ii.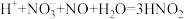
(6)同学们进一步查阅文献资料显示,工业生产硝酸时,会生成亚硝酸等物质。亚硝酸能分解为 (易分解为
(易分解为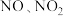 )等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是
)等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是___________ 。
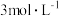 稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。
稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。
 与浓
与浓 反应的化学方程式为
反应的化学方程式为(2)己知
 与浓
与浓 反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因
反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因(3)查阅资料:
①二氧化氮溶于水的过程产生
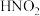 。
。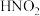 中氮元素的化合价为
中氮元素的化合价为②
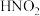 (亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。
(亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。(4)分析溶液A与铜片立即产生气泡,而相同条件下,
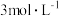 稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设:
稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设: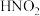 对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中
对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中(5)催化剂能够加快化学反应速率的原因是:改变反应历程,先参加反应,后又生成,所以反应前后催化剂的量和性质不发生改变。由此同学们推测
 与稀硝酸反应中
与稀硝酸反应中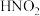 起催化作用的过程如下:
起催化作用的过程如下:i.
ii.
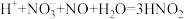
(6)同学们进一步查阅文献资料显示,工业生产硝酸时,会生成亚硝酸等物质。亚硝酸能分解为
 (易分解为
(易分解为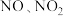 )等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是
)等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是
您最近一年使用:0次
5 . 1-溴丁烷可用于合成麻醉药盐酸丁卡因,也用于生产染料和香料,是稀有元素萃取的溶剂及有机合成的中间体,其制备如图(夹持装置略):
ⅱ.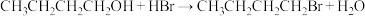
ⅲ.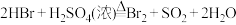
请回答下列问题:制备装置
(1)仪器a的名称是_______ 。装置b的作用是吸收尾气防止污染空气且能_______ 。
(2)制备过程中,加热回流,在此期间要不断地摇动反应装置,其原因为_______ 。
(3)若选用较浓的硫酸作为反应物,得到的产品会呈黄色,为除去颜色,最好选择下列的_______(填标号)溶液来洗涤产品。
(4)探究小组为研究1-溴丁烷的水解反应和消去反应,设计如下探究实验:_______ 。
②实验ⅲ的有机化学反应方程式是_______ 。
③为深入研究1-溴丁烷与 溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):加热圆底烧瓶一段时间后,试管中酸性高锰酸钾溶液褪色。
溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):加热圆底烧瓶一段时间后,试管中酸性高锰酸钾溶液褪色。_______ ;
II.乙同学对实验进行了改进,依据实验现象可判断是否发生消去反应,改进的方案是_______ 。


ⅱ.
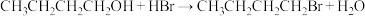
ⅲ.
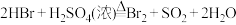
请回答下列问题:制备装置
(1)仪器a的名称是
(2)制备过程中,加热回流,在此期间要不断地摇动反应装置,其原因为
(3)若选用较浓的硫酸作为反应物,得到的产品会呈黄色,为除去颜色,最好选择下列的_______(填标号)溶液来洗涤产品。
| A.四氯化碳 | B.硫酸钠 | C.氢氧化钠 | D.亚硫酸钠 |
(4)探究小组为研究1-溴丁烷的水解反应和消去反应,设计如下探究实验:
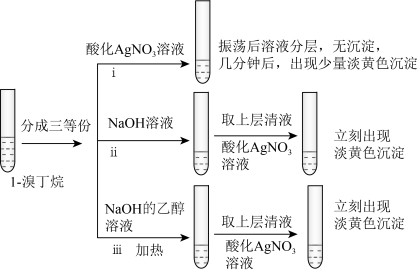
②实验ⅲ的有机化学反应方程式是
③为深入研究1-溴丁烷与
 溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):加热圆底烧瓶一段时间后,试管中酸性高锰酸钾溶液褪色。
溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):加热圆底烧瓶一段时间后,试管中酸性高锰酸钾溶液褪色。
II.乙同学对实验进行了改进,依据实验现象可判断是否发生消去反应,改进的方案是
您最近一年使用:0次
名校
解题方法
6 . 某小组同学探究三种价态(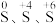 )疏元素间的相互转化。可以选用的试剂有:①
)疏元素间的相互转化。可以选用的试剂有:① 水溶液、②浓硫酸、③稀硫酸、④
水溶液、②浓硫酸、③稀硫酸、④ 溶液、⑤
溶液、⑤ 溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨
溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨ 溶液。
溶液。
(1)补全实验表格i ___________ ,ii ___________ ,iii ___________ 。
(2)实验5的化学方程式为___________ 。
(3)为了进一步验证实验1中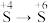 的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量
的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。
①实验a的目的是通过检验___________ ,证明转化得以实现。
②加稀盐酸的作用是___________ 。
乙同学认为还需要补充实验b:取等量的 溶液,向其中先加过量稀盐酸,再加足量
溶液,向其中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。
③补充实验b的原因是___________ 。
④综合实验a和b,实验1中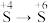 转化得以实现的证据是
转化得以实现的证据是___________ 。
(4)丙同学分析实验3和实验4现象不同的原因,在实验4中又添加了一种试剂___________ (填试剂编号),出现浑浊。发生反应的离子方程式是___________ 。
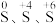 )疏元素间的相互转化。可以选用的试剂有:①
)疏元素间的相互转化。可以选用的试剂有:① 水溶液、②浓硫酸、③稀硫酸、④
水溶液、②浓硫酸、③稀硫酸、④ 溶液、⑤
溶液、⑤ 溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨
溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨ 溶液。
溶液。| 实验序号 | 预期的价态转化 | 选择的试剂 (填入试剂编号) | 实验现象 |
| 1 | 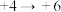 | ④⑥ | |
| 2 | i___________ | ii___________ | |
| 3 |  | ①⑤ | 出现浑浊 |
| 4 | ④⑤ | 无明显现象 | |
| 5 | 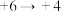 | iii___________ |
(2)实验5的化学方程式为
(3)为了进一步验证实验1中
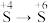 的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量
的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。①实验a的目的是通过检验
②加稀盐酸的作用是
乙同学认为还需要补充实验b:取等量的
 溶液,向其中先加过量稀盐酸,再加足量
溶液,向其中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。③补充实验b的原因是
④综合实验a和b,实验1中
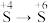 转化得以实现的证据是
转化得以实现的证据是(4)丙同学分析实验3和实验4现象不同的原因,在实验4中又添加了一种试剂
您最近一年使用:0次
名校
解题方法
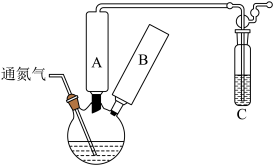
7 . 醋酸钴与双水杨醛缩乙二胺形成的配合物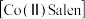 具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:
具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:___________ (填名称,下同),B处应安装的仪器是___________ ;装置C的作用是___________ ,通氮气的目的是___________ 。
(2)回流 ,沉淀转化为暗红色晶体。回流结束后进行如下操作:
,沉淀转化为暗红色晶体。回流结束后进行如下操作:
①停止通氮气 ②停止加热 ③关闭冷凝水
正确的操作顺序为___________ (填标号)。充分冷却后将溶液过滤,洗涤并干燥,得到配合物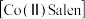 。
。
(3)测定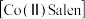 的载氧能力。将
的载氧能力。将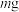 的
的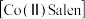 (相对分子质量为
(相对分子质量为 )加入圆底烧瓶中,在恒压漏斗中加入
)加入圆底烧瓶中,在恒压漏斗中加入 (配合物在
(配合物在 中可吸氧),如图搭建装置。
中可吸氧),如图搭建装置。___________ ,然后调节水平仪的水位至与量气管水位产生一定液面差。装置不漏气的现象是___________ 。
②调整水平仪高度,待___________ (填现象)时,记录量气管水位的体积刻度为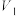 。将
。将 加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为
加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为 。已知大气压为
。已知大气压为 ,氧气的压强为
,氧气的压强为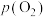 ,温度为
,温度为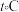 。配合物载氧量的
。配合物载氧量的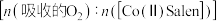 计算式为
计算式为___________ 。
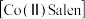 具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:
具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:
(2)回流
 ,沉淀转化为暗红色晶体。回流结束后进行如下操作:
,沉淀转化为暗红色晶体。回流结束后进行如下操作:①停止通氮气 ②停止加热 ③关闭冷凝水
正确的操作顺序为
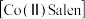 。
。(3)测定
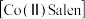 的载氧能力。将
的载氧能力。将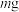 的
的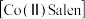 (相对分子质量为
(相对分子质量为 )加入圆底烧瓶中,在恒压漏斗中加入
)加入圆底烧瓶中,在恒压漏斗中加入 (配合物在
(配合物在 中可吸氧),如图搭建装置。
中可吸氧),如图搭建装置。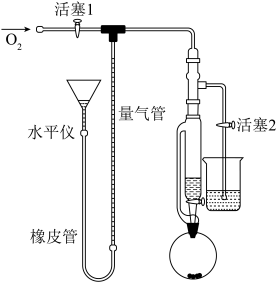
②调整水平仪高度,待
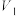 。将
。将 加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为
加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为 。已知大气压为
。已知大气压为 ,氧气的压强为
,氧气的压强为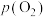 ,温度为
,温度为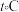 。配合物载氧量的
。配合物载氧量的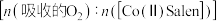 计算式为
计算式为
您最近一年使用:0次
8 . 按照下图进行铜与浓硫酸反应的探究实验,下列说法正确的是
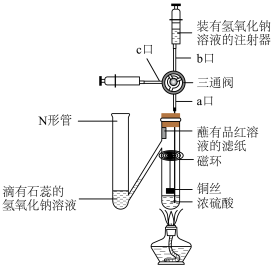
A.蘸有品红溶液的滤纸褪色,说明 具有强氧化性 具有强氧化性 |
| B.N形管溶液变为红色,说明有酸性气体进入N形管 |
| C.反应后,从c口抽取反应液加到足量的氨水中最终产生蓝色沉淀 |
| D.实验结束后从b口注入足量NaOH溶液,会有2种物质与NaOH反应 |
您最近一年使用:0次
9 . 实验室用如图所示装置检验草酸晶体( )分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入
)分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入 的盐酸溶液中生成黑色Pd粉。下列说法错误的是
的盐酸溶液中生成黑色Pd粉。下列说法错误的是
 )分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入
)分解生成的含碳气体产物(不考虑草酸蒸气)。已知:常温下,CO通入 的盐酸溶液中生成黑色Pd粉。下列说法错误的是
的盐酸溶液中生成黑色Pd粉。下列说法错误的是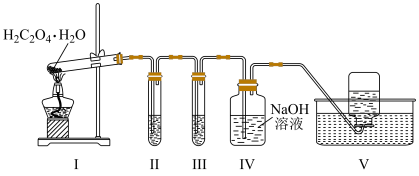
| A.Ⅰ中大试管口向上倾斜,可能因为草酸晶体的熔点低于分解温度 |
| B.由Ⅱ中现象可推断草酸晶体分解生成CO |
| C.Ⅱ、Ⅲ中现象可推断草酸晶体分解反应存在元素化合价变化 |
| D.可用燃烧法代替Ⅴ进行尾气处理 |
您最近一年使用:0次
名校
解题方法
10 . 实验小组探究溶液酸碱性对含锰化合物和 氧化还原反应的影响。
氧化还原反应的影响。
资料: .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。
 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。
 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。
 .
.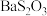 为微溶物。
为微溶物。
已知:实验 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是
 氧化还原反应的影响。
氧化还原反应的影响。资料:
 .
. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。 .
. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。 .
. 的还原产物与溶液酸碱性有关,通常酸性条件下被还原为
的还原产物与溶液酸碱性有关,通常酸性条件下被还原为 ,中性条件下被还原为
,中性条件下被还原为 ,碱性条件下被还原为
,碱性条件下被还原为 。
。 .
.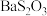 为微溶物。
为微溶物。| 实验 | 序号 | 试剂 | 现象 |
| i.先加试剂a ii.再加试剂b
|  | a:10滴3mol/LH2SO4溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液紫色变浅至接近无色,静置一段时间后出现乳白色浑浊 |
 | a:10滴蒸馏水 b:20滴0.002mol/LNa2S2O3溶液 | 产生棕黑色沉淀 | |
 | a:x滴6mol/LNaOH溶液 b:20滴0.002mol/LNa2S2O3溶液 | 溶液变为绿色,无沉淀生成;静置5min,绿色变浅,有棕黑色沉淀生成 |
 、
、 、
、 中
中 均被氧化为
均被氧化为 。下列说法不正确的是
。下列说法不正确的是A.实验 中出现乳白色浑浊发生反应:S2O 中出现乳白色浑浊发生反应:S2O +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
B.实验 所得溶液中 所得溶液中 的检验:取少量溶液加入足量 的检验:取少量溶液加入足量 ,若有白色沉淀生成,则说明有 ,若有白色沉淀生成,则说明有 |
| C.x=10 |
D.实验 产生棕黑色沉淀可能原因是 产生棕黑色沉淀可能原因是 碱性减弱后不稳定生成 碱性减弱后不稳定生成 棕黑色沉淀 棕黑色沉淀 |
您最近一年使用:0次