1 . 某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。

实验操作及现象:
试回答下列问题:
(1)操作I中产生气体的化学式为_________ 。操作I的目的是___________ 。
(2)C装置中白色沉淀的化学式是_______ 。操作II中当C装置中产生白色沉淀时立刻将B装置上提的原因是____________ 。
(3)操作III中A装置中产生无色气体的化学方程式是_____________ 。
(4)E装置内气体颜色逐渐加深的原因是__________ 。
(5)操作V现象产生的原因是(用两个化学方程式说明)_____ ,________ 。

实验操作及现象:
| 实验操作 | 现象 |
| I.将B装置下移,使碳酸钙与稀硝酸接触 | 产生气体 |
| II.当C装置中产生白色沉淀时,立刻将B装置上提 | |
| III.将A装置中铜丝放入稀硝酸中,给A装置微微加热 | A装置中产生无色气体,E装置中开始时出现浅红棕色气体 |
| IV.用F装置向E装置中鼓入空气 | E装置中气体颜色逐渐加深 |
| V.一段时间后 | C装置中白色沉淀溶解 |
(1)操作I中产生气体的化学式为
(2)C装置中白色沉淀的化学式是
(3)操作III中A装置中产生无色气体的化学方程式是
(4)E装置内气体颜色逐渐加深的原因是
(5)操作V现象产生的原因是(用两个化学方程式说明)
您最近一年使用:0次
2 . 已知:乙炔是无色无味的气体,实验室制的乙炔因电石中含有  、
、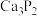 等,与水反应产生
等,与水反应产生 、
、 等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
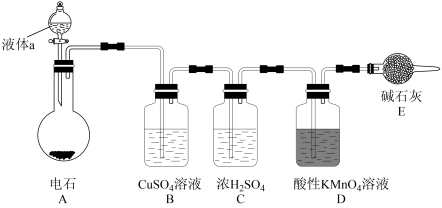
(1)写出实验室制取乙炔的化学方程式:_______
(2)实验室制取乙炔时,分液漏斗中的液体a通常是(填名称):_______
(3)①CuSO4溶液的作用是:_______
②装置D中的现象是:_______
(4)若将乙炔气体通入足量的溴水溶液中,溴水褪色,其反应的化学反应方程式为:_______
(5)装置E的作用是_______ 。
(6)乙炔可通过下列合成路线合成聚氯乙烯:乙炔→A→聚氯乙烯,由制A取聚氯乙烯的化学方程式为_______ 。
 、
、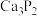 等,与水反应产生
等,与水反应产生 、
、 等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
(1)写出实验室制取乙炔的化学方程式:
(2)实验室制取乙炔时,分液漏斗中的液体a通常是(填名称):
(3)①CuSO4溶液的作用是:
②装置D中的现象是:
(4)若将乙炔气体通入足量的溴水溶液中,溴水褪色,其反应的化学反应方程式为:
(5)装置E的作用是
(6)乙炔可通过下列合成路线合成聚氯乙烯:乙炔→A→聚氯乙烯,由制A取聚氯乙烯的化学方程式为
您最近一年使用:0次
名校
3 . SO2的污染防治与利用对于环境保护意义重大。某化学小组在实验室中对SO2的制备、性质及回收利用等相关问题进行探究。请回答下列问题:
(1)制备并收集纯净的SO2

①用上图装置制备纯净的SO2,发生装置中反应的化学方程式为_______ 。
②装置的连接顺序为:a→_______ (按气流方向,用字母标号表示)。
(2)设计实验探究SO2中+4价S的性质
限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉KI溶液、新制H2S溶液
填写表格中相应内容:
①_______ ; ②_______ ;③_______ ; ④_______ 。
(3)设计回收利用SO2的途径: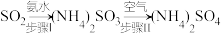 。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
①检验沉淀是否洗净的方法是_______ 。
②α=_______ ×100%(用含c、m的代数式表示)。

(1)制备并收集纯净的SO2

①用上图装置制备纯净的SO2,发生装置中反应的化学方程式为
②装置的连接顺序为:a→
(2)设计实验探究SO2中+4价S的性质
限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉KI溶液、新制H2S溶液
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 将SO2通入新制H2S溶液中 | 溶液变浑浊 | SO2中+4价S具有________性 |
| 实验二 | 将SO2通入_________中 | ________ | SO2中+4价S具有还原性,反应的离子方程式为_______ |
①
(3)设计回收利用SO2的途径:
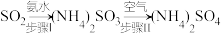 。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。①检验沉淀是否洗净的方法是
②α=

您最近一年使用:0次
2022-07-12更新
|
368次组卷
|
2卷引用:辽宁省锦州市2021-2022学年高一下学期期末考试化学试卷
4 . 工业上利用氧化铝基废催化剂(主要成分为Al2O3,含少量Pd)回收Al2(SO4)3及Pd的流程如下:
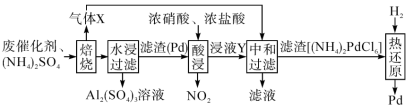
已知:浸液Y的主要成分为H2PdCl6。
(1)焙烧时产生的气体X的结构式为___________ 。
(2)写出“酸浸”的化学方程式___________ 。
(3)“热还原”过程中发生反应的化学方程式为___________ 。
(4)利用电化学原理处理流程中产生的NO2,既能有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,设计的电池装置如图所示:
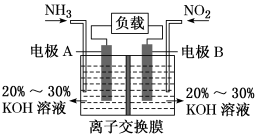
①电极A的电极反应式为___________ 。
②当有2.24 L(标准状况)NO2被处理时,转移电子的物质的量为___________ 。
(5)上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。某兴趣小组为探究高温下硫酸铵的分解产物,通过如下图所示装置进行实验,观察到B中溶液颜色变浅,C中无明显现象。
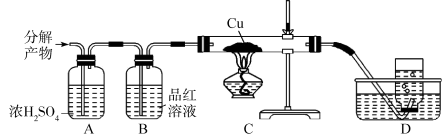
①置B的作用是___________ 。
②进一步测定可知:D中收集的气体是大气的主要成分之一、写出(NH4)2SO4高温分解的化学方程式___________ 。

已知:浸液Y的主要成分为H2PdCl6。
(1)焙烧时产生的气体X的结构式为
(2)写出“酸浸”的化学方程式
(3)“热还原”过程中发生反应的化学方程式为
(4)利用电化学原理处理流程中产生的NO2,既能有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,设计的电池装置如图所示:

①电极A的电极反应式为
②当有2.24 L(标准状况)NO2被处理时,转移电子的物质的量为
(5)上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。某兴趣小组为探究高温下硫酸铵的分解产物,通过如下图所示装置进行实验,观察到B中溶液颜色变浅,C中无明显现象。

①置B的作用是
②进一步测定可知:D中收集的气体是大气的主要成分之一、写出(NH4)2SO4高温分解的化学方程式
您最近一年使用:0次
5 . 某研究性学习小组利用如图装置制备 ,并对
,并对 的性质进行探究(装置的气密性已检查)。
的性质进行探究(装置的气密性已检查)。
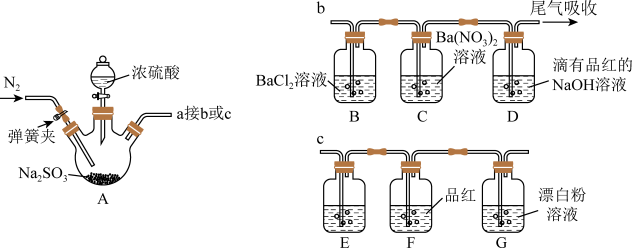
Ⅰ.探究 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)
(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是_______ 。
(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是_______ ,装置C中反应的离子方程式是_______ 。
(3)装置D中 全部转化为
全部转化为 的离子方程式为:
的离子方程式为:_______ 。
Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是_______
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是_______ ,其作用是_______ ,通过_______ 现象即可证明亚硫酸的酸性强于次氯酸。
 ,并对
,并对 的性质进行探究(装置的气密性已检查)。
的性质进行探究(装置的气密性已检查)。
Ⅰ.探究
 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间
 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是
(3)装置D中
 全部转化为
全部转化为 的离子方程式为:
的离子方程式为:Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是
您最近一年使用:0次
2022-06-17更新
|
142次组卷
|
2卷引用:辽宁省六校2021-2022学年高一下学期第三次联考化学试题
6 . 某化学自主实验小组通过实验制备 并探究
并探究 的性质。
的性质。
实验I:利用图1装置制取氨气并探究 与
与 的反应。
的反应。

(1)装置A中烧瓶内的试剂可选用_______ (填标号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,则需在 的导管末端连接表中的装置
的导管末端连接表中的装置_______ (填序号)。当装置D中集满氨气后,关闭 、
、 ,打开
,打开 ,引发喷泉的实验操作是
,引发喷泉的实验操作是_______ 。
(3)若探究氨气与氯气的反应,则需打开 、
、 ,
, 处导管连接制取纯净、干燥氯气的装置。
处导管连接制取纯净、干燥氯气的装置。
①装置D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为____ 。
②从 处导管速出的气体中含有少量
处导管速出的气体中含有少量 ,则装置C中应盛放
,则装置C中应盛放_______ (填化学式)溶液, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
实验II:利用图2装置探究 与
与 的反应。
的反应。
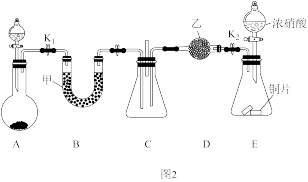
(4)装置E中反应的化学方程式为_______ 。
(5)若 能够被
能够被 还原,预期装置C中能观察到的现象是
还原,预期装置C中能观察到的现象是_______ 。
(6)此实验装置存在的一个明显缺陷是_______ 。
 并探究
并探究 的性质。
的性质。实验I:利用图1装置制取氨气并探究
 与
与 的反应。
的反应。
| 备选装置(水中含酚酞溶液) | ||
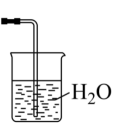 | 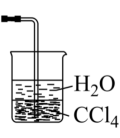 | 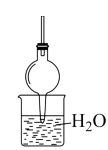 |
| I | II | III |
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,则需在
 的导管末端连接表中的装置
的导管末端连接表中的装置 、
、 ,打开
,打开 ,引发喷泉的实验操作是
,引发喷泉的实验操作是(3)若探究氨气与氯气的反应,则需打开
 、
、 ,
, 处导管连接制取纯净、干燥氯气的装置。
处导管连接制取纯净、干燥氯气的装置。①装置D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为
②从
 处导管速出的气体中含有少量
处导管速出的气体中含有少量 ,则装置C中应盛放
,则装置C中应盛放 发生反应的离子方程式为
发生反应的离子方程式为实验II:利用图2装置探究
 与
与 的反应。
的反应。
(4)装置E中反应的化学方程式为
(5)若
 能够被
能够被 还原,预期装置C中能观察到的现象是
还原,预期装置C中能观察到的现象是(6)此实验装置存在的一个明显缺陷是
您最近一年使用:0次
2022-06-14更新
|
96次组卷
|
2卷引用:辽宁省葫芦岛市协作校2021-2022学年高一下学期第一次联考化学试题
7 . 为探究 的性质,进行了如下实验(
的性质,进行了如下实验( 和
和 溶液浓度均为
溶液浓度均为 )。
)。
依据上述实验现象,结论不合理的是
 的性质,进行了如下实验(
的性质,进行了如下实验( 和
和 溶液浓度均为
溶液浓度均为 )。
)。| 实验 | 操作与现象 |
| ① | 在 水中滴加2滴 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。 溶液,呈棕黄色;煮沸,溶液变红褐色。 |
| ② | 在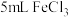 溶液中滴加2滴 溶液中滴加2滴 溶液,变红褐色; 溶液,变红褐色;再滴加  溶液,产生蓝色沉淀。 溶液,产生蓝色沉淀。 |
| ③ | 在 溶液中滴加2滴 溶液中滴加2滴 溶液,变红褐色; 溶液,变红褐色;将上述混合液分成两份,一份滴加  溶液,无蓝色沉淀生成; 溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉淀。 |
A.实验①说明加热促进 水解反应 水解反应 |
B.实验②说明 既发生了水解反应,又发生了还原反应 既发生了水解反应,又发生了还原反应 |
C.实验③说明 发生了水解反应,但没有发生还原反应 发生了水解反应,但没有发生还原反应 |
D.整个实验说明 对 对 的水解反应无影响,但对还原反应有影响 的水解反应无影响,但对还原反应有影响 |
您最近一年使用:0次
2022-06-10更新
|
12789次组卷
|
48卷引用:辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题
辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题2022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(11-14)(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编(已下线)专题12 化学实验方案的设计与评价-三年(2020-2022)高考真题分项汇编(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第06讲 氧化还原反应(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古通辽市开鲁县第一中学2021-2022学年高二下学期6月检测化学试题(已下线)第03讲 氧化还原反应(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)湖北省荆州市公安县第三中学2022-2023学年高三上学期8月月考化学试题山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题(已下线)第23讲 盐类水解 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省株洲市攸县第三中学2022-2023学年高三上学期第一次月考化学试题广东省广州市海珠外国语实验中学2022-2023学年高三上学期第二次阶段性考试化学试题(已下线)易错点34 化学实验方案的设计与评价-备战2023年高考化学考试易错题河北省石家庄市第二中学2022-2023学年高二上学期10月月考化学试题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)河南省顶级名校2022-2023学年高三上学期12月摸底考试化学试题河南省商丘市第一高级中学2022-2023学年高二上学期期末考试化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期开学暑假阶段验收化学测试题辽宁省沈阳市第二中学2023-2024学年高三上学期开学考试化学试题宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破坚持素养导向 突出创新命题湖南省长沙市第一中学2022-2023学年高三上学期月考卷(五)化学试题(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价湖南省攸县第三中学2022-2023学年高三第六次月考化学试题趋势1 创新命题形式(已下线)题型181 “实验-现象-结论”微型实验方案的设计与评价(已下线)题型45 物质性质探究型综合实验(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)河北省石家庄市第二中学2022-2023学年高三下学期2月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第4讲 盐类的水解山东省枣庄市第三中学2023-2024学年高三上学期10月月考化学试题山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
8 . 利用下列有关实验装置进行相关实验,不能达到实验目的的是


| A.用图甲所示装置检验金属钠与水反应的热效应 |
B.用图乙所示装置制取并收集干燥纯净的 |
C.用图丙所示装置可以比较 、 、 、S的氧化性 、S的氧化性 |
| D.用图丁所示装置检验氨气的水溶性 |
您最近一年使用:0次
2022-06-03更新
|
364次组卷
|
5卷引用:辽宁省葫芦岛市协作校2021-2022学年高一下学期第一次联考化学试题
9 . 某化学兴趣小组为探究浓硫酸的氧化性和 的性质,用如图所示装置(夹持仪器已省略)进行实验。回答下列问题:
的性质,用如图所示装置(夹持仪器已省略)进行实验。回答下列问题:
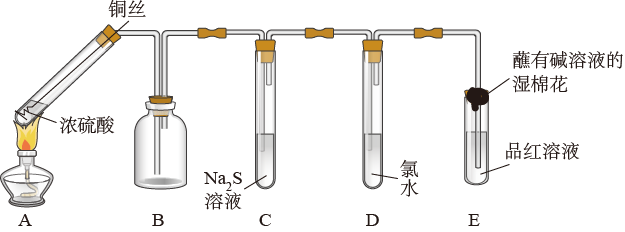
(1)装置A中反应的化学方程式为_______ ,A中铜丝可抽动,其优点是_______ 。
(2)B的作用为_______ 。
(3)①C中有黄色固体出现,说明 有
有_______ (填“氧化”或“还原”)性。
②D中生成两种强酸,写出化学反应方程式:_______ 。
(4)装置E中的现象是_______ ,试管口蘸有碱溶液的湿棉花的作用为_______ 。
 的性质,用如图所示装置(夹持仪器已省略)进行实验。回答下列问题:
的性质,用如图所示装置(夹持仪器已省略)进行实验。回答下列问题:
(1)装置A中反应的化学方程式为
(2)B的作用为
(3)①C中有黄色固体出现,说明
 有
有②D中生成两种强酸,写出化学反应方程式:
(4)装置E中的现象是
您最近一年使用:0次
10 . 氮氧化物(NOX)是大气污染物之一,处理工业废气中的NOx对于环境保护具有重要的意义。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
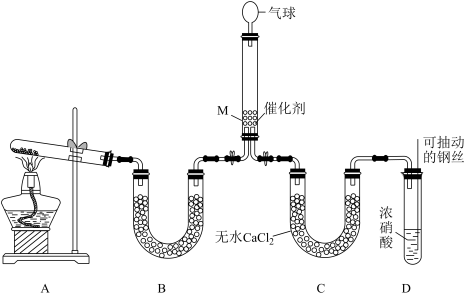
①用装置A制备NH3,其中发生反应的化学方程式为_______ ;装置B中的试剂是_______ 。
②装置D中发生反应的离子方程式是_______ ,铜丝可抽动的优点是_______ 。
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O,不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:
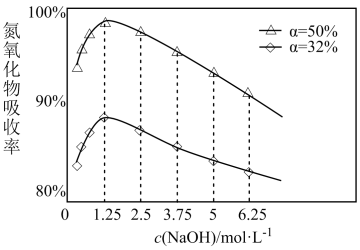
(α表示NOx中NO2的含量)
①用NaOH溶液吸收氮氧化物的最佳条件为:α=_______ ,c(NaOH)=_______ 。
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为_______ 。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。

①用装置A制备NH3,其中发生反应的化学方程式为
②装置D中发生反应的离子方程式是
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O,不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:

(α表示NOx中NO2的含量)
①用NaOH溶液吸收氮氧化物的最佳条件为:α=
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为
您最近一年使用:0次



