1 . 下面是某校化学研究性学习小组探究足量锌与浓硫酸反应的实验:
Ⅰ.甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。_______ 。
(2)若按气体从左到右的流向,气体流经的各装置连接顺序是_______ 。
(3)E中干燥管的作用是_______ 。
(4)证明混合气体中含有H2的实验现象为_______ 。
Ⅱ.乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。_______ (填序号)。
A.H2O2溶液 B.酸性KMnO4溶液 C.溴水 D.稀硫酸
该混合气体中二氧化硫的体积分数为_______ 。(用含m的代数式表示)
Ⅰ.甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。

(2)若按气体从左到右的流向,气体流经的各装置连接顺序是
(3)E中干燥管的作用是
(4)证明混合气体中含有H2的实验现象为
Ⅱ.乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。
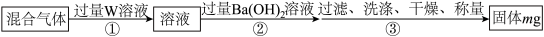
A.H2O2溶液 B.酸性KMnO4溶液 C.溴水 D.稀硫酸
该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
名校
2 . H2O2广泛应用于化学品合成、纸浆和纺织品的漂白,是环保型液体漂白剂。有研究表明,H2O2溶液的漂白性是 所致。
所致。
资料: 和H2O2可以发生反应:
和H2O2可以发生反应: 。
。
(1) H2O2___________ (填“是”或“不是”)直线型分子,其电子式可表示为___________ 。
(2) H2O2溶液显弱酸性,测得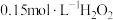 溶液pH约为6.写出H2O2第一步电离方程式:
溶液pH约为6.写出H2O2第一步电离方程式:___________ 。
(3)其他条件相同时,研究不同初始pH条件下H2O2溶液的漂白效果,结果如图:___________ 。
(4)实验发现:若pH>11,则H2O2溶液的漂白效果随pH增大而降低。针对这一现象,继续进行实验,测定不同初始pH条件下,初始浓度均为 的H2O2溶液发生分解反应,结果如表:
的H2O2溶液发生分解反应,结果如表:
①用离子方程式解释1小时后pH没有明显变化的原因:___________ 。
②分析pH过大,H2O2溶液漂白效果会降低的原因:___________ 。
(5)为验证 对H2O2分解的催化作用,该小组向四支盛有
对H2O2分解的催化作用,该小组向四支盛有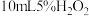 的试管中滴加不同溶液,实验记录如表:
的试管中滴加不同溶液,实验记录如表:
实验Ⅲ和实验Ⅳ过程中都观察到有白色沉淀(CuCl)生成,反应的机理表示为:
i.
ii.___________ 。
反应速率:反应i<反应ii
气泡速率从Ⅱ到Ⅳ依次加快的原因:___________ 。
 所致。
所致。资料:
 和H2O2可以发生反应:
和H2O2可以发生反应: 。
。(1) H2O2
(2) H2O2溶液显弱酸性,测得
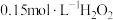 溶液pH约为6.写出H2O2第一步电离方程式:
溶液pH约为6.写出H2O2第一步电离方程式:(3)其他条件相同时,研究不同初始pH条件下H2O2溶液的漂白效果,结果如图:

(4)实验发现:若pH>11,则H2O2溶液的漂白效果随pH增大而降低。针对这一现象,继续进行实验,测定不同初始pH条件下,初始浓度均为
 的H2O2溶液发生分解反应,结果如表:
的H2O2溶液发生分解反应,结果如表:| 初始pH | pH=6 | pH=10 | pH=12 |
初始 浓度 浓度 |  |  |  |
1小时后 浓度 浓度 |  | 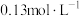 | 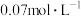 |
| 1小时后pH | pH=6 | pH约为10 | pH约为12 |
②分析pH过大,H2O2溶液漂白效果会降低的原因:
(5)为验证
 对H2O2分解的催化作用,该小组向四支盛有
对H2O2分解的催化作用,该小组向四支盛有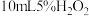 的试管中滴加不同溶液,实验记录如表:
的试管中滴加不同溶液,实验记录如表:| 试管 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 滴加试剂 | 2滴1mol/LNaCl | 2滴 | 2滴 和2滴1mol/LNaCl 和2滴1mol/LNaCl | 2滴 和4滴1mol/LNaCl 和4滴1mol/LNaCl |
| 现象 | 无气泡产生 | 均产生气泡,且气泡速率从Ⅱ到Ⅳ依次加快 | ||
i.

ii.
反应速率:反应i<反应ii
气泡速率从Ⅱ到Ⅳ依次加快的原因:
您最近一年使用:0次
2023-10-06更新
|
161次组卷
|
2卷引用:湖南师范大学附属中学2024届高三上学期月考(二) 化学试题
名校
解题方法
3 . 某化学兴趣小组的同学探究FeCl3溶液是否能做催化剂以加速H2O2溶液的分解,做了以下探究。
(1)请你帮助他们完成实验报告:
(2)已知FeCl3在水中可电离出Fe3+和Cl-,同学们提出以下猜想。甲同学的猜想:FeCl3溶液中的Fe3+起催化作用;
乙同学的猜想:FeCl3溶液中的Cl-起催化作用。
对这两个猜想用实验进行了探究。请你仔细分析后完成下表:
(1)请你帮助他们完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 实验1:在一支试管中加入5mL5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管 | FeCl3溶液可以催化H2O2分解 |
乙同学的猜想:FeCl3溶液中的Cl-起催化作用。
对这两个猜想用实验进行了探究。请你仔细分析后完成下表:
| 实验过程 | 实验现象 | 实验结论 |
| 实验2:向盛有5mL5%的H2O2溶液的试管中加入少量的 | 无明显现象 | |
| 实验3:向盛有5mL5%的H2O2溶液的试管中加入少量的 | 同实验1 |
您最近一年使用:0次
4 . 染料化工企业产生的废水中含有高浓度的氨氮(氨和铵盐)成分,直接排放会造成环境污染。实验小组探索下列方法对氨氮废水进行处理。

(1)实验室检测上述废水中是否含有氨氮的方法是___ 。
(2)“吹脱”步骤中,在废水池的底部吹入大量热气泡,其目的是___ 。
(3)“氧化”步骤中加入了微生物,NH3被氧化为N2。反应的化学方程式为___ 。
(4)“沉淀"步骤中将剩余的NH3·H2O转化为NH4MgPO4•6H2O沉淀,发生反应的离子方程式为___ 。NH4MgPO4•6H2O在农业生产中具有重要应用价值,其原因是___ 。

(1)实验室检测上述废水中是否含有氨氮的方法是
(2)“吹脱”步骤中,在废水池的底部吹入大量热气泡,其目的是
(3)“氧化”步骤中加入了微生物,NH3被氧化为N2。反应的化学方程式为
(4)“沉淀"步骤中将剩余的NH3·H2O转化为NH4MgPO4•6H2O沉淀,发生反应的离子方程式为
您最近一年使用:0次
2020-07-18更新
|
183次组卷
|
2卷引用:湖南省益阳市桃江县2022-2023学年高一下学期7月期末考试化学试题
5 . 小云同学对烧煮食物的某种固体酒精产生了浓厚的兴趣,于是她进行了以下探究活动。
【提出问题】:固体酒精是固态的酒精吗?
【查阅资料一】:酒精,学名乙醇,化学式为C2H6O,熔点为-114.1℃,沸点为78.5℃,易溶于水,能与水以任意比互溶。
【得出结论】:小云认为固体酒精不是固态的酒精,理由是:___ 。
【实验探究Ⅰ】:取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残余了少量白色固体。
【提出新问题】:白色固体究竟是什么呢?
【查阅资料二】:由硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,酒精填充在硬脂酸钠骨架间隙中即得到固体酒精。固体酒精在较高的温度下燃烧时,硬脂酸钠可完全转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水。
【实验探究Ⅱ】:请你完成以下实验报告。
实验结论:小云认为该白色固体为___ 。
【联想与解释】小云联想到老师用玻璃导管将纯净的氢气导出并点燃时,燃烧火焰为黄色,其原因可能是:___ 。
【提出问题】:固体酒精是固态的酒精吗?
【查阅资料一】:酒精,学名乙醇,化学式为C2H6O,熔点为-114.1℃,沸点为78.5℃,易溶于水,能与水以任意比互溶。
【得出结论】:小云认为固体酒精不是固态的酒精,理由是:
【实验探究Ⅰ】:取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残余了少量白色固体。
【提出新问题】:白色固体究竟是什么呢?
【查阅资料二】:由硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,酒精填充在硬脂酸钠骨架间隙中即得到固体酒精。固体酒精在较高的温度下燃烧时,硬脂酸钠可完全转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水。
【实验探究Ⅱ】:请你完成以下实验报告。
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 用铂丝蘸取该固体在酒精灯上灼烧。 | 火焰呈黄色 | 固体中含有Na+ |
| ② | 将该固体置于足量蒸馏水中。 | 固体全部溶解。 | 固体可溶于水。 |
| ③ | 取少量①所得溶液,滴加紫色石蕊试液,振荡。 | 溶液变蓝。 | 溶液为碱性。 |
| ④ | (不填) |
实验结论:小云认为该白色固体为
【联想与解释】小云联想到老师用玻璃导管将纯净的氢气导出并点燃时,燃烧火焰为黄色,其原因可能是:
您最近一年使用:0次
11-12高三上·湖南·阶段练习
6 . 某实验小组利用如下图所示装置完成有关实验。
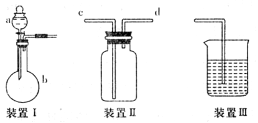
(1) 有关气体的制取、收集、尾气处理问题
①仪器a的名称:__________ ,若装置I用于制取SO2,则反应的化学方程式为: __________ ;装置III可用于气体的吸收,若用于吸收Cl2,则IH中所盛放液体为____________________
A.水 B.浓硫酸 C.NaOH溶液 D.饱和NaCl溶液
②装置II可以是收集装置也可以是洗气装置.若用来收集N0,请简述其操作方法:____________________
(2) 比较碳、硅两种元素的非金属性强弱(a中装的盐酸、装置II中装有Na2SiO3溶液)
则装置II中盛放的溶液为____________________
装置III中反应的离子方程式为____________________

(1) 有关气体的制取、收集、尾气处理问题
①仪器a的名称:
A.水 B.浓硫酸 C.NaOH溶液 D.饱和NaCl溶液
②装置II可以是收集装置也可以是洗气装置.若用来收集N0,请简述其操作方法:
(2) 比较碳、硅两种元素的非金属性强弱(a中装的盐酸、装置II中装有Na2SiO3溶液)
则装置II中盛放的溶液为
装置III中反应的离子方程式为
您最近一年使用:0次



