名校
解题方法
1 . 磺酰氯( )为无色发烟液体,熔点
)为无色发烟液体,熔点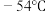 ,沸点69℃,极易水解,遇潮湿空气会产生白雾,其水解时两个氯原子被羟基所取代。磺酰氯在工业上可用作氯化剂,长期放置会分解,磺酰氯可以按如下流程制备或转化。
,沸点69℃,极易水解,遇潮湿空气会产生白雾,其水解时两个氯原子被羟基所取代。磺酰氯在工业上可用作氯化剂,长期放置会分解,磺酰氯可以按如下流程制备或转化。
(1)磺酰氯分子的结构式为___________ ,其水解后产物的化学式为___________ 。
(2)下列说法正确的是___________。
(3) 和等物质的量的乙醇发生取代反应,生成A和一种氢化物,写出该反应的化学方程式
和等物质的量的乙醇发生取代反应,生成A和一种氢化物,写出该反应的化学方程式___________ 。
(4)设计实验方案证明磺酰氯中含有氯元素:向水中加入少量 ,振荡、静置得到无色溶液;取少量溶液于试管中,
,振荡、静置得到无色溶液;取少量溶液于试管中,___________ 。
 )为无色发烟液体,熔点
)为无色发烟液体,熔点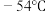 ,沸点69℃,极易水解,遇潮湿空气会产生白雾,其水解时两个氯原子被羟基所取代。磺酰氯在工业上可用作氯化剂,长期放置会分解,磺酰氯可以按如下流程制备或转化。
,沸点69℃,极易水解,遇潮湿空气会产生白雾,其水解时两个氯原子被羟基所取代。磺酰氯在工业上可用作氯化剂,长期放置会分解,磺酰氯可以按如下流程制备或转化。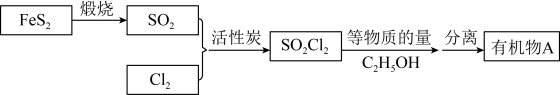
已知: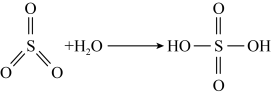
(1)磺酰氯分子的结构式为
(2)下列说法正确的是___________。
A. 、活性炭、氯水都能使红墨水褪色,其原理相同 、活性炭、氯水都能使红墨水褪色,其原理相同 |
B. 煅烧所生成的含铁化合物主要是 煅烧所生成的含铁化合物主要是 |
C. 和 和 在制备磺酰氯前,均可用浓硫酸干燥 在制备磺酰氯前,均可用浓硫酸干燥 |
| D.磺酰氯久置后呈现黄色是因为分解产生的氯气溶解在其中 |
(3)
 和等物质的量的乙醇发生取代反应,生成A和一种氢化物,写出该反应的化学方程式
和等物质的量的乙醇发生取代反应,生成A和一种氢化物,写出该反应的化学方程式(4)设计实验方案证明磺酰氯中含有氯元素:向水中加入少量
 ,振荡、静置得到无色溶液;取少量溶液于试管中,
,振荡、静置得到无色溶液;取少量溶液于试管中,
您最近一年使用:0次
名校
2 . 氯气和亚氯酸钠(NaClO2)都是重要的漂白剂。
(I)某小组以KMnO4和浓盐酸为原料制备干燥、纯净的氯气___________ 。
(2)制备氯气时,可选用的发生装置为___________ (填序号),选择上述合适的装置,其连接顺序为:发生装置→___________ →i(按气流方向,用小写字母表示)。
(3)F装置所盛溶液是___________ (填溶液名称)。
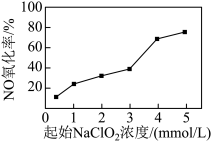
(II)工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得,实验流程如下:___________ 。
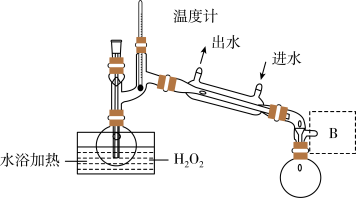
(5)已知H2O2(沸点150℃)浓度对反应速率有影响。通过下图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是___________ 。___________ 。
(I)某小组以KMnO4和浓盐酸为原料制备干燥、纯净的氯气
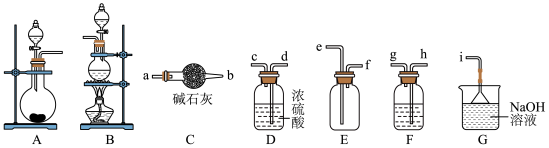
(2)制备氯气时,可选用的发生装置为
(3)F装置所盛溶液是
(II)工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得,实验流程如下:

(5)已知H2O2(沸点150℃)浓度对反应速率有影响。通过下图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是
您最近一年使用:0次
3 . Ⅰ.按要求回答下列问题:
(1)下列物质中① ;②乙醇;③熔融
;②乙醇;③熔融 ;④
;④ 溶液;⑤固态
溶液;⑤固态 ,其中属于电解质的是
,其中属于电解质的是___________ (只填序号,下同),属于非电解质的是___________ 。所给状态下能导电的是___________ 。
(2)配平方程式,并在方程式上用双线桥表示出电子转移情况。____________ 。

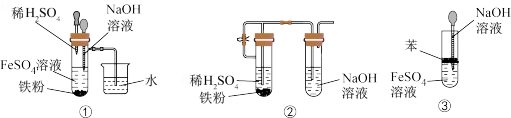
Ⅱ.下图所示装置,可用来制取 和观察
和观察 在空气中被氧化的颜色变化。实验时必须使用铁屑和
在空气中被氧化的颜色变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。
的硫酸,其他试剂任选。
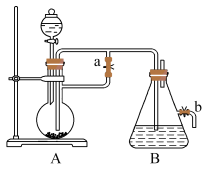
(3)实验开始时应先将活塞a___________ (填“打开”或“关闭”)。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为___________ 。
(5)下图中___________ 装置能较长时间看到 白色沉淀(填装置序号)。
白色沉淀(填装置序号)。
(1)下列物质中①
 ;②乙醇;③熔融
;②乙醇;③熔融 ;④
;④ 溶液;⑤固态
溶液;⑤固态 ,其中属于电解质的是
,其中属于电解质的是(2)配平方程式,并在方程式上用双线桥表示出电子转移情况。

Ⅱ.下图所示装置,可用来制取
 和观察
和观察 在空气中被氧化的颜色变化。实验时必须使用铁屑和
在空气中被氧化的颜色变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。
的硫酸,其他试剂任选。
(3)实验开始时应先将活塞a
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为
(5)下图中
 白色沉淀(填装置序号)。
白色沉淀(填装置序号)。
您最近一年使用:0次
名校
解题方法
4 .  溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有
溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有 。由该酸性废液X回收
。由该酸性废液X回收 的流程如图所示。下列说法中
的流程如图所示。下列说法中不正确 的是
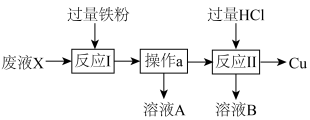
 溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有
溶液是一种铜电路板的蚀刻剂,蚀刻后的废液经过检测其中含有 。由该酸性废液X回收
。由该酸性废液X回收 的流程如图所示。下列说法中
的流程如图所示。下列说法中
A.废液X中一定存在 |
| B.“反应I”中有1种或2种氧化剂与铁粉反应 |
| C.“操作a”为过滤 |
| D.收集溶液A、B,再通入足量氯气,可实现蚀刻剂的再生 |
您最近一年使用:0次
2023-11-19更新
|
296次组卷
|
4卷引用:浙江省浙南名校2023-2024学年高一下学期开学化学试题
5 . FeCl3能用于金属蚀刻、污水处理、印染工业。某化学研究性学习小组模拟工业生产流程制备氯化铁并对产物做如下探究实验(部分夹持装置省略)。

已知:三氯化铁易升华,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。
(1)A中装浓HCl的仪器名称___________ ,D中装碱石灰的仪器名称___________ 。
(2)实验中制取氯气的离子方程式为___________ 。
(3)装置的连接顺序为:a→_________ →f。
(4)实验结束时,先移走_________ (选“A”或“B”)处的酒精灯。
(5)碱石灰的作用是___________ 。
(6)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

用离子方程式表示淡红色溶液中加入过量H2O2后,溶液颜色变深的原因有:
a:____________________ ;
b:

已知:三氯化铁易升华,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。
(1)A中装浓HCl的仪器名称
(2)实验中制取氯气的离子方程式为
(3)装置的连接顺序为:a→
(4)实验结束时,先移走
(5)碱石灰的作用是
(6)实验结束并冷却后,将收集器中的固体物质转移至锥形瓶中,进行如下实验:

用离子方程式表示淡红色溶液中加入过量H2O2后,溶液颜色变深的原因有:
a:
b:

您最近一年使用:0次
名校
6 . 我国力争2060年前实现碳中和,利用NaOH溶液按如下流程捕捉回收CO2可以减少碳排放。
(1)下列说法正确的是___________。
(2)研究表明一水草酸钙(CaC2O4·H2O)热分解制得的CaO疏松多孔也可以捕捉回收CO2,写出一水草酸钙分解的反应方程式___________ 。
(3)工业上利用捕捉到的CO2可以制备Na2CO3,工艺流程图如下:___________ 。
②产品Na2CO3中含有NaHCO3,下列方案中不能测定Na2CO3质量分数的是___________ 。
A.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b克固体
B.取a克混合物与足量稀盐酸充分反应,逸出气体用碱石灰吸收,质量增加b克
C.取a克混合物与足量NaOH溶液充分反应,加热、蒸干、灼烧,得到b克固体
D.取a克混合物与足量Ca(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
③产品Na2CO3中含有NaHCO3,如果用加热分解的方法测定产品中碳酸氢钠的质量分数。加热质量为m1g的该产品,最终测得剩余固体质量为m2g。则产品中碳酸氢钠的质量百分数可表示为___________ (用字母m1和m2表示)。
(4)实验室探究钠与CO2反应的过程中,发现钠在CO2中剧烈燃烧,并产生大量白烟和黑色固体,写出可能发生反应的方程式___________ 。

(1)下列说法正确的是___________。
| A.为了充分吸收CO2,捕捉室中NaOH溶液常喷成雾状 |
| B.捕捉室中反应生成的产物为Na2CO3 |
| C.整个过程中,发生的化学反应无氧化还原反应 |
| D.整个过程中,可以循环利用的物质只有CaO |
(2)研究表明一水草酸钙(CaC2O4·H2O)热分解制得的CaO疏松多孔也可以捕捉回收CO2,写出一水草酸钙分解的反应方程式
(3)工业上利用捕捉到的CO2可以制备Na2CO3,工艺流程图如下:

②产品Na2CO3中含有NaHCO3,下列方案中不能测定Na2CO3质量分数的是
A.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b克固体
B.取a克混合物与足量稀盐酸充分反应,逸出气体用碱石灰吸收,质量增加b克
C.取a克混合物与足量NaOH溶液充分反应,加热、蒸干、灼烧,得到b克固体
D.取a克混合物与足量Ca(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
③产品Na2CO3中含有NaHCO3,如果用加热分解的方法测定产品中碳酸氢钠的质量分数。加热质量为m1g的该产品,最终测得剩余固体质量为m2g。则产品中碳酸氢钠的质量百分数可表示为
(4)实验室探究钠与CO2反应的过程中,发现钠在CO2中剧烈燃烧,并产生大量白烟和黑色固体,写出可能发生反应的方程式
您最近一年使用:0次
2023-10-07更新
|
74次组卷
|
2卷引用:浙江省杭州市四校2023-2024学年高一上学期10月联考化学试题
名校
解题方法
7 . 某实验小组用如图装置制备无水FeCl3。
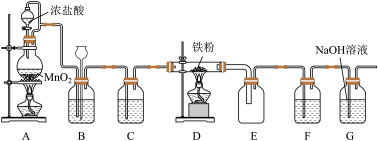
已知:FeCl3固体易升华,易吸收水分变质。
请回答:
(1)装置A中有分液漏斗,分液漏斗在使用前应该先______ 。
(2)装置B的作用是______ 。
(3)实验中有两处需要加热,点燃酒精灯的顺序是______ 。
(4)有同学提出装置F和G可以用一个球形干燥管来代替,球形干燥管中所装试剂的名称是_____ 。
(5)待反应停止,装置冷却后,取出D中少量固体,加入足量稀盐酸溶解,检验该溶液中是否含有Fe3+的方法是______ 。

已知:FeCl3固体易升华,易吸收水分变质。
请回答:
(1)装置A中有分液漏斗,分液漏斗在使用前应该先
(2)装置B的作用是
(3)实验中有两处需要加热,点燃酒精灯的顺序是
(4)有同学提出装置F和G可以用一个球形干燥管来代替,球形干燥管中所装试剂的名称是
(5)待反应停止,装置冷却后,取出D中少量固体,加入足量稀盐酸溶解,检验该溶液中是否含有Fe3+的方法是
您最近一年使用:0次
名校
解题方法
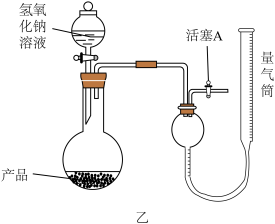
8 . 某兴趣小组的同学设计的用 与Mg反应制备少量单质硅的实验流程如下:
与Mg反应制备少量单质硅的实验流程如下:

已知:① (易自燃)。
(易自燃)。
②量气管的刻度上端为0,下端为50.00mL。
回答下列问题:
(1)用于盛装 与镁粉反应的坩埚的材质适宜为
与镁粉反应的坩埚的材质适宜为___________ (填“陶瓷”“玻璃”或“铁”)。
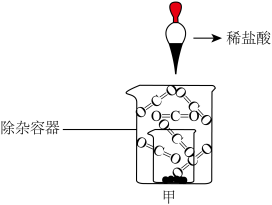
(2)步骤②的除杂装置如图甲所示,除杂必须在 气氛中的原因是
气氛中的原因是___________ ,将步骤①反应后的固体冷却并迅速转移至小烧杯中,加入足量盐酸,反应完成时的现象是___________ 。
(3)测定产品中硅的纯度(利用Si与NaOH溶液反应产生氢气的体积进行换算):
①该反应的化学方程式为___________ 。
②称取一定量的产品硅,加入圆底烧瓶中,如图乙所示,向其中加入足量NaOH溶液,测量产生氢气的体积涉及如下步骤,正确的顺序是___________ (填字母)。
a.读数 b.冷却到室温 c.调节使量气管液面与球形漏斗中的液面相平
③称取wg产品,利用装置乙测定产品纯度,反应前量气管液面读数为 ,反应后量气管液面读数为
,反应后量气管液面读数为 (实验数据均转化为标准状况下),则产品的纯度为
(实验数据均转化为标准状况下),则产品的纯度为___________ (列出计算式)。
 与Mg反应制备少量单质硅的实验流程如下:
与Mg反应制备少量单质硅的实验流程如下:
已知:①
 (易自燃)。
(易自燃)。②量气管的刻度上端为0,下端为50.00mL。
回答下列问题:
(1)用于盛装
 与镁粉反应的坩埚的材质适宜为
与镁粉反应的坩埚的材质适宜为(2)步骤②的除杂装置如图甲所示,除杂必须在
 气氛中的原因是
气氛中的原因是
(3)测定产品中硅的纯度(利用Si与NaOH溶液反应产生氢气的体积进行换算):
①该反应的化学方程式为
②称取一定量的产品硅,加入圆底烧瓶中,如图乙所示,向其中加入足量NaOH溶液,测量产生氢气的体积涉及如下步骤,正确的顺序是
a.读数 b.冷却到室温 c.调节使量气管液面与球形漏斗中的液面相平
③称取wg产品,利用装置乙测定产品纯度,反应前量气管液面读数为
 ,反应后量气管液面读数为
,反应后量气管液面读数为 (实验数据均转化为标准状况下),则产品的纯度为
(实验数据均转化为标准状况下),则产品的纯度为
您最近一年使用:0次
名校
9 . 氯酸锶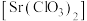 白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:

(1)仪器b的名称是___________ 。
(2)A中发生反应的离子方程式为___________ 。
(3)装置B中所装试剂名称为:___________ ,其作用是___________ 。
(4)装置C中搅拌的目的是___________ ;发生反应的化学方程式为___________ 。
(5)装置D的作用___________ ;反应一段时间后,可观察到装置D中红色逐渐褪去,某实验小组的同学对红色突然褪去的原因进行猜想:
猜想一:氯水中的酸或氯分子与NaOH发生反应,将NaOH消耗所致
猜想二:氯水中次氯酸的强氧化性,使红色褪去所致。
假如猜想一成立,请设计实验证明该猜想红色褪去的原因:___________ 。
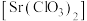 白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
(1)仪器b的名称是
(2)A中发生反应的离子方程式为
(3)装置B中所装试剂名称为:
(4)装置C中搅拌的目的是
(5)装置D的作用
猜想一:氯水中的酸或氯分子与NaOH发生反应,将NaOH消耗所致
猜想二:氯水中次氯酸的强氧化性,使红色褪去所致。
假如猜想一成立,请设计实验证明该猜想红色褪去的原因:
您最近一年使用:0次
2023-02-28更新
|
114次组卷
|
2卷引用:浙江省台州市路桥中学2023-2024学年高一上学期10月月考化学试题
解题方法
10 . 某兴趣小组在实验室用下图装置(夹持仪器已省略)制备无水 。
。

已知: 易潮解,300℃左右时升华。请回答:
易潮解,300℃左右时升华。请回答:
(1)仪器Ⅰ的名称_______ :为了更好地收集 ,装置E应采用
,装置E应采用_______ 水浴(填“热”或“冷”)。
(2)本实验合理的操作步骤:按上图连接仪器→_______ 。(按操作顺序选择序号)。
①添加药品 ②检查装置气密性 ③点燃A处酒精灯 ④点燃D处酒精灯 ⑤使D中硬质玻璃管内充满黄绿色气体
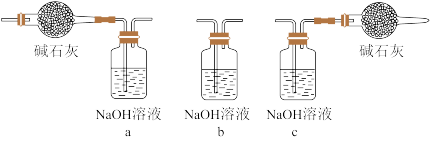
(3)将上图中装置组装完整,虚框F应选用_______ 。
(4)为了保证仪器Ⅰ中液体顺利流下,应采用的操作是_______ 。
(5)反应结束后,在硬质玻璃管中有固体残留,同学们进行如下实验探究,你认为正确的是_______。
 。
。
已知:
 易潮解,300℃左右时升华。请回答:
易潮解,300℃左右时升华。请回答:(1)仪器Ⅰ的名称
 ,装置E应采用
,装置E应采用(2)本实验合理的操作步骤:按上图连接仪器→
①添加药品 ②检查装置气密性 ③点燃A处酒精灯 ④点燃D处酒精灯 ⑤使D中硬质玻璃管内充满黄绿色气体
(3)将上图中装置组装完整,虚框F应选用

(4)为了保证仪器Ⅰ中液体顺利流下,应采用的操作是
(5)反应结束后,在硬质玻璃管中有固体残留,同学们进行如下实验探究,你认为正确的是_______。
| A.取少量固体加水溶解,若不能溶解,则说明有铁残留 |
| B.取少量固体加水溶解,若全部溶解,则说明无铁残留 |
| C.取少量固体溶于足量的盐酸,先滴加3滴KSCN溶液,若溶液呈血红色,则说明只有氯化铁残留 |
| D.取少量固体溶于水中,先滴加3滴KSCN溶液无明显现象,再滴加少量新制氯水溶液呈血红色,则说明铁、氯化铁都有残留 |
您最近一年使用:0次



