1 . 我国的歼-20战机使用了大量的钛金属, 是生产钛的重要中间原料,实验室用如下装置制备
是生产钛的重要中间原料,实验室用如下装置制备 (夹持装置略去)。
(夹持装置略去)。 溶液反应产生黑色金属钯。
溶液反应产生黑色金属钯。
②有关物质的性质。
请回答下列问题:
(1)装置A中a的作用是_______ ,A中制 的离子方程式为
的离子方程式为_______ 。
(2)装置C中的药品为_______ ,装置E用冰盐水浴的目的是_______ 。
(3)装置D中发生两个反应,其中副反应为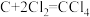 ,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应的化学方程式
,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应的化学方程式_______ 。
(4)进一步提纯E中产物的方法是_______(填编号)。
(5)测定产品纯度:准确量取3.4g产品,配成250mL含 的溶液,取25.00mL该溶液,加入还原剂将
的溶液,取25.00mL该溶液,加入还原剂将 全部转化为
全部转化为 ,再加入指示剂,用
,再加入指示剂,用 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为。重复操作2~3次,消耗标准溶液平均体积为17.00mL。
氧化为。重复操作2~3次,消耗标准溶液平均体积为17.00mL。
①滴定时所用的指示剂为_______ (填标号)。
A.酚酞溶液 B.甲基橙 C.KSCN溶液 D. 溶液
溶液
②产品中 的纯度为
的纯度为_______ 。
 是生产钛的重要中间原料,实验室用如下装置制备
是生产钛的重要中间原料,实验室用如下装置制备 (夹持装置略去)。
(夹持装置略去)。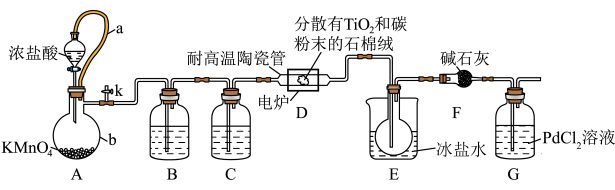
 溶液反应产生黑色金属钯。
溶液反应产生黑色金属钯。②有关物质的性质。
| 熔点/℃ | 沸点/℃ | 密度 | 水溶性 | |
 | -24 | 136.4 | 1.7 | 遇水极易水解,同时出现白雾 |
 | -23 | 76.8 | 1.6 | 难溶于水,与 互溶 互溶 |
(1)装置A中a的作用是
 的离子方程式为
的离子方程式为(2)装置C中的药品为
(3)装置D中发生两个反应,其中副反应为
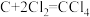 ,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应的化学方程式
,主反应中氧化剂与还原剂的物质的量相等且只有两种产物,写出主反应的化学方程式(4)进一步提纯E中产物的方法是_______(填编号)。
| A.过滤 | B.蒸发 | C.蒸馏 | D.分液 |
(5)测定产品纯度:准确量取3.4g产品,配成250mL含
 的溶液,取25.00mL该溶液,加入还原剂将
的溶液,取25.00mL该溶液,加入还原剂将 全部转化为
全部转化为 ,再加入指示剂,用
,再加入指示剂,用 标准溶液滴定至终点,将
标准溶液滴定至终点,将 氧化为。重复操作2~3次,消耗标准溶液平均体积为17.00mL。
氧化为。重复操作2~3次,消耗标准溶液平均体积为17.00mL。①滴定时所用的指示剂为
A.酚酞溶液 B.甲基橙 C.KSCN溶液 D.
 溶液
溶液②产品中
 的纯度为
的纯度为
您最近一年使用:0次
2 .  大量排放造成环境污染,以
大量排放造成环境污染,以 还原
还原 的的选择性催化还原(
的的选择性催化还原( )技术广泛应用于烟气(含NO、
)技术广泛应用于烟气(含NO、 、
、 等)脱硝。
等)脱硝。
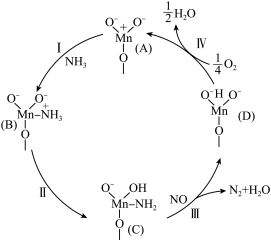
(1)以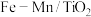 催化的
催化的 反应机理如图所示,
反应机理如图所示, 反应的化学方程式为:
反应的化学方程式为:___________ 。
(2)以 催化的
催化的 。
。
①催化剂的制备。将预先制备的一定量的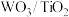 粉末置于80℃的水中,在搅拌下加入一定量的
粉末置于80℃的水中,在搅拌下加入一定量的 溶液,经蒸发、焙烧等工序得到颗粒状
溶液,经蒸发、焙烧等工序得到颗粒状 催化剂。在水溶液中
催化剂。在水溶液中 水解为
水解为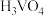 沉淀的离子方程式为
沉淀的离子方程式为___________ ;反应选用 溶液而不选用
溶液而不选用 溶液的原因是
溶液的原因是___________ 。
②催化剂的应用。将一定物质的量浓度的NO、 、
、 (其余为
(其余为 )气体匀速通过装有
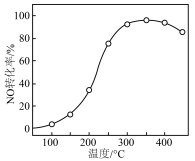
)气体匀速通过装有 催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是___________ ;反应温度高于380℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有___________ (用化学方程式表示)。
③废催化剂的回收。回收 并制备
并制备 的过程如下图所示:
的过程如下图所示:
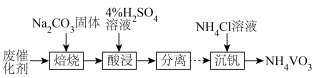
酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有___________ 。
 大量排放造成环境污染,以
大量排放造成环境污染,以 还原
还原 的的选择性催化还原(
的的选择性催化还原( )技术广泛应用于烟气(含NO、
)技术广泛应用于烟气(含NO、 、
、 等)脱硝。
等)脱硝。
(1)以
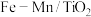 催化的
催化的 反应机理如图所示,
反应机理如图所示, 反应的化学方程式为:
反应的化学方程式为:(2)以
 催化的
催化的 。
。①催化剂的制备。将预先制备的一定量的
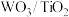 粉末置于80℃的水中,在搅拌下加入一定量的
粉末置于80℃的水中,在搅拌下加入一定量的 溶液,经蒸发、焙烧等工序得到颗粒状
溶液,经蒸发、焙烧等工序得到颗粒状 催化剂。在水溶液中
催化剂。在水溶液中 水解为
水解为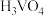 沉淀的离子方程式为
沉淀的离子方程式为 溶液而不选用
溶液而不选用 溶液的原因是
溶液的原因是②催化剂的应用。将一定物质的量浓度的NO、
 、
、 (其余为
(其余为 )气体匀速通过装有
)气体匀速通过装有 催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是
③废催化剂的回收。回收
 并制备
并制备 的过程如下图所示:
的过程如下图所示:
酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有
您最近一年使用:0次
3 . 化学工业为疫情防控提供了强有力的物质支撑。次氯酸溶液是常用的消毒剂,可利用Cl2O与水反应得到。根据该原理,某化学兴趣小组利用如下装置制备一定浓度的次氯酸溶液。已知:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42℃以上会分解为Cl2和O2。实验时,将氯气和空气(不参与反应)按体积比为1:3混合通入含水8%的碳酸钠糊状物中,请回答下列问题:
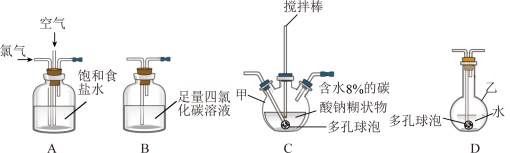
(1)实验室一般通过MnO2与浓盐酸加热制备氯气,发生反应的离子方程式为_______ 。
(2)装置C中的仪器甲的名称为_______ ,仪器甲中发生反应的化学方程式为_______ ,为了提高 的产率,需控制反应在合适的温度,可采取的操作为
的产率,需控制反应在合适的温度,可采取的操作为_______ 。
(3)装置 的作用为
的作用为_______ ,有同学建议将装置 中的仪器乙换为棕色瓶,原因是
中的仪器乙换为棕色瓶,原因是_______ 。
(4)测定装置D中得到的次氯酸的物质的量浓度。量取 装置D中得到的次氯酸溶液,并稀释至
装置D中得到的次氯酸溶液,并稀释至 ,再从中取出
,再从中取出 至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (滴定反应为
(滴定反应为 )。
)。
①次氯酸与KI溶液反应时氧化剂与还原剂的物质的量之比为_______ 。
②达到滴定终点的现象为_______ 。
③装置D中得到的次氯酸的物质的量浓度为_______ mol/L。
④若滴定开始前滴定管尖嘴有气泡,滴定结束后气泡消失,则测定的次氯酸的物质的量浓度将_______ (填“偏低”、“偏高”或“无影响”)。

(1)实验室一般通过MnO2与浓盐酸加热制备氯气,发生反应的离子方程式为
(2)装置C中的仪器甲的名称为
 的产率,需控制反应在合适的温度,可采取的操作为
的产率,需控制反应在合适的温度,可采取的操作为(3)装置
 的作用为
的作用为 中的仪器乙换为棕色瓶,原因是
中的仪器乙换为棕色瓶,原因是(4)测定装置D中得到的次氯酸的物质的量浓度。量取
 装置D中得到的次氯酸溶液,并稀释至
装置D中得到的次氯酸溶液,并稀释至 ,再从中取出
,再从中取出 至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
至锥形瓶中,并加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (滴定反应为
(滴定反应为 )。
)。①次氯酸与KI溶液反应时氧化剂与还原剂的物质的量之比为
②达到滴定终点的现象为
③装置D中得到的次氯酸的物质的量浓度为
④若滴定开始前滴定管尖嘴有气泡,滴定结束后气泡消失,则测定的次氯酸的物质的量浓度将
您最近一年使用:0次
4 . 以工厂烟气中的 为原料制备脱氯剂
为原料制备脱氯剂 。
。
(1) 制备。边搅拌边向
制备。边搅拌边向 溶液中通入
溶液中通入 。
。
① 溶液中通入
溶液中通入 得到
得到 ,其离子方程式为
,其离子方程式为_______ 。
② 溶液中
溶液中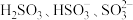 随
随 的分布下图所示。确定何时停止通
的分布下图所示。确定何时停止通 的操作为
的操作为_______ 。

(2) 制备。请补充完整由S和
制备。请补充完整由S和 溶液制备
溶液制备 的实验方案:向过量硫磺粉中加入
的实验方案:向过量硫磺粉中加入 溶液,加热充分反应,
溶液,加热充分反应,_______ ,低温干燥得产品。[实验中必须使用的试剂:无水乙醇]
(3)废水中 的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的
的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的 溶液,充分反应后加入2~3滴淀粉溶液,然后用
溶液,充分反应后加入2~3滴淀粉溶液,然后用 标准溶液滴定。已知:
标准溶液滴定。已知: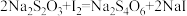 。
。

①滴定达到终点时的实验现象是_______ 。
②若滴定过程中滴定管中的液面如图所示,则a=_______  。
。
 为原料制备脱氯剂
为原料制备脱氯剂 。
。(1)
 制备。边搅拌边向
制备。边搅拌边向 溶液中通入
溶液中通入 。
。①
 溶液中通入
溶液中通入 得到
得到 ,其离子方程式为
,其离子方程式为②
 溶液中
溶液中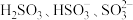 随
随 的分布下图所示。确定何时停止通
的分布下图所示。确定何时停止通 的操作为
的操作为
(2)
 制备。请补充完整由S和
制备。请补充完整由S和 溶液制备
溶液制备 的实验方案:向过量硫磺粉中加入
的实验方案:向过量硫磺粉中加入 溶液,加热充分反应,
溶液,加热充分反应,(3)废水中
 的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的
的测定。取出一定量废水于锥形瓶中,加入足量硫酸酸化的 溶液,充分反应后加入2~3滴淀粉溶液,然后用
溶液,充分反应后加入2~3滴淀粉溶液,然后用 标准溶液滴定。已知:
标准溶液滴定。已知: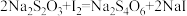 。
。
①滴定达到终点时的实验现象是
②若滴定过程中滴定管中的液面如图所示,则a=
 。
。
您最近一年使用:0次
名校
5 . 聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。该过程中反应温度不宜过高,原因是_______ ;H2O2氧化Fe2+的离子方程式为________ 。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2mol·L−1K2Cr2O7溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将_______ (填“偏大”或“偏小”或“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)_____________ 。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。该过程中反应温度不宜过高,原因是
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2mol·L−1K2Cr2O7溶液滴定至终点(滴定过程中
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将
②计算该样品中铁的质量分数(写出计算过程)
您最近一年使用:0次
6 . 实验室模拟工业生产食品香精菠萝酯( )的简易流程如下:
)的简易流程如下:

有关物质的熔、沸点如表:
试回答下列问题:
(1)反应室I中反应的最佳温度是104℃,为较好地控制温度在102℃~106℃之间,加热时可选用___ (选填字母)。
A.火炉直接加热 B.水浴加热 C.油浴加热
(2)分离室I采取的操作名称是___ 。
(3)反应室I中发生反应的化学方程式是___ 。
(4)分离室II的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是___ (用化学方程式表示)。
 )的简易流程如下:
)的简易流程如下:
有关物质的熔、沸点如表:
| 苯酚 | 氯乙酸 | 苯氧乙酸 | |
| 熔点/℃ | 43 | 62 | 99 |
| 沸点/℃ | 181.9 | 189 | 285 |
试回答下列问题:
(1)反应室I中反应的最佳温度是104℃,为较好地控制温度在102℃~106℃之间,加热时可选用
A.火炉直接加热 B.水浴加热 C.油浴加热
(2)分离室I采取的操作名称是
(3)反应室I中发生反应的化学方程式是
(4)分离室II的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是
您最近一年使用:0次
7 . 阅读下列材料,完成下列小题。
戴维发现Cl2的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。多余的Cl2可用NaOH溶液吸收。液氯用于自来水消毒已成为目前给水系统中最为经济有效的消毒技术,但其消毒后生成的副产物对人体存在健康隐患。ClO2是一种易溶于水的气体,是国际上公认的高效、安全、无毒的绿色消毒剂。
MnCl2+Cl2↑+2H2O。多余的Cl2可用NaOH溶液吸收。液氯用于自来水消毒已成为目前给水系统中最为经济有效的消毒技术,但其消毒后生成的副产物对人体存在健康隐患。ClO2是一种易溶于水的气体,是国际上公认的高效、安全、无毒的绿色消毒剂。
1. 戴维发现Cl2的反应中,还原剂是____
A. MnO2 B. HCl C. MnCl2 D. Cl2
2. 从氧化还原反应的角度分析,下列物质中不 可以替代MnO2的是____
A. O2 B. NaClO3 C. NaClO D. NaCl
3. Cl2被NaOH溶液吸收时会生成NaClO。NaClO属于____
A. 酸 B. 碱 C. 盐 D. 氧化物
4. 下列物质中可以替代NaOH溶液吸收Cl2的是____
A. 石灰乳 B. 食盐水 C. 浓硫酸 D. 稀盐酸
5. 实验室收集ClO2可以采用的方法是____
A. B.
B.  C.
C.  D.
D. 
戴维发现Cl2的反应为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。多余的Cl2可用NaOH溶液吸收。液氯用于自来水消毒已成为目前给水系统中最为经济有效的消毒技术,但其消毒后生成的副产物对人体存在健康隐患。ClO2是一种易溶于水的气体,是国际上公认的高效、安全、无毒的绿色消毒剂。
MnCl2+Cl2↑+2H2O。多余的Cl2可用NaOH溶液吸收。液氯用于自来水消毒已成为目前给水系统中最为经济有效的消毒技术,但其消毒后生成的副产物对人体存在健康隐患。ClO2是一种易溶于水的气体,是国际上公认的高效、安全、无毒的绿色消毒剂。1. 戴维发现Cl2的反应中,还原剂是
A. MnO2 B. HCl C. MnCl2 D. Cl2
2. 从氧化还原反应的角度分析,下列物质中
A. O2 B. NaClO3 C. NaClO D. NaCl
3. Cl2被NaOH溶液吸收时会生成NaClO。NaClO属于
A. 酸 B. 碱 C. 盐 D. 氧化物
4. 下列物质中可以替代NaOH溶液吸收Cl2的是
A. 石灰乳 B. 食盐水 C. 浓硫酸 D. 稀盐酸
5. 实验室收集ClO2可以采用的方法是
A.
 B.
B.  C.
C.  D.
D. 
您最近一年使用:0次
8 . 用离子方程式(不能用离子方程式的用化学方程式)解释下列实验事实
⑴用纸层析法分离Fe3+、Cu2+时,氨熏显色后出现蓝色斑点_______________________________________________________________________ 。
⑵用新制的氢氧化铜检验牙膏中的甘油______________________________________________________________________ 。
⑶用AgNO3溶液、稀硝酸和NaNO2溶液直接检验火柴头中的氯元素_______________________________________________________________________ 。
⑷用水杨酸和乙酸酐在酸性条件下制备阿司匹林________________________________________________________________________ 。
⑴用纸层析法分离Fe3+、Cu2+时,氨熏显色后出现蓝色斑点
⑵用新制的氢氧化铜检验牙膏中的甘油
⑶用AgNO3溶液、稀硝酸和NaNO2溶液直接检验火柴头中的氯元素
⑷用水杨酸和乙酸酐在酸性条件下制备阿司匹林
您最近一年使用:0次
18-19高三上·福建漳州·阶段练习
名校
9 . 硫酸锰在电解锰、染料、造纸以及陶瓷等工业生产中有广泛的应用。利用软锰矿( 主要成分为MnO2,含铁的化合物等杂质)和闪锌矿(主要成分ZnS)制得硫酸锰的流程如下:

(1)“酸浸”时,为了缩短浸取时间,常加入少量FeSO4溶液,FeSO4的作用可能是___________________ ;MnO2、ZnS 及硫酸反应转变为两种硫酸盐的化学方程式为______________________ 。
(2)常温下,Ksp(ZuS) =1.2×l0-24、Ksp(MnS)=1.5×10-15,“沉锌”反应为:Zn2+(aq)+MnS ZnS+Mn2+(aq),该反应的平衡常数K=
ZnS+Mn2+(aq),该反应的平衡常数K=__________________ 。
(3)在强酸性条件下加入MnO2 氧化Fe2+ 的离子方程式为___________________ 。
(4)“除铁”时需要调节pH 约为3~4,过滤所得的滤渣2 中除MnO2 以外的另一种物质是________________ 。(写化学式)
(5)该工艺流程中可以循环利用的物质是____________________ 。

(1)“酸浸”时,为了缩短浸取时间,常加入少量FeSO4溶液,FeSO4的作用可能是
(2)常温下,Ksp(ZuS) =1.2×l0-24、Ksp(MnS)=1.5×10-15,“沉锌”反应为:Zn2+(aq)+MnS
 ZnS+Mn2+(aq),该反应的平衡常数K=
ZnS+Mn2+(aq),该反应的平衡常数K=(3)在强酸性条件下加入MnO2 氧化Fe2+ 的离子方程式为
(4)“除铁”时需要调节pH 约为3~4,过滤所得的滤渣2 中除MnO2 以外的另一种物质是
(5)该工艺流程中可以循环利用的物质是
您最近一年使用:0次
2018-03-04更新
|
582次组卷
|
4卷引用:【南昌新东方】2019 南大附中 高二上 期中
(已下线)【南昌新东方】2019 南大附中 高二上 期中福建省龙海市第二中学2019届高三上学期第二次月考化学试题江苏省无锡市普通高中2018届高三上学期期末考试化学试题甘肃省白银市靖远县第四中学2020届高三12月月考化学试题
名校
10 . 苯乙酸铜是合成优良催化剂、传感材料纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
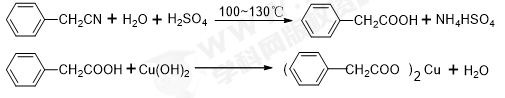

制备苯乙酸的装置如右图所示(加热和夹持装置等略),已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____________________ 。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是______________ ;仪器c的名称是__________ ,其作用是__________________ 。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是_______ 。下列仪器中可用于分离苯乙酸粗品的是___________ (填标号)。
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒


制备苯乙酸的装置如右图所示(加热和夹持装置等略),已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒
您最近一年使用:0次



