11. 某实验小组在电压12V电流3A的条件下电解2mol/L的氯化铜溶液并探究其产物的性质。
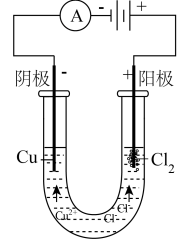
(1)根据电解原理,预测:阴极发生的实验现象是
______。阳极发生的电极反应式为
_______。电解氯化铜溶液总的化学方程式为
_______。
(2)小组同学在实际电解过程中,意外的观察到下表的实验现象:
条件 | 电极 | 现象 |
电压12V
电流3A | 阴极 | 3min后,附近溶液变成棕褐色。30min后,溶液变成深棕褐色。电极底部表面有少量红色金属生成,还有少量白色物质。 |
| 阳极 | 开始出现少量气泡,后来气泡增多。 |
实验小组学生对阴极区产生异常现象的原因进行了探究:
资料1:CuCl是白色的难溶物,用Cu还原CuCl
2溶液可以得到CuCl沉淀,它易溶于浓盐酸,用水稀释CuCl的浓盐酸溶液则又析出CuCl白色沉淀。
资料2:[CuCl
2.CuCl
2(H
2O)]
-(棕褐色)

CuCl+Cu
2++3Cl
-+H
2O。
Ⅰ.探究阴极表面产生的白色物质:
①根据资料写出Cu还原CuCl
2溶液反应的化学方程式
______。
②学生为了确定阴极产物进行实验A:取2mol/L的CuCl
2溶液,加入铜粉,充分振荡,几分钟后,试管底有白色沉淀生成,过滤出白色固体,加入浓盐酸,固体溶解,加水稀释,又析出白色沉淀。
如果要确认阴极产生的白色沉淀是CuCl,还需要进行对照实验B,该实验的设计方案是
______。
实验结论:通过实验A和实验B的对比,可以确定阴极产生的白色固体是CuCl。
Ⅱ.探究阴极区域溶液呈现棕褐色的原因:
猜想1:可能是Cu
2+与高浓度的Cl
-发生络合反应所致。
实验C:向2mol/L的CuCl
2溶液中加入
______,溶液呈现绿色,没有变成棕褐色。
实验结论:溶液颜色呈现棕褐色
______(填“是”或者“不是”)由于Cu
2+与高浓度的Cl
-发生络合反应所致。
猜想2:棕褐色溶液可能与+1价Cu有关。
实验D:用铜粉和2mol/L的CuCl
2溶液反应制备[CuCl
2•CuCl
2(H
2O)],取少量该标准溶液与实验中得到的棕褐色溶液进行对照实验。
步骤一:配制标准[CuCl
2.CuCl
2(H
2O)]
-棕褐色溶液进行稀释,实验流程如图所示:
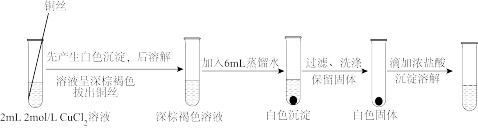
步骤二:取阴极附近的棕褐色溶液,重复上述实验进行对照,请画出对照实验的流程图
______。
实验结论:通过对照实验,确认棕褐色溶液与+1价Cu有关。