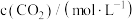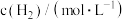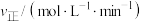CO2的捕集和利用因为其工业价值和减少CO2排放的环境意义而受到广泛关注。
(1)下列物质中可以作为CO2捕获剂的是______ 。
A.NH4Cl B.Na2CO3 C.HOCH2CH2OH D.HOCH2CH2NH2 E.(NH4)2CO3
(2)在Cu/ZnO催化剂条件下,CO2与H2可生成CH3OH,CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
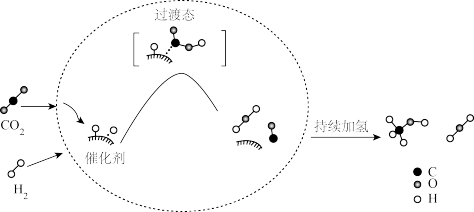
已知:第一步反应I:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ.mol-1
CO(g)+H2O(g) ΔH2=+41kJ.mol-1
①第二步反应的热化学方程式是______ 。
②CO2与H2生成CH3OH反应的平衡常数表达式K=______ 。
③下图是其他条件一定时,反应温度对CO2平衡转化率影响的曲线,请结合化学用语说明温度低于350℃时,CO2的平衡转化率随温度变化的原因是______ 。

(3)O2辅助的Al—CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2。电池反应产物Al2(C2O4)3是重要的化工原料。电池原理如下:
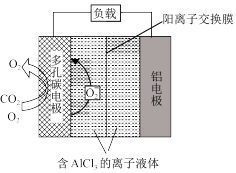
①O2作为正极反应的催化剂,可能的催化过程如下,将i补充完整,并写出ii的离子方程式。
i.O2+_____ ===_____ ;
ii._______ 。
②结合电极反应式简述Al2(C2O4)3的生成______ 。
(1)下列物质中可以作为CO2捕获剂的是
A.NH4Cl B.Na2CO3 C.HOCH2CH2OH D.HOCH2CH2NH2 E.(NH4)2CO3
(2)在Cu/ZnO催化剂条件下,CO2与H2可生成CH3OH,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
CH3OH(g)+H2O(g) ΔH1=-53.7kJ.mol-1。科研人员提出了该催化反应历程的示意图如下,其中CO是重要的中间产物。
已知:第一步反应I:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ.mol-1
CO(g)+H2O(g) ΔH2=+41kJ.mol-1①第二步反应的热化学方程式是
②CO2与H2生成CH3OH反应的平衡常数表达式K=
③下图是其他条件一定时,反应温度对CO2平衡转化率影响的曲线,请结合化学用语说明温度低于350℃时,CO2的平衡转化率随温度变化的原因是

(3)O2辅助的Al—CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2。电池反应产物Al2(C2O4)3是重要的化工原料。电池原理如下:

①O2作为正极反应的催化剂,可能的催化过程如下,将i补充完整,并写出ii的离子方程式。
i.O2+
ii.
②结合电极反应式简述Al2(C2O4)3的生成
更新时间:2020-09-16 21:25:46
|
相似题推荐
【推荐1】2020年9月,习近平主席在第75届联合国大会提出我国要实现2030年前碳达峰、2060年前碳中和的目标。因此CO2的捕集、利用与封存成为科学家研究的重要课题。
Ⅰ.工业上可以利用CO2和H2合成CH3OH,CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
(1)达到平衡时,反应a、b对比: 的体积分数
的体积分数
_______ 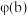 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)下列能说明反应a达到平衡状态的是_______(填标号)。
Ⅱ. 和
和 合成甲烷也是
合成甲烷也是 资源化利用的重要方法。对于反应
资源化利用的重要方法。对于反应
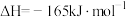 ,催化剂的选择是
,催化剂的选择是 甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得
甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得 转化率和生成
转化率和生成 选择性随温度变化的影响如下图所示。
选择性随温度变化的影响如下图所示。

(3)高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是_______ 。
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是_______ 。
Ⅲ.研究表明 与
与 在催化剂存在下可发生反应制得合成气:
在催化剂存在下可发生反应制得合成气: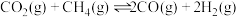 。
。
(5)此反应的活化能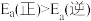 ,利于反应自发进行的条件是
,利于反应自发进行的条件是_______ (填“高温”或“低温”)。
(6)一定温度下,向一恒容密闭容器中充入 和
和 发生上述反应、初始时
发生上述反应、初始时 和
和 的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅳ.以铅蓄电池为电源可将 转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。

(7)阴极上的电极反应式为_______ ;每生成0.5mol乙烯,理论上需消耗铅蓄电池中_______ mol硫酸。
Ⅰ.工业上可以利用CO2和H2合成CH3OH,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表: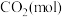 |  |  | 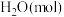 | |
| 反应a(恒温恒容) | 1 | 3 | 0 | 0 |
| 反应b(绝热恒容) | 0 | 0 | 1 | 1 |
(1)达到平衡时,反应a、b对比:
 的体积分数
的体积分数
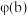 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)下列能说明反应a达到平衡状态的是_______(填标号)。
A. |
| B.混合气体的平均摩尔质量不再改变 |
C.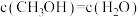 |
| D.容器内压强不再改变 |
Ⅱ.
 和
和 合成甲烷也是
合成甲烷也是 资源化利用的重要方法。对于反应
资源化利用的重要方法。对于反应
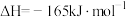 ,催化剂的选择是
,催化剂的选择是 甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得
甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得 转化率和生成
转化率和生成 选择性随温度变化的影响如下图所示。
选择性随温度变化的影响如下图所示。
(3)高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是
Ⅲ.研究表明
 与
与 在催化剂存在下可发生反应制得合成气:
在催化剂存在下可发生反应制得合成气: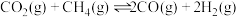 。
。(5)此反应的活化能
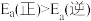 ,利于反应自发进行的条件是
,利于反应自发进行的条件是(6)一定温度下,向一恒容密闭容器中充入
 和
和 发生上述反应、初始时
发生上述反应、初始时 和
和 的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。Ⅳ.以铅蓄电池为电源可将
 转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
(7)阴极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】超细二硫化钼 粉末广泛应用于摩擦润滑、储氢、电极催化等领域,工业生产
粉末广泛应用于摩擦润滑、储氢、电极催化等领域,工业生产 粉末的反应如下:
粉末的反应如下: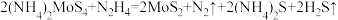 据此回答下列问题:
据此回答下列问题:
(1)肼 的电子式为
的电子式为_______ 。
(2)可用 溶液检验硫化氢的生成,写出该检验的化学反应方程式:
溶液检验硫化氢的生成,写出该检验的化学反应方程式:_______ 。
(3)硫化铵是一种重要的硝酸纤维脱硝剂,已知相关物质的解离常数如下:
 时,
时, 的
的 溶液呈
溶液呈______ 性(填“酸性”、“碱性”或“中性”);解释其原因:________________________ 。
(4)此反应产生的有污染的尾气通常采用电解法去除,装置如图:
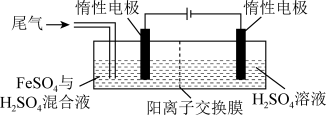
已知阳极半反应为 ,吸收一段时间以后阳极池产生
,吸收一段时间以后阳极池产生 淡黄色沉淀,写出阳极吸收尾气的离子反应方程式
淡黄色沉淀,写出阳极吸收尾气的离子反应方程式___________ ;此时阳极溶液中未检测到 ,则理论上阴极产生的气体标准状况下的体积为
,则理论上阴极产生的气体标准状况下的体积为______________ 。
 粉末广泛应用于摩擦润滑、储氢、电极催化等领域,工业生产
粉末广泛应用于摩擦润滑、储氢、电极催化等领域,工业生产 粉末的反应如下:
粉末的反应如下: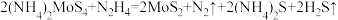 据此回答下列问题:
据此回答下列问题:(1)肼
 的电子式为
的电子式为(2)可用
 溶液检验硫化氢的生成,写出该检验的化学反应方程式:
溶液检验硫化氢的生成,写出该检验的化学反应方程式:(3)硫化铵是一种重要的硝酸纤维脱硝剂,已知相关物质的解离常数如下:
| 物质 | 25 | |
NH3 H2O H2O | Kb=1.74 10-5 10-5 | |
| H2S | Ka1=1.3 10-7 10-7 | Ka2=7.1 10-15 10-15 |
 时,
时, 的
的 溶液呈
溶液呈(4)此反应产生的有污染的尾气通常采用电解法去除,装置如图:

已知阳极半反应为
 ,吸收一段时间以后阳极池产生
,吸收一段时间以后阳极池产生 淡黄色沉淀,写出阳极吸收尾气的离子反应方程式
淡黄色沉淀,写出阳极吸收尾气的离子反应方程式 ,则理论上阴极产生的气体标准状况下的体积为
,则理论上阴极产生的气体标准状况下的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】废旧铅蓄电池会导致铅污染,国内外对废蓄电池的湿法处理进行了广泛研究,RSR工艺回收铅是其成果之一,具体化工流程如下:

已知:I.铅膏主要成分是 、
、 ;
;
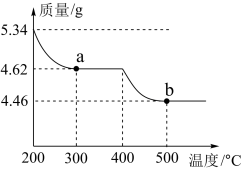
Ⅱ. 是强酸;
是强酸;
Ⅲ.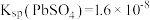 、
、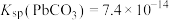 。
。
回答下列问题:
(1)写出副产品M的化学式___________ ;气体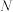 的电子式
的电子式___________ 。
(2)写出步骤①反应的化学方程式___________ 。
(3)步骤②中存在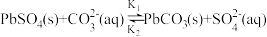 平衡,比较
平衡,比较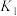
___________  (填“<”,“=”,“>”);检验
(填“<”,“=”,“>”);检验 固体是否洗涤干净的操作是
固体是否洗涤干净的操作是___________ 。
(4)步骤④加入 时边加边搅拌的目的是
时边加边搅拌的目的是___________ 。
(5)步骤⑤电解 溶液时,电路中转移0.5mol电子时阴极增重
溶液时,电路中转移0.5mol电子时阴极增重___________ g,阳极产生气体___________ L(标况)。
(6)已知焙烧 可制得铅的氧化物,为了研究其产物成分取
可制得铅的氧化物,为了研究其产物成分取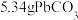 进行焙烧,其热重曲线如图所示,请写出
进行焙烧,其热重曲线如图所示,请写出 时所得铅的氧化物的化学式
时所得铅的氧化物的化学式___________ 。

已知:I.铅膏主要成分是
 、
、 ;
;Ⅱ.
 是强酸;
是强酸;Ⅲ.
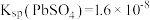 、
、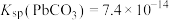 。
。回答下列问题:
(1)写出副产品M的化学式
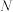 的电子式
的电子式(2)写出步骤①反应的化学方程式
(3)步骤②中存在
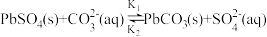 平衡,比较
平衡,比较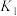
 (填“<”,“=”,“>”);检验
(填“<”,“=”,“>”);检验 固体是否洗涤干净的操作是
固体是否洗涤干净的操作是(4)步骤④加入
 时边加边搅拌的目的是
时边加边搅拌的目的是(5)步骤⑤电解
 溶液时,电路中转移0.5mol电子时阴极增重
溶液时,电路中转移0.5mol电子时阴极增重(6)已知焙烧
 可制得铅的氧化物,为了研究其产物成分取
可制得铅的氧化物,为了研究其产物成分取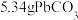 进行焙烧,其热重曲线如图所示,请写出
进行焙烧,其热重曲线如图所示,请写出 时所得铅的氧化物的化学式
时所得铅的氧化物的化学式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】研究人员开发新型Cu-Pd催化剂实现CO还原制备 :
:
 。
。
(1)已知:①

②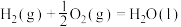

③

上述反应中,
_______ (用 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)一定温度下,在2L恒容密闭容器中充入4mol CO和 ,发生上述反应。测得
,发生上述反应。测得 的物质的量(mol)与时间(min)的关系如下表所示。
的物质的量(mol)与时间(min)的关系如下表所示。
下列说法错误的是_______(填标号)。
(3)在恒容密闭容器中充入一定量CO和 发生上述反应,测得单位时间内CO的转化率与催化剂Cat1、Cat2以及温度的关系如图l所示。
发生上述反应,测得单位时间内CO的转化率与催化剂Cat1、Cat2以及温度的关系如图l所示。
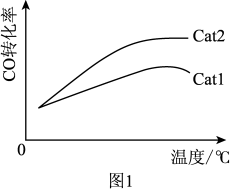
在相同条件下,催化效率较高的是_______ (填“Cat1”或“Cat2”)。
(4)在某温度下,向2L恒容密闭容器中充入2mol CO和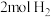 ,发生上述反应,测得混合气体总压强变化如图2所示。
,发生上述反应,测得混合气体总压强变化如图2所示。

0~5min内
_______ (填“大于”“小于”或“等于”)5~10min内 。该温度下,上述反应的平衡常数K=
。该温度下,上述反应的平衡常数K=_______ 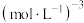 。
。
(5)下列有关“Cu-Pd催化剂”的说法正确的是_______(填标号)。
 :
:
 。
。(1)已知:①


②
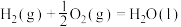

③


上述反应中,

 、
、 、
、 的代数式表示)。
的代数式表示)。(2)一定温度下,在2L恒容密闭容器中充入4mol CO和
 ,发生上述反应。测得
,发生上述反应。测得 的物质的量(mol)与时间(min)的关系如下表所示。
的物质的量(mol)与时间(min)的关系如下表所示。| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
 | 0.00 | 0.80 | 1.00 | 1.20 | 1.30 | 1.30 |
| A.15~20min时混合气体的密度不随时间变化 |
| B.CO消耗速率等于乙酸消耗速率的3倍时达到平衡状态 |
C.0~10min内 |
| D.上述条件下CO的平衡转化率为65% |
 发生上述反应,测得单位时间内CO的转化率与催化剂Cat1、Cat2以及温度的关系如图l所示。
发生上述反应,测得单位时间内CO的转化率与催化剂Cat1、Cat2以及温度的关系如图l所示。
在相同条件下,催化效率较高的是
(4)在某温度下,向2L恒容密闭容器中充入2mol CO和
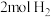 ,发生上述反应,测得混合气体总压强变化如图2所示。
,发生上述反应,测得混合气体总压强变化如图2所示。
0~5min内

 。该温度下,上述反应的平衡常数K=
。该温度下,上述反应的平衡常数K=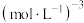 。
。(5)下列有关“Cu-Pd催化剂”的说法正确的是_______(填标号)。
A.降低CO和 制备乙酸反应的活化能 制备乙酸反应的活化能 | B.能提高CO和 的总能量 的总能量 |
C.能改变CO和 反应历程 反应历程 | D.能提高活化分子百分率 |
您最近一年使用:0次
【推荐2】(1)已知下列热化学方程式:
Ⅰ、H2(g)+ O2(g)===H2O(l) ΔH=-285.0 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.0 kJ·mol-1
Ⅱ、H2(g)+ O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
Ⅲ、C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
Ⅳ、C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
①上述反应中属于放热反应的是____________________________ 。(填编号)
②H2的燃烧热ΔH=___________ 。
③燃烧10 g H2生成液态水,放出的热量为________ 。
④CO的燃烧热ΔH=________ 。
(2)已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如图所示:
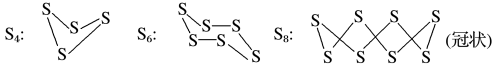
若已知硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,S(s)+O2(g)===SO2(g) ΔH=-a kJ·mol-1,则S8分子硫硫键的键能为________ 。
(3)下表是部分化学键的键能数据:
①已知白磷的燃烧热为2 982 kJ·mol-1,白磷(P4)、P4O6、P4O10结构如图所示,则上表中x=________ 。
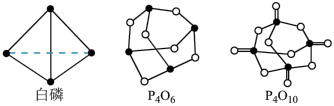
②0.5 mol白磷(P4)与O2完全反应生成固态P4O6,放出的热量为________ kJ。
Ⅰ、H2(g)+
 O2(g)===H2O(l) ΔH=-285.0 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.0 kJ·mol-1Ⅱ、H2(g)+
 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1Ⅲ、C(s)+
 O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1Ⅳ、C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
①上述反应中属于放热反应的是
②H2的燃烧热ΔH=
③燃烧10 g H2生成液态水,放出的热量为
④CO的燃烧热ΔH=
(2)已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如图所示:

若已知硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,S(s)+O2(g)===SO2(g) ΔH=-a kJ·mol-1,则S8分子硫硫键的键能为
(3)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O==O | P==O |
键能/kJ·mol-1 | 198 | 360 | 498 | x |
①已知白磷的燃烧热为2 982 kJ·mol-1,白磷(P4)、P4O6、P4O10结构如图所示,则上表中x=

②0.5 mol白磷(P4)与O2完全反应生成固态P4O6,放出的热量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】碳的化合物在生产、生活中有着重要的作用。
(1)已知:2CO(g)+O2(g)=2CO2(g) △H1=-566kJ•mol-1
H2O(g)+CO(g)=H2(g)+CO2(g) △H2=-41kJ•mol-1
CO(g)+2H2(g)=CH3OH(g) △H3=-107kJ•mol-1
则2CO2(g)+4H2O(g)=2CH3OH(g)+3O2(g) △H=_______ kJ•mol-1。
(2)T℃时,向容积为2L的恒容密闭容器中通入4.0molCO2和6.8molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=50kJ•mol-1,5分钟时反应达到平衡,CO2的转化率为50%,回答下列问题:
CH3OH(g)+H2O(g) △H=50kJ•mol-1,5分钟时反应达到平衡,CO2的转化率为50%,回答下列问题:
①在0~5min内容器中v(H2)=_______ 。
②反应过程中,下列各项指标能表明A容器中反应的v正<v逆的是_______ (填标号)。
A.体系内的压强增大 B.气体的平均相对分子质量减小
C.H2O(g)的物质的量增加 D.v正(CO2)=v逆(H2)
(3)T℃时,通入1.0molCO和3.0molH2于恒压容器(带可移动活塞)中,起始容积为2L,发生反应:CO(g)+2H2(g) CH3OH(g)。5分钟时反应达到平衡,CO的转化率为50%,回答下列问题:
CH3OH(g)。5分钟时反应达到平衡,CO的转化率为50%,回答下列问题:
①该温度下上述反应的平衡常数K=________ ;平衡时H2的转化率是_______ 。
②若达平衡后,再充入1.0nolCO、4.0molH2、1.0molCH3OH,平衡_______ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(4)CH3OH和O2组合形成的燃料电池的结构如图所示,质子(H+)交换膜左右两侧的溶液均为1L2mol/L的H2SO4溶液。电极c是_______ (填“正”或“负”)极,写出物质a在电极c上发生的反应式为_______ 。

(1)已知:2CO(g)+O2(g)=2CO2(g) △H1=-566kJ•mol-1
H2O(g)+CO(g)=H2(g)+CO2(g) △H2=-41kJ•mol-1
CO(g)+2H2(g)=CH3OH(g) △H3=-107kJ•mol-1
则2CO2(g)+4H2O(g)=2CH3OH(g)+3O2(g) △H=
(2)T℃时,向容积为2L的恒容密闭容器中通入4.0molCO2和6.8molH2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=50kJ•mol-1,5分钟时反应达到平衡,CO2的转化率为50%,回答下列问题:
CH3OH(g)+H2O(g) △H=50kJ•mol-1,5分钟时反应达到平衡,CO2的转化率为50%,回答下列问题:①在0~5min内容器中v(H2)=
②反应过程中,下列各项指标能表明A容器中反应的v正<v逆的是
A.体系内的压强增大 B.气体的平均相对分子质量减小
C.H2O(g)的物质的量增加 D.v正(CO2)=v逆(H2)
(3)T℃时,通入1.0molCO和3.0molH2于恒压容器(带可移动活塞)中,起始容积为2L,发生反应:CO(g)+2H2(g)
 CH3OH(g)。5分钟时反应达到平衡,CO的转化率为50%,回答下列问题:
CH3OH(g)。5分钟时反应达到平衡,CO的转化率为50%,回答下列问题:①该温度下上述反应的平衡常数K=
②若达平衡后,再充入1.0nolCO、4.0molH2、1.0molCH3OH,平衡
(4)CH3OH和O2组合形成的燃料电池的结构如图所示,质子(H+)交换膜左右两侧的溶液均为1L2mol/L的H2SO4溶液。电极c是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铜转炉烟灰主要含有Zn[还有少量的Fe(+2价)、Pb、Cu、As等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:
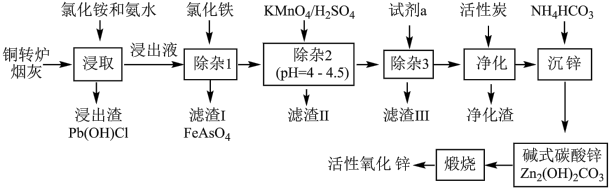
已知:活性炭净化主要是除去有机杂质。
(1)写出氯化铵的电子式___ ,“净化”过程属于___ (填“物理”、“化学”)变化。
(2)在反应温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为___ mol·L-1。若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为___ 。

(3)滴加KMnO4溶液有MnO2生成,目的是除___ 元素,除杂3是置换除杂过程,则试剂a是___ ,“滤渣Ⅲ”的主要成分为___ (填化学式)。
(4)写出“沉锌”时发生反应的离子方程式___ ,此过程中可以循环利用的副产品是___ 。
(5)取mg活性氧化锌样品配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为___ (用代数式表示)。

已知:活性炭净化主要是除去有机杂质。
(1)写出氯化铵的电子式
(2)在反应温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为

(3)滴加KMnO4溶液有MnO2生成,目的是除
(4)写出“沉锌”时发生反应的离子方程式
(5)取mg活性氧化锌样品配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】碳达峰、碳中和是现在需要继续完成的环保任务, 的综合利用成为热点研究对象,
的综合利用成为热点研究对象, 作为碳源加氢是再生能源的有效方法,
作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,
加氢可以合成甲醇, 提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过
提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
反应I: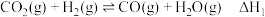
反应Ⅱ:
(1)①相关键能如下表,则
_______ ,该反应的活化能 (正)
(正)_______  (逆)(填“大于”“小于”或“等于”)。
(逆)(填“大于”“小于”或“等于”)。
②已知 的正反应速率
的正反应速率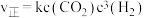 (k为正反应的速率常数),某温度时测得数据如下:
(k为正反应的速率常数),某温度时测得数据如下:
则此温度下,表中
______ 。
(2)据文献报道, 基纳米材料作为高性能催化剂可将
基纳米材料作为高性能催化剂可将 电还原为高能量密度的
电还原为高能量密度的 ,不同催化剂对生成
,不同催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是
的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是_______ 。 的转化率随温度和压强的变化如图,判断
的转化率随温度和压强的变化如图,判断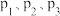 的大小关系:
的大小关系:__________ ;解释压强一定时, 的平衡转化率呈现如图变化的原因:
的平衡转化率呈现如图变化的原因:_________________ 。 ,向容积为
,向容积为 的恒容密闭容器中充入
的恒容密闭容器中充入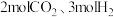 发生反应I、Ⅱ,平衡时
发生反应I、Ⅱ,平衡时 的转化率是
的转化率是 ,体系内剩余
,体系内剩余 ,则反应Ⅱ的平衡常数
,则反应Ⅱ的平衡常数
_______  ,体系内甲醇的平衡分压
,体系内甲醇的平衡分压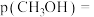
_____  (用含
(用含 的式子表示)。
的式子表示)。
 的综合利用成为热点研究对象,
的综合利用成为热点研究对象, 作为碳源加氢是再生能源的有效方法,
作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,
加氢可以合成甲醇,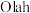 提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过
提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:反应I:
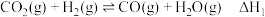
反应Ⅱ:

(1)①相关键能如下表,则

 (正)
(正) (逆)(填“大于”“小于”或“等于”)。
(逆)(填“大于”“小于”或“等于”)。化学键 |
|
|
|
|
键能 | 436 | 1071 | 464 | 803 |
 的正反应速率
的正反应速率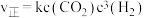 (k为正反应的速率常数),某温度时测得数据如下:
(k为正反应的速率常数),某温度时测得数据如下:
|
|
| |
1 | 0.02 | 0.01 |
|
2 | 0.02 | 0.02 | a |

(2)据文献报道,
 基纳米材料作为高性能催化剂可将
基纳米材料作为高性能催化剂可将 电还原为高能量密度的
电还原为高能量密度的 ,不同催化剂对生成
,不同催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是
的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是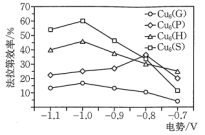
 的转化率随温度和压强的变化如图,判断
的转化率随温度和压强的变化如图,判断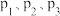 的大小关系:
的大小关系: 的平衡转化率呈现如图变化的原因:
的平衡转化率呈现如图变化的原因:
 ,向容积为
,向容积为 的恒容密闭容器中充入
的恒容密闭容器中充入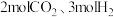 发生反应I、Ⅱ,平衡时
发生反应I、Ⅱ,平衡时 的转化率是
的转化率是 ,体系内剩余
,体系内剩余 ,则反应Ⅱ的平衡常数
,则反应Ⅱ的平衡常数
 ,体系内甲醇的平衡分压
,体系内甲醇的平衡分压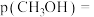
 (用含
(用含 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氮及化合物的性质与应用是科学研究的热点。
(1) 分子呈正四面体结构,如图所示。已知断裂1molN—N键吸收190kJ能量,断裂
分子呈正四面体结构,如图所示。已知断裂1molN—N键吸收190kJ能量,断裂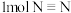 键吸收940kJ能量,则
键吸收940kJ能量,则 气体转化为
气体转化为 时要
时要_______ (填“吸收”或“放出”)能量_______ kJ。

(2)利用 和
和 生成
生成 的反应设计成原电池,装置如图所示。电极B是
的反应设计成原电池,装置如图所示。电极B是_______ 极(填“正”或“负”), 通过离子交换膜向
通过离子交换膜向_______ (填“A”或“B”)极移动,写出电极A的电极反应式:_______ 。

(3)水体中 的污染可用纳米铁粉消除,反应的离子方程式为
的污染可用纳米铁粉消除,反应的离子方程式为 。研究发现,若pH偏低将会导致
。研究发现,若pH偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是_______ 。相同条件下,纳米铁粉去除不同水样中 的速率有较大差异如图,产生该差异的可能原因是
的速率有较大差异如图,产生该差异的可能原因是_______ 。

I.含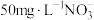 的水样
的水样
II.含 的水样
的水样
(1)
 分子呈正四面体结构,如图所示。已知断裂1molN—N键吸收190kJ能量,断裂
分子呈正四面体结构,如图所示。已知断裂1molN—N键吸收190kJ能量,断裂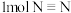 键吸收940kJ能量,则
键吸收940kJ能量,则 气体转化为
气体转化为 时要
时要
(2)利用
 和
和 生成
生成 的反应设计成原电池,装置如图所示。电极B是
的反应设计成原电池,装置如图所示。电极B是 通过离子交换膜向
通过离子交换膜向
(3)水体中
 的污染可用纳米铁粉消除,反应的离子方程式为
的污染可用纳米铁粉消除,反应的离子方程式为 。研究发现,若pH偏低将会导致
。研究发现,若pH偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是 的速率有较大差异如图,产生该差异的可能原因是
的速率有较大差异如图,产生该差异的可能原因是
I.含
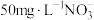 的水样
的水样II.含
 的水样
的水样
您最近一年使用:0次