显示答案
|
共 4 道试题
解答题-工业流程题
|
适中(0.65)
解题方法
(衡水金卷 2018-2019年度高三第三次联合质量测评理综 )氟化锂(LiF)难溶于水,可用于核工业、光学玻璃制造等。以透锂长石(含Li2O、Al2O3、SiO2)为原料制备氟化锂的工艺流程如下:
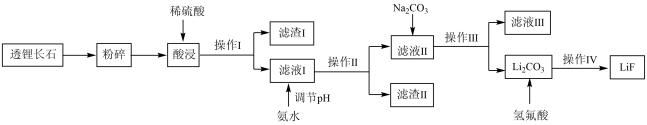
回答下列问题:
(1 )滤液I中含有的金属离子有_______ ,滤渣I的一种用途是____________ 。
(2)滤渣Ⅱ是目前应用最广泛的无机阻燃剂,写出生成滤渣Ⅱ的离子方程式:________ 。常温下,若向滤液I中滴加氨水调节pH=5时,溶液中c(Al3+)=_____ mol·L-1,则溶液中A13+______ (填“是”或“否”)沉淀完全(已知Ksp[Al(OH)3]=2.0×10-33,且溶液中的离子浓度小于1.0×10-5mol·L-1时沉淀完全)。
(3)操作Ⅳ包括_________ 、_________ 和干燥。
(4)写出Li2CO3与氢氟酸反应的化学方程式:________ ,该反应不能在玻璃容器中进行的原因是_________ (用化学方程式表示)。

回答下列问题:
(
(2)滤渣Ⅱ是目前应用最广泛的无机阻燃剂,写出生成滤渣Ⅱ的离子方程式:
(3)操作Ⅳ包括
(4)写出Li2CO3与氢氟酸反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
我国科学家团队于2017年 1月成功合成世界首个全 氮阴离子盐,使氮原子簇化合物的研究又有了新的突破。请根据材料回答以下问题:
(1 )基态N原子的价电子占据的能量最高的能级是___ ,价电子在该能级上的排布遵循的原则是__ 。
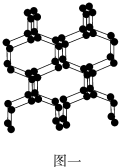
(2)除了已知的氮气,科学家还先后研究出了N4、N60、N70、高聚氮等物质。而高聚氮结构具有空间网状结构,如图一所示,则N70的沸点___  填“
填“ ”、“
”、“ ”或“
”或“ ”
” 高聚氮的沸点,原因是
高聚氮的沸点,原因是___ ;
(3)叠氮化物是研究较早的含全 氮阴离子的化合物,如:氢叠氮酸(HN3)、叠氮化钠(NaN3)等。与全 氮阴离子互为等电子体的一种非极性分子的结构式为___ 。叠氮化物能形成多种配合物,在[CO(N3)(NH3)5]SO4,其中钴原子的配体是___ ,SO42-的立体构型为___ 。
(4)HN3是一种全 氮阴离子酸,可由肼(N2H4)被HNO2氧化制得。下列说法正确的是____ 。
A.酸性:HNO2>HNO3
B.N2H4分子中N原子均采取sp3杂化
C.NaN3的晶格能大于KN3的晶格能
D.纯叠氮酸HN3在常温下是一种液体,是因为分子中存在一种特殊的化学键-氢键
(5)N8是一种由全 氮阳离子和全 氮阴离子构成的特殊物质,已知阳离子由5个氮原子排列成V形,每个氮原子均达到8电子稳定结构,则阳离子的电子式为___ 。
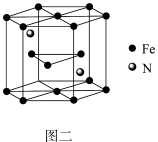
(6)一种氮铁化合物的结构如图二所示,若图中六棱柱的体积为Vcm3,用NA表示阿伏加 德罗常数的值,则该晶体的密度为__ 。
(
(2)除了已知的氮气,科学家还先后研究出了N4、N60、N70、高聚氮等物质。而高聚氮结构具有空间网状结构,如图一所示,则N70的沸点
 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 高聚氮的沸点,原因是
高聚氮的沸点,原因是
(3)叠氮化物是研究较早的含
(4)HN3是一种
A.酸性:HNO2>HNO3
B.N2H4分子中N原子均采取sp3杂化
C.NaN3的晶格能大于KN3的晶格能
D.纯叠氮酸HN3在常温下是一种液体,是因为分子中存在一种特殊的化学键-氢键
(5)N8是一种由
(6)一种氮铁化合物的结构如图二所示,若图中六棱柱的体积为Vcm3,用NA表示阿伏加 德罗常数的值,则该晶体的密度为

您最近一年使用:0次
南京理工大学化工学院胡炳成教授团队于2017年 1月成功合成世界首个全 氮阴离子盐,使氮原子簇化合物的研究又有了新的突破。请回答以下问题:
(1 )基态N原子的电子排布图为___________ ,该原子中2p轨道上电子的排布遵循的原则是___________ 。
(2)第二周期元素原子的第一电离能介于B、N之间的有___________ 。
(3)科学家目前合成了N4分子,该分子中N—N—N的键角为___________ ;N4分解后能产生N2并释放出大量能量,推测其用途:___________ (写出一种即可)。
(4)N8是一种由全 氮阳离子和全 氮阴离子构成的特殊物质,已知阳离子由5个氮原子排列成V形,每个氮原子均达到8电子稳定结构,则阳离子的电子式为___________ 。
(
(2)第二周期元素原子的第一电离能介于B、N之间的有
(3)科学家目前合成了N4分子,该分子中N—N—N的键角为
(4)N8是一种由
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
(四川省高中2019届毕业班第二次诊断性考试理综 )钒是一种重要的金属材料,其用途之一是制备催化剂,如接触法生产硫酸中使用的催化剂(主要成分V2O5、V2O4)。利用废催化剂回收制备V2O5的工艺流程如下:
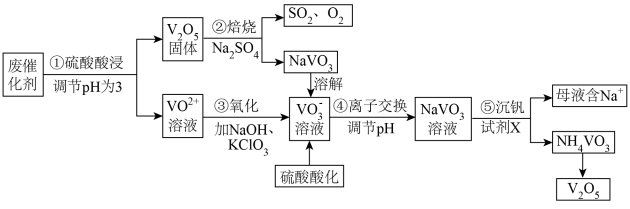
已知:20℃时,NH4VO3的Ksp=1.68×10-2
回答下列问题:
(1 )步骤①为提高浸取效率采取的方法有______ (任写两条)
(2)步骤②中反应的氧化剂是_______ 。
(3)步骤③中ClO3-被还原为Cl-,该反应的离子方程式为______ 。
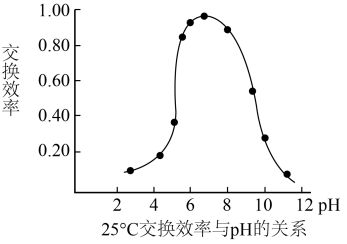
(4)步骤④中,离子交换效率与pH的关系如右图,为提高交换效率应控制的pH范围是_______ 。
(5)步骤⑤所发生反应的离子方程式为___ 。若母液中NH4+的浓度为1.0mol/L,则c(VO3-)=____ 。
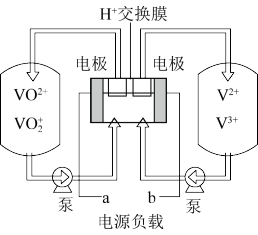
(6)全 钒电池是以溶解在一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO2+)为电极反应的活性物质。一种全 钒电池原理如下图,放电时H+从右向左移动。写出充电时阳极的电极反应式_____ ,当转移0.1mol电子时,转移H+的物质的量为____ mol。

已知:20℃时,NH4VO3的Ksp=1.68×10-2
回答下列问题:
(
(2)步骤②中反应的氧化剂是
(3)步骤③中ClO3-被还原为Cl-,该反应的离子方程式为
(4)步骤④中,离子交换效率与pH的关系如右图,为提高交换效率应控制的pH范围是

(5)步骤⑤所发生反应的离子方程式为
(6)

您最近一年使用:0次



