名校
解题方法
1 . 下列实验的设计方案、现象和结论有错误的是
选项 | 实验目的 | 设计方案和实验现象 | 结论 |
A | 检验菠菜中是否含有铁元素 | 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后,再加入KSCN溶液,溶液变红 | 菠菜中含有铁元素 |
B | 检验尿液中是否含有葡萄糖 | 取尿液适量,向其中加入NaOH至溶液呈碱性,加入新制的 悬浊液,加热煮沸,产生砖红色沉淀 悬浊液,加热煮沸,产生砖红色沉淀 | 尿液中含有葡萄糖 |
C | 向 的水溶液中滴加硝酸银溶液 的水溶液中滴加硝酸银溶液 | 无明显现象 | 该配合物中 的配位数是6 的配位数是6 |
D | 比较配离子 、 、 的稳定性 的稳定性 | 将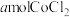 固体溶于水,加入适量浓盐酸后,再加入 固体溶于水,加入适量浓盐酸后,再加入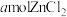 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 呈粉红色, 呈粉红色, 呈蓝色, 呈蓝色, 呈无色) 呈无色) | 稳定性: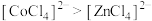 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)实验室制备氨气,下列方法中可以选用的是_______ 。
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因_______ 。
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式_______ 。
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式_______ ;
②求硝酸的浓度_______ mol·L-1;
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式_______ ,若往试管中通入氧气让液体充满试管,则通入氧气的物质的量_______ mol。
(1)实验室制备氨气,下列方法中可以选用的是
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式
②求硝酸的浓度
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式
您最近一年使用:0次
解题方法
3 . 已知:稀硝酸能与SO2发生氧化还原反应:3SO2+2HNO3+2H2O=3H2SO4+2NO。下列过程中最终的白色沉淀不一定是BaSO4的是
| A.Fe(NO3)2溶液→通入SO2+过量盐酸→加BaCl2溶液→白色沉淀 |
| B.Ba(NO3)2溶液→加过量盐酸→加Na2SO3溶液→白色沉淀 |
| C.无色溶液→加稀HNO3→加BaCl2溶液→白色沉淀 |
| D.无色溶液→加过量盐酸→无色溶液→加BaCl2溶液→白色溶液 |
您最近一年使用:0次
4 . 下列物质中,保存方法正确的是
| A.漂白粉敞口存放 | B.金属钠保存在煤油中 |
| C.钢铁在潮湿环境存放 | D.浓硝酸保存在无色试剂瓶中 |
您最近一年使用:0次
2024-03-29更新
|
73次组卷
|
2卷引用:2023年6月福建省普通高中学业水平合格性考试化学试题
名校
5 . 几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是
| 元素代号 | X | Y | Z | W |
原子半径/ | 160 | 143 | 70 | 66 |
| 主要化合价 |  |  |  、 、 、 、 |  |
A.X、Y元素的金属性: |
| B.Y的氧化物是碱性氧化物 |
| C.Y的最高价氧化物对应的水化物能溶于稀氨水 |
| D.一定条件下,Y单质可以与Z的最高价氧化物对应的水化物反应 |
您最近一年使用:0次
6 . 碱式硫酸铁[Fe(OH)SO4]难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:

(1) 的空间结构为
的空间结构为___________ ;锥形瓶中发生反应的化学方程式为___________ ;某同学认为用H2O2溶液代替稀硝酸更好,理由是___________ 。
(2)酸性高锰酸钾溶液可除去一氧化氮,反应的离子方程式为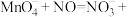
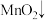 。该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为
。该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为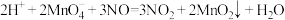 ,则第二步反应的离子方程式为
,则第二步反应的离子方程式为___________ 。
(3)某同学测定产物纯度的方法如下:称取2.5g产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用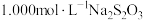 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 (涉及的反应方程式为
(涉及的反应方程式为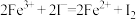 、
、 )。
)。
①盛装Na2S2O3标准溶液的滴定管应选用___________ (填“酸式”或“碱式”)滴定管。
②判断达到滴定终点的方法为___________ 。
③该产品的纯度为___________ %。滴定过程中,如果滴定速度过慢,可能导致所测结果___________ (填“偏高”“偏低”或“无影响”)。

(1)
 的空间结构为
的空间结构为(2)酸性高锰酸钾溶液可除去一氧化氮,反应的离子方程式为
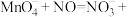
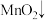 。该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为
。该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为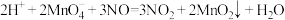 ,则第二步反应的离子方程式为
,则第二步反应的离子方程式为(3)某同学测定产物纯度的方法如下:称取2.5g产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用
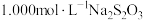 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 (涉及的反应方程式为
(涉及的反应方程式为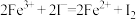 、
、 )。
)。①盛装Na2S2O3标准溶液的滴定管应选用
②判断达到滴定终点的方法为
③该产品的纯度为
您最近一年使用:0次
解题方法
7 . 下列各组中的离子,能在其水溶液中大量共存的是
A.Na+、Al3+、NO 、OH- 、OH- | B. |
C. | D.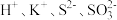 |
您最近一年使用:0次
名校
解题方法
8 . 某实验小组同学用KSCN探究久置FeSO4固体变质的情况。将0.3gFeSO4固体用10mL蒸馏水溶解,配成待测液,进行实验。
【初步实验】
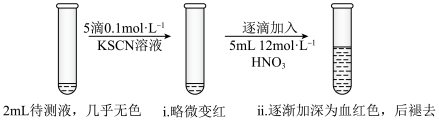
(1)用KSCN检验Fe3+的原理是___________ (用离子方程式表示)。
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被___________ (填化学式)氧化。结合平衡移动原理解释ⅱ中血红色褪去的可能原因___________ 。
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是___________ 。
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
(4)请补全步骤Ⅱ中的操作:___________ 。
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是___________ (填字母序号)。
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有___________ (至少2条)。
【初步实验】

(1)用KSCN检验Fe3+的原理是
(2)甲同学认为FeSO4固体几乎未变质,ⅱ中变血红色是由于Fe2+被
(3)乙同学不认同甲对现象的解释,他推测加入浓硝酸后ⅱ中变血红色还可能与其它因素有关,可能的影响因素是
为验证该猜测,乙同学继续进行了以下实验。【继续探究】
| 步骤 | 操作 | 现象 |
| Ⅰ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,再加入5mL浓KNO3溶液 | 溶液无明显变化 |
| Ⅱ | 取2mL待测液,加入5滴0.1mol·L-1KSCN溶液,___________ | 溶液变为红色 |
| Ⅲ | 向Ⅱ中所得溶液中逐滴加入浓硝酸,边加边振荡 | 溶液逐渐加深为血红色,继续滴加浓硝酸,溶液褪色,pH变化始终不明显 |
(4)请补全步骤Ⅱ中的操作:
(5)由Ⅰ~Ⅲ推测FeSO4固体变质的情况是
a.几乎未变质 b.部分变质 c.完全变质
【反思与迁移】
(6)从上述探究中获得启发,在用KSCN检验Fe3+及进行Fe2+还原性验证实验时,需要注意的事项有
您最近一年使用:0次
名校
解题方法
9 . 下列实验操作与预期实验目的或结论一致的是
选项 | 实验操作和现象 | 预期实验日的或结论 |
A | 向 溶液中滴加盐酸,溶液转为黄色 溶液中滴加盐酸,溶液转为黄色 | 说明盐酸具有氧化性 |
B | 向 溶液中通入 溶液中通入 气体,出现黑色沉淀 气体,出现黑色沉淀 | 说明 酸性强于稀硫酸 酸性强于稀硫酸 |
C | 向一定浓度的 溶液中通入适量的 溶液中通入适量的 气体,有白色沉淀产生 气体,有白色沉淀产生 | 说明非金属性 |
D | 将少量 和 和 的混合溶液滴入 的混合溶液滴入 溶液中,观察到有红褐色沉淀产生 溶液中,观察到有红褐色沉淀产生 | 说明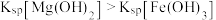 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 设NA为阿伏加德罗常数的值,下列说法错误的是
A.3.2g 完全溶于一定量的浓硝酸中,转移的电子数一定为0.1NA 完全溶于一定量的浓硝酸中,转移的电子数一定为0.1NA |
| B.100mL0.1mol/LCH3COONa溶液中阴离子数目大于0.01NA |
| C.标准状况下,22.4L甲醇中含有-OH的数目为NA个 |
D.密闭容器中1molNO与1mol 充分反应,产物的分子数小于1.5NA 充分反应,产物的分子数小于1.5NA |
您最近一年使用:0次



