2014-2015学年福建省四地六校高一上学期第三次月考化学试卷
福建
高一
阶段练习
2017-07-26
237次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学与STSE、化学反应原理
一、单选题 添加题型下试题
| A.在常温常压下,11.2 L N2含有的分子数为0.5NA |
| B.在常温常压下,2g H2含有的原子数为2NA |
| C.在标准状况下,18 g H2O的体积约为22.4 L |
| D.0.1mol/L NaCl溶液中所含的Na+数为0.1 NA |
【知识点】 化学计量
| A.钠保存在煤油中 | B.氯水保存棕色细口瓶中 |
| C.液氯可以保存在干燥的钢瓶中 | D.溴化银保存在无色试剂瓶中 |
| A.镁合金:航空、航天材料 | B.小苏打:焙制糕点的发酵粉 |
| C.明矾:消毒、杀菌作用 | D.过氧化钠:漂白剂和供氧剂 |
【知识点】 化学与材料的发展
| A.①②③④⑤ | B.②⑤①③④ | C.①③⑤②④ | D.②①③⑤④ |
【知识点】 海带中碘的提取及检验解读
| A.金属钠和硫酸铜溶液 | B.过氧化钠和氯化镁溶液 |
| C.氧化钠和氯化铵溶液并加热 | D.硫酸铵和氢氧化钡溶液并加热 |
【知识点】 离子反应的发生及书写
| A.Na和H2O | B.Na2O和H2O |
| C.Cl2和H2O | D.Na2O2和H2O |
【知识点】 氧化还原反应基本概念
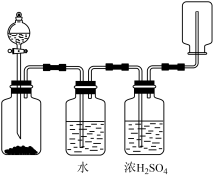
| A.锌和盐酸生成氢气 |
| B.二氧化锰和浓盐酸生成氯气 |
| C.碳酸钙和盐酸生成二氧化碳 |
| D.过氧化氢和MnO2生成氧气 |
【知识点】 氯气的实验室制法解读 常见气体的制备与收集解读
| A.二氧化硫溶于水能导电,故二氧化硫属于电解质 |
| B.硫酸钡难溶于水,故硫酸钡属于弱电解质 |
| C.硫酸是强电解质,故纯硫酸能导电 |
| D.氢离子浓度相同的盐酸和醋酸溶液导电能力相同 |
【知识点】 电解质、非电解质概念解读 强电解质和弱电解质的判断
A.氯气溶于水:Cl2 + H2O  H+ + Cl– + HClO H+ + Cl– + HClO |
| B.用小苏打治疗胃酸过多:HCO3-+H+===CO2↑+H2O(胃酸的主要成分是稀盐酸) |
| C.金属铁与稀H2SO4反应:Fe + 2H+== Fe3+ + H2↑ |
| D.铝与过量氢氧化钠溶液反应:2Al+2OH-+2H2O===2AlO2-+3H2↑ |
【知识点】 离子反应的发生及书写
| A.Na+、Ba2+、Cl-、SO42- | B.H+、CH3COO-、Cl-、K+ |
| C.H+、Na+、NO3-、Cl- | D.NH4+、Cl-、Na+、OH- |
【知识点】 离子共存
| A.在氮气的容器内冷却 | B.在空气中冷却 |
| C.在氦气的环境里冷却 | D.在二氧化碳气体里冷却 |
| A.二种 | B.三种 | C.四种 | D.五种 |
| A.稀硫酸、氯化钡溶液 | B.硫酸铝溶液、氨水 |
| C.氯化钠溶液、硝酸银溶液 | D.氯化铝溶液、氢氧化钠溶液 |
【知识点】 离子反应的发生及书写 铝盐与强碱溶液反应解读
二、填空题 添加题型下试题
(1)铝在反应中容易失去电子,发生
(2)生产中曾用铝热反应焊接钢轨,写出铝与氧化铁发生反应的化学方程式为并标出电子转移的方向和数目:
(3)胃舒平是治疗胃酸过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示):
(4)在同温同压下,等质量的铝分别投入足量的稀盐酸和NaOH溶液中,产生气体的体积之比为
(5)铝合金在空气中很稳定,可以制造多种建筑型材。向一只小烧杯里加入少量CuSO4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝合金取出,无明显现象。将另一小块铝合金先放入NaOH溶液里,片刻后取出,用蒸馏水冲洗后浸入CuSO4溶液里,1~2分钟后将铝片取出,发现铝片表面有亮红色的固体附着,NaOH溶液的作用是
【知识点】 氧化还原反应基本概念 铝热反应解读 氢氧化铝与强酸反应解读

试回答下列问题:
(1)我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为
(2)为除去粗盐中的Ca2+、Mg2+、SO
 及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是
及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是(3)写出电解饱和食盐水的化学方程式
(4)以海边贝壳为原料可以制取石灰乳,贝壳的主要化学成分为
(5)目前,世界上生产的镁有60%自海水,由“母液”制“镁”的过程中,发生了
(6)电解氯化镁所得的氯气,除用于生产盐酸外,还可以用于制取漂白粉,漂白粉的有效成分是
(7)溴主要以Br-形式存在于海水中,提取食盐后剩下的母液(也叫卤水)中,Br-的浓度较大,工业上 制备的Br2的操作步骤为:一定条件下,将Cl2通入卤水中,生成Br2,利用热空气将Br2吹出,Br2可用热空气吹出,其原因是
【知识点】 氧化还原反应有关计算 卤素及其化合物 资源合理开发利用
三、解答题 添加题型下试题

(1)请写出CO2与过量的NaOH发生反应的离子方程式:
(2)选择任意一种实验装置进行实验,简述预计出现的实验现象。你选择的实验装置是
(3)上述实验中,如果二氧化碳过量,还可能生成
Ⅱ、为探究碳酸钠和碳酸氢钠固体的热稳定性,某同学设计了“套管实验”,装置如图,大试管A与小试管a相连通,大试管B小试管b相连通。

(1)小试管B中应装的药品是
(2)小试管a中出现的现象预计是
Ⅲ、工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀经
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液为饱和碳酸氢钠溶液,因为二氧化碳难溶于饱和碳酸氢钠溶液,但选用该溶液后实验结果仍然不够准确,会使Na2CO3的质量分数偏大,其原因可能是

四、计算题 添加题型下试题
Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O。试计算:
CuSO4+SO2↑+2H2O。试计算:(1)反应中消耗的铜的质量;
(2)将生成的硫酸铜配制成500mL溶液,则该溶液中CuSO4的物质的量浓度是多少?
试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.64 | 化学计量 | |
| 2 | 0.94 | 氯水的性质 钠单质的保存与用途 仪器使用与实验安全 | |
| 3 | 0.64 | 化学与材料的发展 | |
| 4 | 0.64 | 卤素及其化合物 | |
| 5 | 0.65 | 海带中碘的提取及检验 | |
| 6 | 0.64 | 离子反应的发生及书写 | |
| 7 | 0.64 | 氧化还原反应基本概念 | |
| 8 | 0.65 | 氯气的实验室制法 常见气体的制备与收集 | |
| 9 | 0.85 | 硝酸的强氧化性 铝与酸溶液反应 | |
| 10 | 0.85 | 电解质、非电解质概念 强电解质和弱电解质的判断 | |
| 11 | 0.65 | 铝与强碱溶液反应 | |
| 12 | 0.64 | 离子反应的发生及书写 | |
| 13 | 0.85 | 离子共存 | |
| 14 | 0.65 | 镁 镁的结构与化学性质 | |
| 15 | 0.65 | 铵盐与碱反应 含镁化合物 既能与酸反应又能与碱反应的无机物质 铝三角转化 | |
| 16 | 0.85 | 离子反应的发生及书写 铝盐与强碱溶液反应 | |
| 二、填空题 | |||
| 17 | 0.65 | 氧化还原反应基本概念 铝热反应 氢氧化铝与强酸反应 | |
| 18 | 0.64 | 氧化还原反应有关计算 卤素及其化合物 资源合理开发利用 | |
| 三、解答题 | |||
| 19 | 0.4 | 化学实验基础 钠及其化合物 | 实验探究题 |
| 四、计算题 | |||
| 20 | 0.64 | 化学计量 氧族元素及其化合物 | |



