上海音乐学院附属安师实验中学2021-2022学年高一上学期期中考试化学试题
上海
高一
期中
2022-08-29
152次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| A.混合物 | B.单质 | C.化合物 | D.酸 |
| A.微粒的大小 | B.微粒间的距离 |
| C.微粒的种类 | D.微粒的数目 |
【知识点】 气体摩尔体积 决定物质体积大小的微观因素解读
| A.在豆浆里加入盐卤做豆腐 |
| B.河流入海口易形成沙洲 |
| C.一束平行的光线照射蛋白质溶液时,从侧面可以看到光亮的通路 |
| D.硝酸银溶液中 滴加氯化钠溶液有白色沉淀生成 |
| A.硫酸的摩尔质量是96 g |
| B.物质的量是指物质的质量 |
| C.4 g氢氧化钠加1升水,氢氧化钠溶液的浓度是0.1 mol/L |
| D.摩尔是物质的量的单位 |
| A.3.01×1023个 | B.6.02×1023 个 | C.0.5个 | D.1个 |
【知识点】 阿伏加德罗常数的求算解读
| A.28g N2 | B.1mol N2 | C.48g O2 | D.2mol O2 |
【知识点】 22.4L/mol适用条件解读 阿伏加德罗定律及其推论解读
| A.标准状况下,气体摩尔体积约为22.4 L/mol |
| B.非标准状况下,任何气体1 mol不可能为22.4 L |
| C.标准状况下,1 mol任何气体都约含有6.02×1023个分子 |
| D.标准状况下,1 mol H2和O2的混合气体的体积约为22.4 L |
| A.物质的量不相等 | B.所含分子数相等 |
| C.密度相等 | D.所含氧原子个数相等 |
【知识点】 阿伏加德罗定律及其推论解读 物质的量有关计算
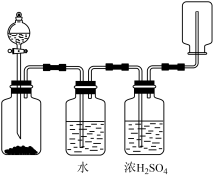
| A.锌和盐酸生成氢气 |
| B.二氧化锰和浓盐酸生成氯气 |
| C.碳酸钙和盐酸生成二氧化碳 |
| D.过氧化氢和MnO2生成氧气 |
【知识点】 氯气的实验室制法解读 常见气体的制备与收集解读
| A.溶液分层,上层紫红色下层无色 |
| B.溶液不分层,溶液紫红色 |
| C.溶液分层,上层无色下层紫红色 |
| D.溶液不分层,溶液黄色 |
【知识点】 化学实验基础操作解读 物质分离、提纯的常见物理方法 萃取和分液解读
| A.从碘水中提取碘时,不可以用酒精做萃取剂 |
| B.萃取时,萃取剂的密度必须比水大 |
| C.可以用过滤的方法除去糖水中的糖 |
| D.利用萃取的方法可以分离硝酸钾晶体中的氯化钠 |
| A.用洁净的铂丝蘸取某溶液,在火焰上灼烧,焰色为黄色,确定不含K+ |
| B.焰色反应只能检验金属单质 |
| C.焰色反应可以检验任何元素 |
| D.焰色反应是物理变化 |
| A.BaCl2溶液 | B.盐酸 | C.CaCl2溶液 | D.AgNO3溶液 |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 物质的检验
| A.硝酸银溶液,有白色沉淀 |
| B.硝酸银溶液和稀硝酸,有白色沉淀 |
| C.硝酸银溶液和稀硫酸,有白色沉淀 |
| D.硝酸银溶液和稀盐酸,有白色沉淀 |
| A.1000 mL,5.850 g | B.950 mL,5.850 g |
| C.任意规格,5.850 g | D.500 mL,5.850 g |
| A.0.4 mol/L | B.0.25 mol/L | C.0.2 mol/L | D.0.1 mol/L |
【知识点】 物质的量浓度计算-溶液稀释的有关计算解读
| A.10 mol/L | B.13 mol/L | C.11.9 mol/L | D.9 mol/L |
【知识点】 依据物质的量浓度公式的基础计算解读
二、解答题 添加题型下试题
【实验制备】
(1)将FeCl3溶液加到沸水中,加热至整个体系呈
(2)制备过程中,发生化学反应的方程式为
(3)小甲同学在制备时,加热时间过久,结果未能得到胶体。小甲得到的是
A.酸 B.碱 C.盐
【性质探究】
(4)小乙同学想证明Fe(OH)3胶体已经制备成功,他可以利用
(5)小丙同学利用

(6)小丁同学将提纯后的Fe(OH)3胶体置于U型管中(下图),通入直流电一段时间后,观察到与电源

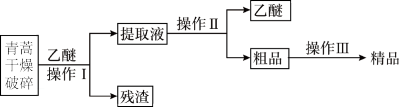
(1)对青蒿进行破碎的目的是
(2)操作I需要的玻璃仪器主要有:烧杯、玻璃棒、
(3)操作Ⅱ的名称是
(4)操作Ⅲ的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
①用电子天平称出相应质量的Na2CO3固体。把它放入烧杯中,加入适量的蒸馏水,使它完全溶解。
②把制得的溶液,小心地注入___________中。
③继续向容量瓶中加蒸馏水至液面距离刻度1-2cm处,改用________小心滴加蒸馏水至液面凹液面最低处与刻度线相切。
④用少量蒸馏水洗涤玻璃棒和烧杯2-3次,每次洗涤的液体都要小心的转入容量瓶中。
⑤将瓶塞塞紧,充分摇匀。
(1)请填写②和③处仪器名称
(2)需要称取碳酸钠固体
(3)操作步骤正确的顺序为
(4)溶液注入容量瓶先需恢复到室温,这是因为
(5)下列操作对配置溶液的浓度大小有何影响?
I.若没有进行步骤④,则所配溶液的浓度将会
A.偏大 B.偏小 C.无影响
Ⅱ.俯视刻度线,则所配制的溶液浓度将会
A.偏大 B.偏小 C.无影响
(6)定容时,取上述溶液100mL稀释至1000mL,所得溶液中钠离子的物质的量浓度为
(7)若实验过程中,加入蒸馏水时,不慎超过了刻度线,应如何处理?
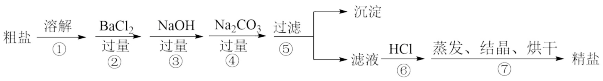
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是
(2)第②步操作加入过量的BaCl2目的是除去粗盐中的
(3)第⑤步“过滤”操作中得到沉淀的成分有泥沙
| A.BaSO4 | B.CaCO3 | C.BaCO3 | D.Mg(OH)2 |
(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是除去滤液中的NaOH和
(6)食盐水也可以通过电解得到更多种类的化工原料,写出电解饱和食盐水的化学方程式
【知识点】 氯碱工业解读 物质的分离、提纯 物质分离、提纯综合应用解读
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 无机物质的分类 单质和化合物 | |
| 2 | 0.65 | 气体摩尔体积 决定物质体积大小的微观因素 | |
| 3 | 0.94 | 物质的转化 | |
| 4 | 0.94 | 分散系概念及其分类 胶体的定义及分类 | |
| 5 | 0.65 | 分散系概念及其分类 胶体的性质和应用 | |
| 6 | 0.65 | 物质的量及单位——摩尔 摩尔质量 物质的量的含义 摩尔质量与相对原子质量区别与联系 | |
| 7 | 0.94 | 阿伏加德罗常数的求算 | |
| 8 | 0.94 | 22.4L/mol适用条件 阿伏加德罗定律及其推论 | |
| 9 | 0.65 | 气体摩尔体积概念 22.4L/mol适用条件 气体物质与NA相关的推算 | |
| 10 | 0.85 | 阿伏加德罗定律及其推论 物质的量有关计算 | |
| 11 | 0.65 | 氯气的实验室制法 常见气体的制备与收集 | |
| 12 | 0.85 | 化学实验基础操作 物质分离、提纯的常见物理方法 萃取和分液 | |
| 13 | 0.85 | 蒸发与结晶 萃取和分液 过滤 | |
| 14 | 0.85 | 焰色试验 | |
| 15 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 物质的检验 | |
| 16 | 0.65 | 氯离子的检验 | |
| 17 | 0.65 | 物质的量浓度计算-与溶质成分有关的计算 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液实验的仪器 | |
| 18 | 0.85 | 物质分离、提纯的常见物理方法 蒸发与结晶 | |
| 19 | 0.65 | 物质的量浓度计算-溶液稀释的有关计算 | |
| 20 | 0.65 | 依据物质的量浓度公式的基础计算 | |
| 二、解答题 | |||
| 21 | 0.85 | 胶体的制备 物质制备的探究 | 实验探究题 |
| 22 | 0.65 | 常用仪器及使用 化学实验基础操作 蒸馏与分馏 过滤 | 实验探究题 |
| 23 | 0.65 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 24 | 0.65 | 氯碱工业 物质的分离、提纯 物质分离、提纯综合应用 | 实验探究题 |



