8. 亚硝酰氯
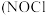
,熔点:
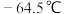
,沸点:
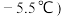
为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。是有机物合成中的重要试剂,常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置如图所示

其中III、IV中均为浓硫酸

:
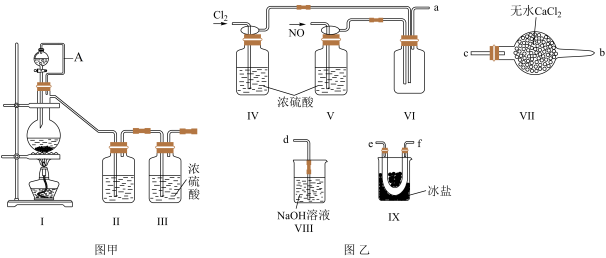
(1)用图甲中装置制备纯净干燥的原料气,补充下表中所缺少的药品。
| | 装置Ⅰ | 装置Ⅱ |
| | 烧瓶中 | 分液漏斗中 |
制备纯净 |  | 浓盐酸 |  _________________ _________________ |
| 制备纯净NO | Cu | 稀硝酸 |  _________________ _________________ |
(2)将制得的NO和

通入图乙对应装置制备NOCl。

装置连接顺序为
 ________
________
按气流自左向右方向,用小写字母表示

。

装置Ⅳ、Ⅴ除可进一步干燥NO、

外,还可以通过观察气泡的多少调节两种气体的流速。

有人认为可以将装置Ⅳ中浓硫酸合并到装置Ⅴ中,撤除装置Ⅳ,直接将NO、

通入装置Ⅴ中,你同意此观点吗?
_______
填“同意”或“不同意”

,原因是
___________。
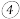
实验开始的时候,先通入氯气,再通入NO,原因为
________________________。
(3)有人认为多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储气的装置
______;
(4)装置Ⅶ吸收尾气时,NOCl发生反应的化学方程式为
_______________________。
(5)有人认为装置Ⅶ中氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资料发现用高锰酸钾溶液可以吸收NO气体,因此在装置Ⅶ氢氧化钠溶液中加入高锰酸钾,反应产生黑色沉淀,写出该反应的离子方程式:
__________________________________。
(6)制得的NOCl中可能含有少量

杂质,为测定产品纯度进行如下实验:称取
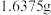
样品溶于

溶液中,加入几滴

溶液作指示剂,用足量硝酸酸化的
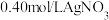
溶液滴定至产生砖红色沉淀,消耗

溶液

。则该样品的纯度为
__________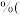
保留1位小数
