19. Ⅰ.水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态为B点。
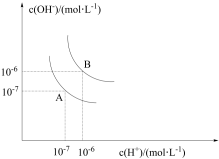
(1)在100℃时,
Kw的表达式为
________,在此温度下,
Kw的值为
________ mol
2/L
2。
(2)在室温下,将pH=9的Ba(OH)
2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)
2溶液与盐酸的体积比为
________。
(3)室温时将pH为3的硫酸溶液稀释100倍,稀释后溶液中,c(

)和c(H
+)之比为
________。
Ⅱ.现有溶质为①CH
3COOH,②HCl、③H
2SO
4的三种溶液,根据要求回答下列问题:
(1)写出①的电离方程式:
________。
(2)当它们pH相同时,其物质的量浓度最大的是
________(填序号)。
(3)当它们的物质的量浓度相同时,其pH最小的是
________(填序号)。
(4)在室温下,将c(H
+)均为0.1mol/L的三种酸分别加水稀释至原来的10倍,c(H
+)由大到小的顺序为
________(填序号)。
(5)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为
________。
(6)三种酸溶液的pH相同时,若消耗等量的Zn,则需三种酸溶液的体积大小关系为
________(填序号)。