 是被广泛应用的金属之一,铜器件在空气中久置会生成铜锈:
是被广泛应用的金属之一,铜器件在空气中久置会生成铜锈: 。回答下列问题:
。回答下列问题:(1)
 元素在元素周期表中的位置为
元素在元素周期表中的位置为 原子的核外电子排布式为
原子的核外电子排布式为 有
有(2)参与生成铜锈的物质
 中
中 原子的杂化方式为
原子的杂化方式为 分子的空间构型是
分子的空间构型是(3)
 的晶体类型是
的晶体类型是 含
含 σ键。
σ键。(4)
 、
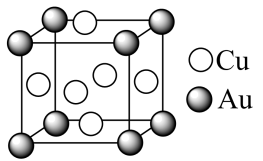
、 可形成金属互化物,其晶胞结构如图所示,若该
可形成金属互化物,其晶胞结构如图所示,若该 、
、 金属互化物的密度为
金属互化物的密度为 ,阿伏加 德罗常数为
,阿伏加 德罗常数为 ,则晶胞边长
,则晶胞边长 =
=
(5)金属铜单独与氨水或过氧化氢均不能反应,但可与过氧化氢和过量氨水的混合溶液反应生成一种配位化合物,其反应的化学方程式可表示为
更新时间:2020-05-19 08:34:22
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】按要求回答下列问题
(1)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有_______ 个C原子。
(2)CsCl晶体中每个Cs+周围有_________ 个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有________ 个。
(3)白磷分子中的键角为__________ ,分子的空间结构为__________ ,每个P原子与___ 个P原子结合成共价键。若将1分子白磷中的所有P-P键打开并各插入一个氧原子,共可结合_______ 个氧原子, 若每个P原子上的孤对电子再与氧原子配位,就可以得到磷的另一种氧化物_______________ (填分子式)。

(4)二氧化硅是一种________ 晶体,每个硅原子周围有_________ 个氧原子。
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____ 个硼原子组成,共含有________ 个B-B键。
(1)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有
(2)CsCl晶体中每个Cs+周围有
(3)白磷分子中的键角为

(4)二氧化硅是一种
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】元素周期表中第四周期元素在生产生活中有着广泛应用。
(1)锰元素在周期表中的位置是____ ,基态锰原子能量最高的电子的电子云形状为 ______ 。
(2)硒常用作半导体,基态硒原子的价电子排布图为_______ ;与硒同周期的p区元素中第一电离能大于硒的元素有______ 种;SeO2的空间构型是 _______ 。
(3)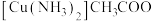 中碳原子的杂化类型是
中碳原子的杂化类型是____ ;已知: ;该反应中,肯定有
;该反应中,肯定有____ 形成(填标号)。
a.离子键 b.配位键 c.σ键 d.非极性键
(4)已知: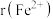 为62pm,
为62pm,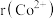 为66pm。在隔绝空气条件下分别加热FeCO3和CoCO3实验测得FeCO3的分解温度低于CoCO3,原因是
为66pm。在隔绝空气条件下分别加热FeCO3和CoCO3实验测得FeCO3的分解温度低于CoCO3,原因是 _______ 。
(5)某铁的氧化物晶胞如图所示:
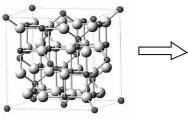
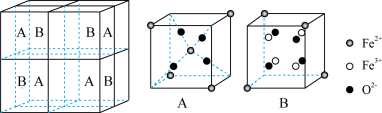
该晶胞可视为由A、B组成,则该氧化物与足量稀硝酸反应的化学方程式为_______ 。已知该晶体的晶胞参数为a pm,阿伏加 德罗常数的值为 ,该晶体的密度为
,该晶体的密度为______  (用含a和
(用含a和 的代数式表示)。
的代数式表示)。
(1)锰元素在周期表中的位置是
(2)硒常用作半导体,基态硒原子的价电子排布图为
(3)
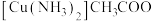 中碳原子的杂化类型是
中碳原子的杂化类型是 ;该反应中,肯定有
;该反应中,肯定有a.离子键 b.配位键 c.σ键 d.非极性键
(4)已知:
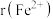 为62pm,
为62pm,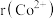 为66pm。在隔绝空气条件下分别加热FeCO3和CoCO3实验测得FeCO3的分解温度低于CoCO3,原因是
为66pm。在隔绝空气条件下分别加热FeCO3和CoCO3实验测得FeCO3的分解温度低于CoCO3,原因是 (5)某铁的氧化物晶胞如图所示:


该晶胞可视为由A、B组成,则该氧化物与足量稀硝酸反应的化学方程式为
 ,该晶体的密度为
,该晶体的密度为 (用含a和
(用含a和 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】物质结构与性质]单质铁、锂、砷及它们的化合物广泛应用于超导体材料等领域,回答下列问题:
(1)Fe原子的核外电子排布式为[Ar]_______ ,Li原子核外占据最高能层电子的电子云轮廓图形状为_______ 。
(2)As 的卤化物的熔点如下:
表中卤化物熔点差异的原因是_______ ,AsCl3分子的立体构型为_______ 。
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶体的密度是_______ g/cm3(用含a、NA的式子表示)。
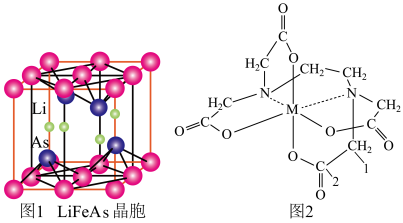
(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有_______ 个σ键,2号碳原子采取_______ 杂化方式;Fe3+与氮原子之间形成的化学键是_______ ,Fe3+的配位数为_______ ;该配合物中,第二周期的三种元素的第一电离能由大到小的顺序为_______ 。
(1)Fe原子的核外电子排布式为[Ar]
(2)As 的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是
(3)铁、锂、砷形成的化合物LiFeAs是一种超导体,其晶胞结构如图1所示,已知立方晶胞参数acm,则该晶体的密度是

(4)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图2所示,图中M代表Fe3+。则1号碳原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】物质的组成与结构决定了物质的性质与变化。回答下列问题:
(1)四水合磷酸锌[Zn3(PO4)2·4H2O]难溶于水,是一种性能优良的绿色环保防锈颜料。Zn2+的价层电子排布式是_______ , 中的磷原子的杂化轨道类型是
中的磷原子的杂化轨道类型是_______ , 离子的立体构型是
离子的立体构型是_______ 。
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)_______ I1(Pb)(填“大于”或“小于”)。
(3)新制的Cu(OH)2能够溶解于浓氨水中,原因是_______ (用离子方程式表示)。
(4)锌锰干电池中Zn2+可吸收电池反应产生的NH3生成[Zn(NH3)4]2+,1个该离子中含有_______ 个σ键。
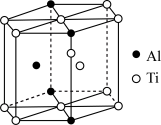
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为_______ ,其结构单元棱长为apm,底面边长为bpm,该合金的密度为_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)四水合磷酸锌[Zn3(PO4)2·4H2O]难溶于水,是一种性能优良的绿色环保防锈颜料。Zn2+的价层电子排布式是
 中的磷原子的杂化轨道类型是
中的磷原子的杂化轨道类型是 离子的立体构型是
离子的立体构型是(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)
(3)新制的Cu(OH)2能够溶解于浓氨水中,原因是
(4)锌锰干电池中Zn2+可吸收电池反应产生的NH3生成[Zn(NH3)4]2+,1个该离子中含有
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】选修X、Y、Z、W、R是元素周期表前四周期元素中的五种常见元素,其原子序数依次增大。X的基态原子的最外层电子排布式为nsnnpn+1。Y、Z同主族且ZY2是导致酸雨的主要物质之一。R位于ds区且原子最外层只有一个电子。W原子次外层电子数为最外层电子数的7倍。回答下列问题:
(1)W位于元素周期表第________ 周期________ 族,其基态原子的核外电子排布式为________ 。
(2)Y的气态氢化物稳定性比Z的气态氢化物的稳定性_______ (填“强”或“弱”)。Y的第一电离能比Z的_________ (填“大”或“小”)。
(3)X的最常见的气体氢化物分子的VSEPR模型为___________ ,分子间的空间构型是________ 。
(4)原子总数相同、价电子总数相同的分子或离子成为等电子体。分别写出一种与XO2-互为等电子体的单质和化合物的化学式___________ 、_______________ 。XO2-的中心原子的杂化轨道类型为________ 。
(5)[W(CN)6]3-离子中W的阳离子与CN-之间的共价键称为__________________ ,该化学键能够形成的原因是______________ 。
(6)下图是R晶体的晶胞结构示意图,每个晶胞中含有_____________ 个R原子。

(1)W位于元素周期表第
(2)Y的气态氢化物稳定性比Z的气态氢化物的稳定性
(3)X的最常见的气体氢化物分子的VSEPR模型为
(4)原子总数相同、价电子总数相同的分子或离子成为等电子体。分别写出一种与XO2-互为等电子体的单质和化合物的化学式
(5)[W(CN)6]3-离子中W的阳离子与CN-之间的共价键称为
(6)下图是R晶体的晶胞结构示意图,每个晶胞中含有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++
2CuCl↓+4H++ 、2CuCl2+SnCl2=2CuCl↓+SnCl4
、2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)C、N、O三种元素的第一电离能由大到小的顺序是_______ 。
(2)SO2分子的空间构型为_______ ;与SnCl4互为等电子体的一种离子的化学式为____ 。
(3)乙二胺分子中氮原子轨道的杂化类型为_______ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_______ 。
(4)②中所形成的配离子中含有的化学键类型有_______(填字母)。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:2Cu2++2Cl-+SO2+2H2O
 2CuCl↓+4H++
2CuCl↓+4H++ 、2CuCl2+SnCl2=2CuCl↓+SnCl4
、2CuCl2+SnCl2=2CuCl↓+SnCl4②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)C、N、O三种元素的第一电离能由大到小的顺序是
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)②中所形成的配离子中含有的化学键类型有_______(填字母)。
| A.配位键 | B.极性键 | C.离子键 | D.非极性键 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3,[Fe(H2NCONH2)6](NO3)3等。
(1)Fe2+基态核外电子排布式为___ 。
(2)与CN-互为等电子体的一种分子是:___ ,CN-可在TiO2作光催化剂下转化为OCN-,OCN-中三种元素的电负性由大到小的顺序为___ ,尿素(H2NCONH2)分子中C、N原子的杂化方式分别为___ 和___ 。
(3)NO3-的空间构型为___ ,1molFe(CN)63-中含有σ键的数目为___ 。
(4)铁的另一种配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则X=___ ,已知该配合物的熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)X晶体属于___ (填晶体类型)。
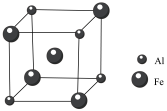
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。则这种晶胞中,离Al原子最近且距离相等的Fe原子有___ 个,该晶体的密度的计算式为:___ (不用化简,已知小立方体的边长为acm,阿伏加 德罗常数的值为NA)。
(1)Fe2+基态核外电子排布式为
(2)与CN-互为等电子体的一种分子是:
(3)NO3-的空间构型为
(4)铁的另一种配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则X=
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。则这种晶胞中,离Al原子最近且距离相等的Fe原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮族元素是元素周期表中的一类重要的元素,其单质及化合物在生活、工农业与科学研究中发挥了重要作用。
(1)As是氮族元素,则基态As的价层电子轨道表示式是_______ 。
(2)氮的单质及化合物的相互转化关系如图所示:

上述反应中,只涉及极性键的断裂与形成的是反应_______ (填编号),NH3中H-N-H的键角_______ (填“>”“<”或“=”)109°28', 的空间构型为
的空间构型为_______ 。
(3)亚胺硫磷(结构简式如图所示)是一种传统农药,可用于防治水稻、棉花、果树、蔬菜等多种作物害虫。

①组成元素中N、P、S的第一电离能由大到小的顺序是_______ 。
②该化合物易溶于苯、CCl4,微溶于水,其可能原因是_______ 。
(4)一种含Ca、As的铁基超导材料的晶胞结构如图所示(所有的Ca原子具有相同的化学环境):

①该超导材料中Fe元素的化合价为_______ 价,Ca的配位数是_______ 。
②该晶胞的参数为m pm、m pm、n pm,a处As的原子分数坐标为(0.5,0.5,0.128)。晶胞中x=_______ (用含n的代数式表示)。
(1)As是氮族元素,则基态As的价层电子轨道表示式是
(2)氮的单质及化合物的相互转化关系如图所示:

上述反应中,只涉及极性键的断裂与形成的是反应
 的空间构型为
的空间构型为(3)亚胺硫磷(结构简式如图所示)是一种传统农药,可用于防治水稻、棉花、果树、蔬菜等多种作物害虫。

①组成元素中N、P、S的第一电离能由大到小的顺序是
②该化合物易溶于苯、CCl4,微溶于水,其可能原因是
(4)一种含Ca、As的铁基超导材料的晶胞结构如图所示(所有的Ca原子具有相同的化学环境):

①该超导材料中Fe元素的化合价为
②该晶胞的参数为m pm、m pm、n pm,a处As的原子分数坐标为(0.5,0.5,0.128)。晶胞中x=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氢、碳、氮都是重要的非金属元素,它们单质及其化合物在科学研究和工业生产中有重要的应用。
(1)下列微粒基态的电子排布中未成对电子数最多的是_______ (填序号)
a.Fe
b.Mn
c.Cu
d.Cr
e.C
(2)含氮配合物W的结构如图所示(配位键未标出方向),请在结构图中用“→”标出W中所存在的所有配位键的方向。

(3)C、H元素形成的某有机化合物分子中共有16个电子,该分子中 键与
键与 键的个数比为
键的个数比为_______ ;该有机化合物在一定条件下形成的聚合物中C原子采取_______ 杂化。
(4)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为_______ 。该化合物的相对分子质量为M, 为阿伏加德罗常数。若该晶胞的边长为a pm,则该晶体的密度是
为阿伏加德罗常数。若该晶胞的边长为a pm,则该晶体的密度是_______ g.pm 。
。

(1)下列微粒基态的电子排布中未成对电子数最多的是
a.Fe
b.Mn
c.Cu
d.Cr
e.C
(2)含氮配合物W的结构如图所示(配位键未标出方向),请在结构图中用“→”标出W中所存在的所有配位键的方向。

(3)C、H元素形成的某有机化合物分子中共有16个电子,该分子中
 键与
键与 键的个数比为
键的个数比为(4)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为
 为阿伏加德罗常数。若该晶胞的边长为a pm,则该晶体的密度是
为阿伏加德罗常数。若该晶胞的边长为a pm,则该晶体的密度是 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】磷及其化合物在工业生产中起着重要的作用。
(1)基态磷原子价电子的轨道表示式是_______ 。
(2)磷元素有白磷、黑磷等常见的单质。
①白磷(P4)是分子晶体,易溶于CS2,难溶于水,可能原因是_______ 。
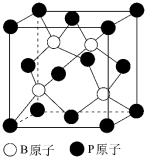
②黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体是与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_______ (填字母序号)
b.分子中磷原子杂化方式为sp2杂化
c.是混合型晶体
(3)Fe3+与水会形成黄色的配离子[Fe(OH)]2+,为避免颜色干扰,常在Fe3+溶液中加入H3PO4形成无色的[Fe(PO4)2]3-。由此推测与Fe3+形成的配离子更稳定的配体是_______ ,其空间构型是_______ 。
(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟的熔点分别为2000、1070℃,从结构角度说明其熔点差异的原因_____ 。
②磷化硼是一种半导体材料,晶胞结构如下图所示。已知晶胞边长apm,阿伏加德罗常数为NA,磷化硼晶体的密度是_______ g/cm3.(1pm=10-10cm)
(1)基态磷原子价电子的轨道表示式是
(2)磷元素有白磷、黑磷等常见的单质。
①白磷(P4)是分子晶体,易溶于CS2,难溶于水,可能原因是
②黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体是与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

b.分子中磷原子杂化方式为sp2杂化
c.是混合型晶体
(3)Fe3+与水会形成黄色的配离子[Fe(OH)]2+,为避免颜色干扰,常在Fe3+溶液中加入H3PO4形成无色的[Fe(PO4)2]3-。由此推测与Fe3+形成的配离子更稳定的配体是
(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟的熔点分别为2000、1070℃,从结构角度说明其熔点差异的原因
②磷化硼是一种半导体材料,晶胞结构如下图所示。已知晶胞边长apm,阿伏加德罗常数为NA,磷化硼晶体的密度是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】草酸镍常用作催化剂或生产镍催化剂。某科研小组利用含镍废料(主要成分为NiS,另含Zn、Fe、CaO、SiO2等)制备草酸镍晶体的工艺流程如图:
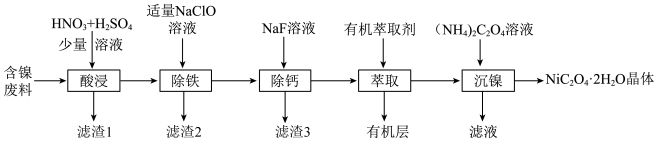
已知:①常温下Ksp(CaF2)=4×10-9;②当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀。回答下列问题:
(1)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:________ 。
(2)除铁时,不同的条件下可以得到不同的滤渣2。滤渣2的成分与温度、pH的关系如图所示。温度60℃、pH=6时,滤渣2的主要成分是________ ;设计简单实验方案检验滤液中是否含有Fe2+:_______ 。

(3)已知“除铁”后所得100mL溶液中c(Ca2+)=0.01mol•L-1,加入100mLNH4F溶液(忽略混合后溶液体积的变化),使Ca2+恰好沉淀完全,则所加溶液c(NH4F)=________ mol•L-1(不考虑F-的水解)。
(4)沉镍工序主要过程为:蒸发浓缩、________ 、过滤所得固体,用75%的乙醇洗涤、110℃下烘干,得到草酸镍晶体,其中用75%的乙醇洗涤的目的是________ 。
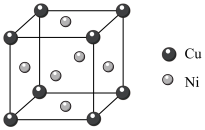
(5)镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。
①晶胞中铜原子与镍原子的原子个数比为_______ 。
②已知一定条件下晶胞的棱长为acm,用NA表示阿伏加德罗常数的值,在该条件下该晶体的摩尔体积为________ m3•mol-1(用含a、NA的代数式表示)。

已知:①常温下Ksp(CaF2)=4×10-9;②当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀。回答下列问题:
(1)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:
(2)除铁时,不同的条件下可以得到不同的滤渣2。滤渣2的成分与温度、pH的关系如图所示。温度60℃、pH=6时,滤渣2的主要成分是

(3)已知“除铁”后所得100mL溶液中c(Ca2+)=0.01mol•L-1,加入100mLNH4F溶液(忽略混合后溶液体积的变化),使Ca2+恰好沉淀完全,则所加溶液c(NH4F)=
(4)沉镍工序主要过程为:蒸发浓缩、
(5)镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。

①晶胞中铜原子与镍原子的原子个数比为
②已知一定条件下晶胞的棱长为acm,用NA表示阿伏加德罗常数的值,在该条件下该晶体的摩尔体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】电池级碳酸锂是制造 等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含
等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含 、
、 、
、 、
、 等)为原料制取电池级
等)为原料制取电池级 的工艺流程如图:
的工艺流程如图: 为有机萃取剂,难溶于水,可萃取
为有机萃取剂,难溶于水,可萃取 ,萃取时发生的反应可表示为:
,萃取时发生的反应可表示为: ;
;
②常温时,
 溶液的
溶液的 。
。
回答下列问题:
(1)“有机层”的主要成分为___________ (填化学式,下同);“滤渣1”中含有的物质为___________ 和 ;使用
;使用 萃取剂时,需加入一定量的
萃取剂时,需加入一定量的 进行处理,其目的是
进行处理,其目的是___________ 。
(2)某种 的结构简式为
的结构简式为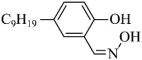 ,该分子中可能与
,该分子中可能与 形成配位键的原子有
形成配位键的原子有___________ 。
(3)加适量草酸的目的___________ 。
(4)“混合沉锂”的离子方程式为___________ 。
(5) 与
与 在空气中加热可以制备重要的电极材料钴酸锂(
在空气中加热可以制备重要的电极材料钴酸锂( )。写出对应的化学方程式
)。写出对应的化学方程式___________ 。
(6)钴酸锂( )是常见的锂离子电池正极材料,其晶胞结构示意图如图所示,各离子位于晶胞的顶点、棱和体内。
)是常见的锂离子电池正极材料,其晶胞结构示意图如图所示,各离子位于晶胞的顶点、棱和体内。___________ 。
②该晶胞密度为___________  。(写出计算式,阿伏加德罗常数为
。(写出计算式,阿伏加德罗常数为 )
)
 等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含
等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含 、
、 、
、 、
、 等)为原料制取电池级
等)为原料制取电池级 的工艺流程如图:
的工艺流程如图: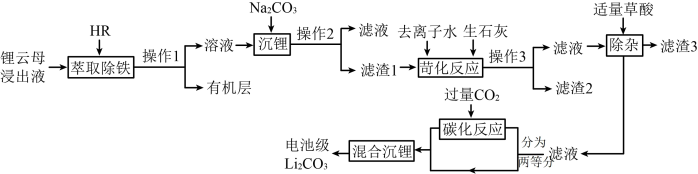
 为有机萃取剂,难溶于水,可萃取
为有机萃取剂,难溶于水,可萃取 ,萃取时发生的反应可表示为:
,萃取时发生的反应可表示为: ;
;②常温时,

 溶液的
溶液的 。
。回答下列问题:
(1)“有机层”的主要成分为
 ;使用
;使用 萃取剂时,需加入一定量的
萃取剂时,需加入一定量的 进行处理,其目的是
进行处理,其目的是(2)某种
 的结构简式为
的结构简式为 ,该分子中可能与
,该分子中可能与 形成配位键的原子有
形成配位键的原子有(3)加适量草酸的目的
(4)“混合沉锂”的离子方程式为
(5)
 与
与 在空气中加热可以制备重要的电极材料钴酸锂(
在空气中加热可以制备重要的电极材料钴酸锂( )。写出对应的化学方程式
)。写出对应的化学方程式(6)钴酸锂(
 )是常见的锂离子电池正极材料,其晶胞结构示意图如图所示,各离子位于晶胞的顶点、棱和体内。
)是常见的锂离子电池正极材料,其晶胞结构示意图如图所示,各离子位于晶胞的顶点、棱和体内。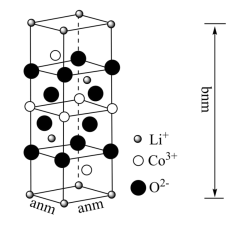
②该晶胞密度为
 。(写出计算式,阿伏加德罗常数为
。(写出计算式,阿伏加德罗常数为 )
)
您最近一年使用:0次



