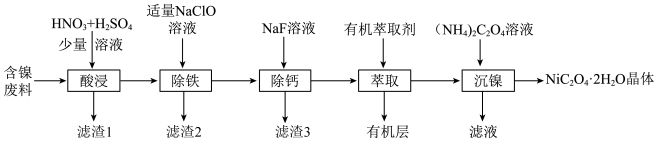
草酸镍常用作催化剂或生产镍催化剂。某科研小组利用含镍废料(主要成分为NiS,另含Zn、Fe、CaO、SiO2等)制备草酸镍晶体的工艺流程如图:
已知:①常温下Ksp(CaF2)=4×10-9;②当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀。回答下列问题:
(1)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:________ 。
(2)除铁时,不同的条件下可以得到不同的滤渣2。滤渣2的成分与温度、pH的关系如图所示。温度60℃、pH=6时,滤渣2的主要成分是________ ;设计简单实验方案检验滤液中是否含有Fe2+:_______ 。

(3)已知“除铁”后所得100mL溶液中c(Ca2+)=0.01mol•L-1,加入100mLNH4F溶液(忽略混合后溶液体积的变化),使Ca2+恰好沉淀完全,则所加溶液c(NH4F)=________ mol•L-1(不考虑F-的水解)。
(4)沉镍工序主要过程为:蒸发浓缩、________ 、过滤所得固体,用75%的乙醇洗涤、110℃下烘干,得到草酸镍晶体,其中用75%的乙醇洗涤的目的是________ 。
(5)镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。
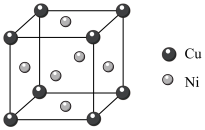
①晶胞中铜原子与镍原子的原子个数比为_______ 。
②已知一定条件下晶胞的棱长为acm,用NA表示阿伏加德罗常数的值,在该条件下该晶体的摩尔体积为________ m3•mol-1(用含a、NA的代数式表示)。

已知:①常温下Ksp(CaF2)=4×10-9;②当某物质浓度小于1.0×10-5mol•L-1时,视为完全沉淀。回答下列问题:
(1)酸浸过程中,1molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:
(2)除铁时,不同的条件下可以得到不同的滤渣2。滤渣2的成分与温度、pH的关系如图所示。温度60℃、pH=6时,滤渣2的主要成分是

(3)已知“除铁”后所得100mL溶液中c(Ca2+)=0.01mol•L-1,加入100mLNH4F溶液(忽略混合后溶液体积的变化),使Ca2+恰好沉淀完全,则所加溶液c(NH4F)=
(4)沉镍工序主要过程为:蒸发浓缩、
(5)镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。

①晶胞中铜原子与镍原子的原子个数比为
②已知一定条件下晶胞的棱长为acm,用NA表示阿伏加德罗常数的值,在该条件下该晶体的摩尔体积为
更新时间:2023-09-28 09:59:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化铈( )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
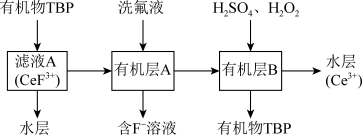
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。
回答下列问题:
(1)滤渣A的主要成分是________ (填化学式);“酸浸”不用盐酸的理由是________ (答一点即可)。
(2)“系列操作”包含以下几个过程:已知: 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: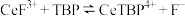 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是________ ,“有机层B”中发生反应的离子方程式为________ 。水层中的一种溶质,理论上可以在工艺流程图中的________ 工序中循环利用,减小“调pH”工序中 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于________ (已知25℃时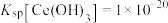 )。
)。
(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为________ 。
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是________ ;晶体中一个Ce周围与其最近的O的个数为________ 。
 )是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含
)是一种典型的金属氧化物,具有较强的氧化性广泛应用于多相催化反应,并作为汽车尾气净化的三效催化剂的重要组成成分。以氟碳铈矿(主要含 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如下图所示:
的一种工艺流程如下图所示: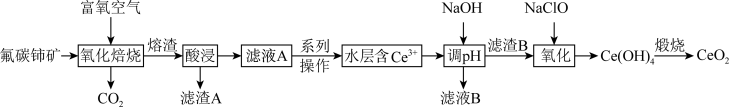
 和
和 ;②滤液A中含:
;②滤液A中含: 、
、 等离子。
等离子。回答下列问题:
(1)滤渣A的主要成分是
(2)“系列操作”包含以下几个过程:已知:
 不能溶于有机物TBP;
不能溶于有机物TBP; 能溶于有机物TBP,且存在反应:
能溶于有机物TBP,且存在反应: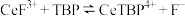 。“滤液A”中加入有机物TBP后的分离方法是
。“滤液A”中加入有机物TBP后的分离方法是 的用量,节约生产成本。
的用量,节约生产成本。
(3)“调pH”中,要使
 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制pH大于
为沉淀完全),应控制pH大于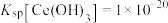 )。
)。(4)“氧化”中,NaClO转化为NaCl,则氧化剂与还原剂的物质的量之比为
(5)二氧化铈立方晶胞如图所示,则铈原子Ce在晶胞中的位置是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】皓矾( )主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为
)主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为 ,还含有少量
,还含有少量 以及Ca、Mg、Fe、Cu等的化合物)制备,制备流程图如下:
以及Ca、Mg、Fe、Cu等的化合物)制备,制备流程图如下:

已知:常温下,金属离子开始沉淀和完全沉淀( )时的pH如下表所示:
)时的pH如下表所示:
回答下列问题:
(1)“浸取”工序中,能加快浸取效率的措施有___________ (任写一种作答)。
(2)“氧化”时需控制温度在40~45℃进行反应,高于45℃的后果是___________ 。
(3)若“调pH过滤”工序中,调节溶液 ,所得“滤渣②”的主要成分有
,所得“滤渣②”的主要成分有 ,则此时“滤液②”中
,则此时“滤液②”中 为
为___________ mol/L。
(4)“滤渣③”经化学除锌、物理加工处理后可得电极材料A,经电解法可在镀件上镀上一层铜。则电解时电极材料A发生的电极反应式是___________ 。
(5)“滤渣④”中含有 和
和 ,可与热的浓硫酸反应制备氢氟酸,写出
,可与热的浓硫酸反应制备氢氟酸,写出 与热的浓硫酸反应的化学方程式
与热的浓硫酸反应的化学方程式___________ 。利用氢氟酸可制取杀鼠药氟乙酸( ),氟乙酸的酸性
),氟乙酸的酸性___________ (填“大于”“等于”或“小于”)乙酸的酸性。
(6)从滤液④获得皓矾晶体的具体操作为蒸发浓缩、___________ 、过滤、洗涤、干燥。
 )主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为
)主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为 ,还含有少量
,还含有少量 以及Ca、Mg、Fe、Cu等的化合物)制备,制备流程图如下:
以及Ca、Mg、Fe、Cu等的化合物)制备,制备流程图如下:
已知:常温下,金属离子开始沉淀和完全沉淀(
 )时的pH如下表所示:
)时的pH如下表所示:| 金属离子 |  |  |  |  |  |
| 开始沉淀时pH | 1.9 | 6.4 | 4.7 | 7.0 | 9.1 |
| 沉淀完全时pH | 3.4 | 8.4 | 6.7 | 9.0 | 11.1 |
(1)“浸取”工序中,能加快浸取效率的措施有
(2)“氧化”时需控制温度在40~45℃进行反应,高于45℃的后果是
(3)若“调pH过滤”工序中,调节溶液
 ,所得“滤渣②”的主要成分有
,所得“滤渣②”的主要成分有 ,则此时“滤液②”中
,则此时“滤液②”中 为
为(4)“滤渣③”经化学除锌、物理加工处理后可得电极材料A,经电解法可在镀件上镀上一层铜。则电解时电极材料A发生的电极反应式是
(5)“滤渣④”中含有
 和
和 ,可与热的浓硫酸反应制备氢氟酸,写出
,可与热的浓硫酸反应制备氢氟酸,写出 与热的浓硫酸反应的化学方程式
与热的浓硫酸反应的化学方程式 ),氟乙酸的酸性
),氟乙酸的酸性(6)从滤液④获得皓矾晶体的具体操作为蒸发浓缩、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为 。某探究小组回收处理流程如图:
。某探究小组回收处理流程如图:

回答下列问题:
(1)硒(Se)位于元素周期表第_______ 周期,第_______ 族。
(2)“酸浸氧化”发生的主要氧化还原反应的离子方程式为_______ 。
(3)已知:25℃, ,
, ,
, ,当金属阳离子浓度小于
,当金属阳离子浓度小于 时沉淀完全,
时沉淀完全, 恰好完全沉淀时溶液的pH约为
恰好完全沉淀时溶液的pH约为_______ (保留一位小数);为探究 在氨水中能否溶解,计算反应
在氨水中能否溶解,计算反应 的平衡常数
的平衡常数
_______ 。(已知: ,
, )
)
(4)“滤渣”与 混合前需要洗涤、干燥,检验滤渣中
混合前需要洗涤、干燥,检验滤渣中 是否洗净的试剂和用品是
是否洗净的试剂和用品是_______ 。
(5)“高温气相沉积”过程中发生的化学反应方程式为_______ 。
 。某探究小组回收处理流程如图:
。某探究小组回收处理流程如图:
回答下列问题:
(1)硒(Se)位于元素周期表第
(2)“酸浸氧化”发生的主要氧化还原反应的离子方程式为
(3)已知:25℃,
 ,
, ,
, ,当金属阳离子浓度小于
,当金属阳离子浓度小于 时沉淀完全,
时沉淀完全, 恰好完全沉淀时溶液的pH约为
恰好完全沉淀时溶液的pH约为 在氨水中能否溶解,计算反应
在氨水中能否溶解,计算反应 的平衡常数
的平衡常数
 ,
, )
)(4)“滤渣”与
 混合前需要洗涤、干燥,检验滤渣中
混合前需要洗涤、干燥,检验滤渣中 是否洗净的试剂和用品是
是否洗净的试剂和用品是(5)“高温气相沉积”过程中发生的化学反应方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】硅与储及其化合物在医药、生产、生活中有着重要的作用。回答下列问题:
(1)某铁的配合物结构如图所示,可由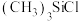 与
与 混合加热制得。
混合加热制得。_______ 区。C、O、H三种元素的电负性从大到小的顺序为_______ 。
②配位体CO分子中碳元素提供孤电子对的原因:_______ 。铁的配合物中碳元素的杂化方式共有_______ 种。
③在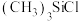 、
、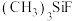 、
、 中,
中,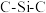 键角最大的是
键角最大的是_______ 。
(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表(已知:绝对零度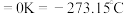 ):
):
0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是_______ (填化学式),沸点依次升高的原因是_______ ,气态SiX4分子的空间结构是_______ 。
(3)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):_______ (填“b”“c”或“d”)图也能表示此化合物的晶胞。
②已知晶胞(a)密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为_______ (用含x、y、z和ρ的式子表示)。
(1)某铁的配合物结构如图所示,可由
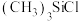 与
与 混合加热制得。
混合加热制得。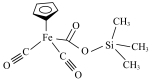
②配位体CO分子中碳元素提供孤电子对的原因:
③在
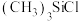 、
、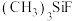 、
、 中,
中,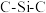 键角最大的是
键角最大的是(2)硅和卤素单质反应可以得到SiX4,SiX4的熔沸点如下表(已知:绝对零度
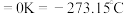 ):
):| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(3)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):
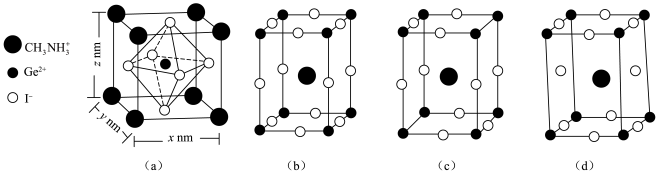
②已知晶胞(a)密度为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】(1)某短周期金属元素R的部分电离能情况如图Ⅰ所示,则元素 R 位于周期表第_______ 族,其基态原子的电子排布式是_______ 。图Ⅱ中A、B、C、D是四种不同主族元素的气态氢化物,其中 A 比 B 分子沸点高的可能原因是_______ 。

(2)图Ⅱ中 C 物质能与很多化合物通过配位键发生相互作用。例如:C 与第二周期中的另一种元素的氢化物相互作用得到的化合物 X 是科学家潜心研究的一种储氢材料,X 是乙烷的等电子体;加热 X 会缓慢释放 H2,转变为化合物 Y,Y 是乙烯的等电子体。
①化合物 C 的分子立体构型为_______ ,X 的结构式为_______ (必须标明配位键)。
②形成 C 物质的中心原子在 X、Y 分子中的杂化方式分别是_______ ,Y 分子中σ键和π键数目之比为_______ 。
(3)过渡金属钛有“生物金属”之称,其化合态以+4价最稳定。回答下列问题:
①工业上通过蒸馏还原 TiCl4制得单质钛。常温下 TiCl4是一种有刺激性臭味的无色液体,熔点-23.2 ℃,沸点136.2 ℃,推断 TiCl4属于_______ 晶体。
②Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色)、[TiCl(H2O)5]Cl2·H2O(绿色),两者配位数_______ (填“相同”或“不同”),绿色晶体中配体是_______ 。
③TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常为链状聚合形式的阳离子,其结构形式如图Ⅲ,化学式为_______ 。

④TiO2与BaCO3一起熔融可制得偏钛酸钡,该物质热稳定性好,介电常数高,是制造大容量电容器的极好材料。该晶体晶胞的结构示意图如图Ⅳ。请写出制备偏钛酸钡的化学方程式:_______ 。

(2)图Ⅱ中 C 物质能与很多化合物通过配位键发生相互作用。例如:C 与第二周期中的另一种元素的氢化物相互作用得到的化合物 X 是科学家潜心研究的一种储氢材料,X 是乙烷的等电子体;加热 X 会缓慢释放 H2,转变为化合物 Y,Y 是乙烯的等电子体。
①化合物 C 的分子立体构型为
②形成 C 物质的中心原子在 X、Y 分子中的杂化方式分别是
(3)过渡金属钛有“生物金属”之称,其化合态以+4价最稳定。回答下列问题:
①工业上通过蒸馏还原 TiCl4制得单质钛。常温下 TiCl4是一种有刺激性臭味的无色液体,熔点-23.2 ℃,沸点136.2 ℃,推断 TiCl4属于
②Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色)、[TiCl(H2O)5]Cl2·H2O(绿色),两者配位数
③TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常为链状聚合形式的阳离子,其结构形式如图Ⅲ,化学式为

④TiO2与BaCO3一起熔融可制得偏钛酸钡,该物质热稳定性好,介电常数高,是制造大容量电容器的极好材料。该晶体晶胞的结构示意图如图Ⅳ。请写出制备偏钛酸钡的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】电负性与电离能是两种定量描述元素原子得失电子能力的参数,请回答下列问题:
(1)非金属性强弱:O____ Cl(填“>”或“<”)。
(2)依据电负性数值,上述元素的原子最容易形成离子键的是____ 和____ (填元素符号)。
(3)某元素Y,其基态原子核外有2个电子层,3个未成对电子,该元素是____ (填元素符号),Y元素电负性的取值范围是____ 。
(4)二氟化氧的结构式为F—O—F,氧元素的化合价为____ ,该分子属于____ 分子(填“极性”或“非极性”)。
(5)已知苯可与ICl发生取代反应,利用电负性相关知识预测反应产物:____ 。
 +I—Cl
+I—Cl ____+____
____+____
(6)随着原子序数的递增,元素气态基态原子的第一电离能呈现起伏变化,而电负性的规律性更强。结合原子核外电子排布式解释Mg的第一电离能比Al的高的原因____ 。

(7)已知SiO2晶胞的棱长均为apm,则SiO2晶体的密度ρ=____ g·cm-3(列出计算式)。

| 元素符号 | H | C | O | F | Mg | Al | Cl |
| 电负性 | 2.1 | 2.5 | 3.5 | 4.0 | 1.2 | 1.5 | 3.0 |
(2)依据电负性数值,上述元素的原子最容易形成离子键的是
(3)某元素Y,其基态原子核外有2个电子层,3个未成对电子,该元素是
(4)二氟化氧的结构式为F—O—F,氧元素的化合价为
(5)已知苯可与ICl发生取代反应,利用电负性相关知识预测反应产物:
 +I—Cl
+I—Cl ____+____
____+____(6)随着原子序数的递增,元素气态基态原子的第一电离能呈现起伏变化,而电负性的规律性更强。结合原子核外电子排布式解释Mg的第一电离能比Al的高的原因

(7)已知SiO2晶胞的棱长均为apm,则SiO2晶体的密度ρ=

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业.CuCl 难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu 和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl 的工艺过程如下:
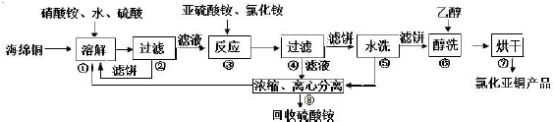
回答下列问题:
(1)步骤①中真正的氧化剂是___________ ,溶解温度应控制在60-70 度,原因是___________ ;
(2)写出步骤③中主要反应的离子方程式是___________ ;
(3)步骤⑧是分离滤液和洗涤液操作,实验室里混有杂质NaCl 的(NH4)2SO4 固体提纯的方法是___________ ;
(4)上述工艺中,步骤⑥不能省略,理由是___________ ;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有___________ (填字母).
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L 的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl 的质量分数为___________ 。

回答下列问题:
(1)步骤①中真正的氧化剂是
(2)写出步骤③中主要反应的离子方程式是
(3)步骤⑧是分离滤液和洗涤液操作,实验室里混有杂质NaCl 的(NH4)2SO4 固体提纯的方法是
(4)上述工艺中,步骤⑥不能省略,理由是
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有
| A.离心机 | B.分馏塔 | C.框式压滤机 | D.反应釜 |
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L 的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl 的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】二氯化砜( )又名磺酰氯,熔点为-54.1℃,沸点69.1℃,常温较稳定,遇水剧烈反应,100℃以上易分解。主要用作氯化剂或氯磺化剂。实验室可利用
)又名磺酰氯,熔点为-54.1℃,沸点69.1℃,常温较稳定,遇水剧烈反应,100℃以上易分解。主要用作氯化剂或氯磺化剂。实验室可利用 和
和 在活性炭催化下发生反应:
在活性炭催化下发生反应: ,得到少量
,得到少量 ,装置如图(部分夹持装置已省略)。请回答相应问题:
,装置如图(部分夹持装置已省略)。请回答相应问题:___________ ;冷凝管的进水口为___________ (填“m”或“n”)。
(2)以上装置按气流方向的连接顺序为___________ →g、h←___________ (用小写字母填写,且装置可重复使用)。连接装置后,应进行的操作是___________ 。
(3)装置甲中发生反应的离子方程式___________ ;装置乙发生反应时浓硫酸体现的性质是___________ 。
(4)球形干燥管中的碱石灰的作用为___________ 。
(5)装置戊中仪器A置于冷水浴中,其原因是___________ 。
(6)某实验小组利用上述装置(浓盐酸、 均足量),最后得到纯净的磺酰氯
均足量),最后得到纯净的磺酰氯 ,则磺酰氯的产率为
,则磺酰氯的产率为___________ (保留三位有效数字)。
 )又名磺酰氯,熔点为-54.1℃,沸点69.1℃,常温较稳定,遇水剧烈反应,100℃以上易分解。主要用作氯化剂或氯磺化剂。实验室可利用
)又名磺酰氯,熔点为-54.1℃,沸点69.1℃,常温较稳定,遇水剧烈反应,100℃以上易分解。主要用作氯化剂或氯磺化剂。实验室可利用 和
和 在活性炭催化下发生反应:
在活性炭催化下发生反应: ,得到少量
,得到少量 ,装置如图(部分夹持装置已省略)。请回答相应问题:
,装置如图(部分夹持装置已省略)。请回答相应问题:

(2)以上装置按气流方向的连接顺序为
(3)装置甲中发生反应的离子方程式
(4)球形干燥管中的碱石灰的作用为
(5)装置戊中仪器A置于冷水浴中,其原因是
(6)某实验小组利用上述装置(浓盐酸、
 均足量),最后得到纯净的磺酰氯
均足量),最后得到纯净的磺酰氯 ,则磺酰氯的产率为
,则磺酰氯的产率为
您最近一年使用:0次
【推荐3】二氧化锗(GeO2)可用于光谱分析和制备催化剂、半导体材料。对ISP炼锌过程所得锗渣(主要成分GeO、GeO2、ZnO·Fe2O3,含有SiO2、难溶物杂质)进行处理的流程如下:

已知:Ksp[Zn(OH)2]=1.0×10-17, Ksp[Fe(OH)3]=1.0×10-38;溶液中离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。
回答下列问题:
(1)二氧化锗(GeO2)中锗元素的化合价______________ 。
(2)“调pH”时,首先生成沉淀的离子为____ (填离子符号),该离子恰好沉淀完全的pH为____________ 。
(3)“还原焙烧”过程中,主要反应的氧化剂与还原剂的物质的量之比为___________ 。
(4)“氧化吸收”过程中,主要反应的离子方程式为_______________ ;在一定时间内GeO的氧化吸收率与温度的关系如图所示。T0℃时吸收率最高的原因为_____________________________ 。
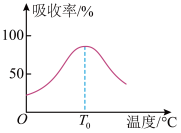
(5)实验室进行“氯化蒸馏”时,蒸馏所用的主要玻璃仪器有酒精灯、锥形瓶、直形冷凝管、牛角管和____________ 。
(6)“水解”时,需控制温度为95℃的目的为______________ 。

已知:Ksp[Zn(OH)2]=1.0×10-17, Ksp[Fe(OH)3]=1.0×10-38;溶液中离子浓度≤10-5mol·L-1时,认为该离子沉淀完全。
回答下列问题:
(1)二氧化锗(GeO2)中锗元素的化合价
(2)“调pH”时,首先生成沉淀的离子为
(3)“还原焙烧”过程中,主要反应的氧化剂与还原剂的物质的量之比为
(4)“氧化吸收”过程中,主要反应的离子方程式为

(5)实验室进行“氯化蒸馏”时,蒸馏所用的主要玻璃仪器有酒精灯、锥形瓶、直形冷凝管、牛角管和
(6)“水解”时,需控制温度为95℃的目的为
您最近一年使用:0次



