高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=
Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=__ ,又知1100℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数__ (填“变大”、“变小”或“不变”)。
(2)1100℃时测得高炉中c(CO2)=0.013mol/L,c(CO)=0.05mol/L,在这种情况下,该反应是否处于化学平衡状态:__ (填“是”或“否”),此时,化学反应速率是v正__ v逆(填“大于”、“小于”或“等于”),其原因__ 。
 Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=
Fe(s)+CO2(g) △H>0,其平衡常数表达式为K=(1)温度升高,化学平衡移动后达到新的平衡,平衡常数
(2)1100℃时测得高炉中c(CO2)=0.013mol/L,c(CO)=0.05mol/L,在这种情况下,该反应是否处于化学平衡状态:
更新时间:2020-06-06 10:17:41
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】高炉炼铁中发生的反应有:FeO(s) + CO(g)=Fe(s) + CO2(g) △H < 0
(1)该反应的平衡常数表达式K=_______ 。
(2)已知1100℃时,K=0.263温度升高,平衡常数K_______ (增大,减少或不变)。
(3)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态_______ (填是或否),此时反应速率是v正_______ v逆(填>,<,=)。
(1)该反应的平衡常数表达式K=
(2)已知1100℃时,K=0.263温度升高,平衡常数K
(3)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】300℃ 时,将2mol A和2mol B两种气体混合加入2L密闭容器中,发生反应3A(g)+B(g) 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末反应达到平衡,生成0.8mol D。
,2min末反应达到平衡,生成0.8mol D。
(1)在2min末,A的平衡浓度为
(2)300℃ 时,将该反应容器体积压缩为1L,则A的转化率
(3)判断该反应是否达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变 C.v(A)=v(C) D.混合气体密度不变
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)⇌2NH3(g) △H<0,其平衡常数K与温度T的关系如表:
①试判断K1_____ K2(填写“>”,“=”或“<”)。
②下列各项能说明该反应已达到平衡状态的是__ (填字母)。
a.单位时间内,消耗1molN2的同时生成2molNH3
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
①试判断K1
②下列各项能说明该反应已达到平衡状态的是
a.单位时间内,消耗1molN2的同时生成2molNH3
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素铬( )在溶液中主要以
)在溶液中主要以 (蓝紫色)、
(蓝紫色)、 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体,回答下列问题:
为难溶于水的灰蓝色固体,回答下列问题:
(1)在 溶液中加入过量
溶液中加入过量 溶液,溶液由蓝紫色变为绿色,写出相应的离子方程式:
溶液,溶液由蓝紫色变为绿色,写出相应的离子方程式:___________ 。
(2) 和
和 在溶液中可相互转化:
在溶液中可相互转化: (反应A)。室温下,初始浓度为
(反应A)。室温下,初始浓度为 的
的 溶液中
溶液中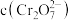 随
随 的变化如图所示(整个过程中溶液体积保持不变)。
的变化如图所示(整个过程中溶液体积保持不变)。
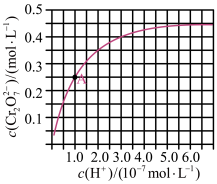
①由图可知,溶液 减小,
减小, 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”)。根据A点数据,计算出反应A的平衡常数为___________ 。
②升高温度,溶液中 的平衡转化率减小;则反应A的
的平衡转化率减小;则反应A的
___________ (填“>”或“<”)0。
③向酸性 溶液中加水,有同学认为溶液中所有离子的浓度都减小,你是否同意并说明理由
溶液中加水,有同学认为溶液中所有离子的浓度都减小,你是否同意并说明理由___________ 。
④向酸性 溶液(橙色)中加入少量氢氧化钠固体(忽略溶液体积的变化),振荡后立即观察到溶液变为黄色,该结果不足以证明
溶液(橙色)中加入少量氢氧化钠固体(忽略溶液体积的变化),振荡后立即观察到溶液变为黄色,该结果不足以证明 浓度的减小使得反应A的平衡逆向移动,理由是:
浓度的减小使得反应A的平衡逆向移动,理由是:___________ 。
(3)在化学分析中采用 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中 为
为___________  。(已知
。(已知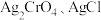 的
的 分别为
分别为 和
和 )
)
(4)向酸性 溶液中加入乙醇(乙醇被氧化为乙酸),溶液变为蓝紫色,反应的离子方程式为
溶液中加入乙醇(乙醇被氧化为乙酸),溶液变为蓝紫色,反应的离子方程式为___________ 。
 )在溶液中主要以
)在溶液中主要以 (蓝紫色)、
(蓝紫色)、 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体,回答下列问题:
为难溶于水的灰蓝色固体,回答下列问题:(1)在
 溶液中加入过量
溶液中加入过量 溶液,溶液由蓝紫色变为绿色,写出相应的离子方程式:
溶液,溶液由蓝紫色变为绿色,写出相应的离子方程式:(2)
 和
和 在溶液中可相互转化:
在溶液中可相互转化: (反应A)。室温下,初始浓度为
(反应A)。室温下,初始浓度为 的
的 溶液中
溶液中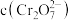 随
随 的变化如图所示(整个过程中溶液体积保持不变)。
的变化如图所示(整个过程中溶液体积保持不变)。
①由图可知,溶液
 减小,
减小, 的平衡转化率
的平衡转化率②升高温度,溶液中
 的平衡转化率减小;则反应A的
的平衡转化率减小;则反应A的
③向酸性
 溶液中加水,有同学认为溶液中所有离子的浓度都减小,你是否同意并说明理由
溶液中加水,有同学认为溶液中所有离子的浓度都减小,你是否同意并说明理由④向酸性
 溶液(橙色)中加入少量氢氧化钠固体(忽略溶液体积的变化),振荡后立即观察到溶液变为黄色,该结果不足以证明
溶液(橙色)中加入少量氢氧化钠固体(忽略溶液体积的变化),振荡后立即观察到溶液变为黄色,该结果不足以证明 浓度的减小使得反应A的平衡逆向移动,理由是:
浓度的减小使得反应A的平衡逆向移动,理由是:(3)在化学分析中采用
 为指示剂,以
为指示剂,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,利用
,利用 与
与 生成砖红色沉淀,指示到达滴定终点。当溶液中
生成砖红色沉淀,指示到达滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中 为
为 。(已知
。(已知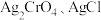 的
的 分别为
分别为 和
和 )
)(4)向酸性
 溶液中加入乙醇(乙醇被氧化为乙酸),溶液变为蓝紫色,反应的离子方程式为
溶液中加入乙醇(乙醇被氧化为乙酸),溶液变为蓝紫色,反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知可逆反应2NO(g) N2(g)+O2(g)。若在某温度下达到平衡时C(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.1mol·L-1 该反应的平衡常数为
N2(g)+O2(g)。若在某温度下达到平衡时C(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.1mol·L-1 该反应的平衡常数为_____________ ,保持温度不变,将容器体积缩小一半,则平衡常数_________ (填增大、减小或不变)。
 N2(g)+O2(g)。若在某温度下达到平衡时C(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.1mol·L-1 该反应的平衡常数为
N2(g)+O2(g)。若在某温度下达到平衡时C(N2)=0.05mol·L-1,C(O2)=0.05mol·L-1,c(NO)=0.1mol·L-1 该反应的平衡常数为
您最近一年使用:0次

 4C(g)+2D(g)。该反应达到化学平衡状态时生成1.6molC,计算此条件下该反应的化学平衡常数和A的平衡转化率
4C(g)+2D(g)。该反应达到化学平衡状态时生成1.6molC,计算此条件下该反应的化学平衡常数和A的平衡转化率

