在2L的密闭容器中,将4molA和2molB混合,在一定条件下发生反应:3A(g)+2B(g) 4C(g)+2D(g)。该反应达到化学平衡状态时生成1.6molC,计算此条件下该反应的化学平衡常数和A的平衡转化率
4C(g)+2D(g)。该反应达到化学平衡状态时生成1.6molC,计算此条件下该反应的化学平衡常数和A的平衡转化率____ 、____ 。
 4C(g)+2D(g)。该反应达到化学平衡状态时生成1.6molC,计算此条件下该反应的化学平衡常数和A的平衡转化率
4C(g)+2D(g)。该反应达到化学平衡状态时生成1.6molC,计算此条件下该反应的化学平衡常数和A的平衡转化率
更新时间:2022-11-26 18:53:10
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)  2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示完成下列问题
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示完成下列问题
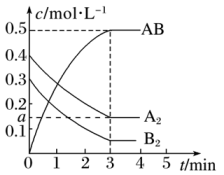
(1)求a=_______
(2)3分钟时反应达到平衡,求平衡时A2的转化率_______
(3)前3分钟AB的速率_______ (保留到小数点后两位)
(4)若向体系中再加入0.2molB2 ,则A2的转化率_______ ,B2的转化率_______ ,(填“增大”“减小”“不变”)
 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示完成下列问题
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示完成下列问题
(1)求a=
(2)3分钟时反应达到平衡,求平衡时A2的转化率
(3)前3分钟AB的速率
(4)若向体系中再加入0.2molB2 ,则A2的转化率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在常压和500℃时把O2和SO2按1∶2体积比混合,如果混合前O2有10mol,平衡时SO3占总体积的91%,求:
(1)平衡时有___________ 摩尔O2转化。
(2)混合气中SO2的体积分数为___________ 。
(3)SO2的转化率___________ 。
(1)平衡时有
(2)混合气中SO2的体积分数为
(3)SO2的转化率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】硫酸是重要的化工材料,二氧化硫与氧气反应生成三氧化硫是工业制硫酸的重要反应之一。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g) 2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。
2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。
①从反应开始到达到平衡,用SO2表示的平均反应速率为________________
②从平衡角度分析采用过量O2的目的是____________ ;
③该反应的平衡常数表达式为K=___________ 。
④已知:K(300℃)>K(350℃),该反应是________ (选填“吸”或“放”)热反应。若反应温度升高,SO2的转化率将_______ (填“增大”、“减小”或“不变”)。
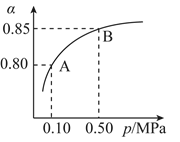
(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示。平衡状态由A变到B时,平衡常数K(A)_______ K(B)(填“>”、“<”或“=”,下同)。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g)
 2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。
2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。①从反应开始到达到平衡,用SO2表示的平均反应速率为
②从平衡角度分析采用过量O2的目的是
③该反应的平衡常数表达式为K=
④已知:K(300℃)>K(350℃),该反应是

(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示。平衡状态由A变到B时,平衡常数K(A)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,发生反应:
气体,发生反应: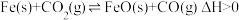 ,
, 的浓度与时间的关系曲线如图所示。回答下列问题:
的浓度与时间的关系曲线如图所示。回答下列问题:
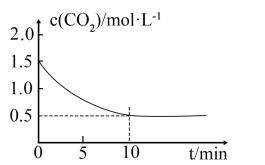
(1)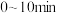 内,用CO表示的化学反应速率为
内,用CO表示的化学反应速率为________________________________________ ,该反应平衡常数的表达式为__________________________________________ ,该条件下反应的平衡常数为______________ ;若铁粉足量,CO2的起始浓度为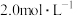 ,则平衡时CO2的浓度为
,则平衡时CO2的浓度为____________ 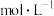 。
。
(2)下列措施能使平衡时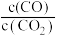 增大的是
增大的是_____________ (填序号)。
A.升高温度 B.增大压强
C.充入一定量的 D.再加入一定量铁粉
D.再加入一定量铁粉
 气体,发生反应:
气体,发生反应: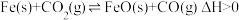 ,
, 的浓度与时间的关系曲线如图所示。回答下列问题:
的浓度与时间的关系曲线如图所示。回答下列问题:
(1)
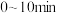 内,用CO表示的化学反应速率为
内,用CO表示的化学反应速率为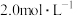 ,则平衡时CO2的浓度为
,则平衡时CO2的浓度为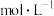 。
。(2)下列措施能使平衡时
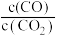 增大的是
增大的是A.升高温度 B.增大压强
C.充入一定量的
 D.再加入一定量铁粉
D.再加入一定量铁粉
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知:H2S(g) H2(g)+
H2(g)+ S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K_______ (填“增大”、“减小”或“不变”)。若985℃时平衡常数K=0.04,则起始浓度c=______ 。

 H2(g)+
H2(g)+ S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】t℃时,在体积为2L的密闭容器中(容积不变)通入3mol A和1mol B,发生反应3A(g)+B(g)  xC(g);经过2min的时间该反应达到平衡状态(假设温度不变),剩余的B的物质的量为0.8mol并测得C的浓度为0.4 mol∙L−1。
xC(g);经过2min的时间该反应达到平衡状态(假设温度不变),剩余的B的物质的量为0.8mol并测得C的浓度为0.4 mol∙L−1。
请回答下列问题:
(1)整个反应过程中,B的平均反应速率为_______
(2)x=_______ ,平衡常数K=_______ 。
(3)如果向该平衡体系中通入少量氮气、增大反应体系的压强,那么化学平衡的移动方向是_______ 。
 xC(g);经过2min的时间该反应达到平衡状态(假设温度不变),剩余的B的物质的量为0.8mol并测得C的浓度为0.4 mol∙L−1。
xC(g);经过2min的时间该反应达到平衡状态(假设温度不变),剩余的B的物质的量为0.8mol并测得C的浓度为0.4 mol∙L−1。请回答下列问题:
(1)整个反应过程中,B的平均反应速率为
(2)x=
(3)如果向该平衡体系中通入少量氮气、增大反应体系的压强,那么化学平衡的移动方向是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应,2NO2(g)(红棕色) N2O4(g)(无色),如图所示。
N2O4(g)(无色),如图所示。
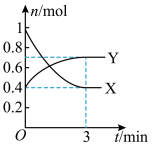
(1)曲线____ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线,
(2)若降低温度,则v(正)____ ,v(逆)____ .(填“加快"或“减慢"或“不变”)
(3)在0到3min中内X的反应速率为____
(4)达到反应限度时X的转化率为____ ,注:物质的转化率=  ×100%
×100%
 N2O4(g)(无色),如图所示。
N2O4(g)(无色),如图所示。
(1)曲线
(2)若降低温度,则v(正)
(3)在0到3min中内X的反应速率为
(4)达到反应限度时X的转化率为
 ×100%
×100%
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某温度下,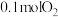 与0.2mol
与0.2mol 在
在 的密闭容器中发生反应:
的密闭容器中发生反应: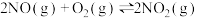 ,其中
,其中 的物质的量随时间变化如下表:
的物质的量随时间变化如下表:
(1)上述反应_______ (填“是”或“不是”)可逆反应,5min时NO的转化率为_______ 。
(2)写出一种加快该反应速率的方法:_______ 。
(3)达到平衡状态时,容器中 的体积分数为
的体积分数为_______ ,2min时氧气的平均反应速率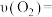
_______ mol∙L−1∙min−1。
(4)下列选项中,能说明该反应已经达到化学平衡状态的有_______ (填字母)。
A.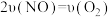 B.
B. 的物质的量不再变化
的物质的量不再变化
C.容器内的颜色不再改变 D.
E.容器内压强不再变化 F.混合气体的密度不再变化
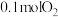 与0.2mol
与0.2mol 在
在 的密闭容器中发生反应:
的密闭容器中发生反应: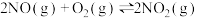 ,其中
,其中 的物质的量随时间变化如下表:
的物质的量随时间变化如下表:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.2 | 0.15 | 0.11 | 0.09 | 0.08 | 0.08 |
(2)写出一种加快该反应速率的方法:
(3)达到平衡状态时,容器中
 的体积分数为
的体积分数为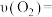
(4)下列选项中,能说明该反应已经达到化学平衡状态的有
A.
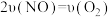 B.
B. 的物质的量不再变化
的物质的量不再变化C.容器内的颜色不再改变 D.

E.容器内压强不再变化 F.混合气体的密度不再变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.
(1)已知CH3OH(g)+ O2(g)
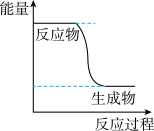
O2(g) CO2(g)+2H2(g)能量变化如图,下列说法正确的是______
CO2(g)+2H2(g)能量变化如图,下列说法正确的是______
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速度v(H2)=__________ ,则CH3OH的转化率为______ 。
(3)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气、KOH(电解质溶液)构成,则下列说法正确的是 ______
(4)写出甲醇燃料电池在酸性条件下负极的反应式为 ______ 。
(1)已知CH3OH(g)+
 O2(g)
O2(g) CO2(g)+2H2(g)能量变化如图,下列说法正确的是______
CO2(g)+2H2(g)能量变化如图,下列说法正确的是______
| A.CH3OH转变成H2的过程是一个吸收能量的过程 |
| B.H2的生成速率与CH3OH的消耗速率之比为1:2 |
| C.化学变化不仅有新物质生成,同时也一定有能量变化 |
| D.1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度 |
(3)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气、KOH(电解质溶液)构成,则下列说法正确的是 ______
| A.电池放电时通入空气的电极为负极 |
| B.电池放电时负极的电极反应式为CH3OH-6e-=CO2↑+2H2O |
| C.电池放电时,电解质溶液的碱性逐渐减弱 |
| D.电池放电时每消耗6.4gCH3OH转移1.2mol电子 |
您最近一年使用:0次



