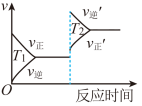
下列叙述中,不能用勒夏特列原理解释的是
| A.高压比常压有利于SO2与O2合成SO3的反应 |
| B.加入催化剂有利于N2与H2合成NH3的反应 |
| C.向橙色K2Cr2O7溶液中加入一定浓度的NaOH溶液后,溶液变为黄色 |
| D.工业制取金属钾Na(1)+KCl(l)⇌NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
更新时间:2020-09-05 16:10:54
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】海洋中的珊瑚虫经如下反应形成石灰石外壳,进而形成珊瑚:Ca2++2
 CaCO3+CO2+H2O。与珊瑚虫共生的藻类会消耗海洋中的CO2,气候变暖,温室效应的加剧干扰了珊瑚虫的生长导致其死亡。下列说法不合理的是
CaCO3+CO2+H2O。与珊瑚虫共生的藻类会消耗海洋中的CO2,气候变暖,温室效应的加剧干扰了珊瑚虫的生长导致其死亡。下列说法不合理的是

 CaCO3+CO2+H2O。与珊瑚虫共生的藻类会消耗海洋中的CO2,气候变暖,温室效应的加剧干扰了珊瑚虫的生长导致其死亡。下列说法不合理的是
CaCO3+CO2+H2O。与珊瑚虫共生的藻类会消耗海洋中的CO2,气候变暖,温室效应的加剧干扰了珊瑚虫的生长导致其死亡。下列说法不合理的是| A.共生藻类消耗CO2,有利于珊瑚的形成 |
| B.温室效应导致海洋中CO2浓度升高,抑制了珊瑚的形成 |
| C.气候变暖,温度升高会增大CO2在海水中的溶解度,抑制了珊瑚的形成 |
| D.与深海地区相比,浅海地区压强较小,有利于珊瑚的形成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关工业生产的叙述中,正确的是
| A.硫酸生产中常采用催化剂提高SO2的转化率 |
| B.合成氨中采用及时分离氨气提高反应速率 |
| C.电镀铜时,溶液中c(Cu2+)基本保持不变 |
| D.用电解熔融氧化镁的方法制取镁 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】一定条件下的反应aA(g)+bB(g) cC(g)+dD(s) ΔH=QkJ·mol−1,反应过程中化学平衡常数(K)与温度,C的百分含量与时间的关系如图所示,以下说法不正确的是
cC(g)+dD(s) ΔH=QkJ·mol−1,反应过程中化学平衡常数(K)与温度,C的百分含量与时间的关系如图所示,以下说法不正确的是
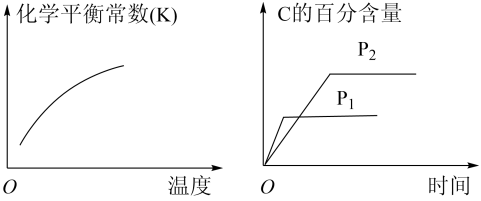
 cC(g)+dD(s) ΔH=QkJ·mol−1,反应过程中化学平衡常数(K)与温度,C的百分含量与时间的关系如图所示,以下说法不正确的是
cC(g)+dD(s) ΔH=QkJ·mol−1,反应过程中化学平衡常数(K)与温度,C的百分含量与时间的关系如图所示,以下说法不正确的是
| A.Q>0 |
| B.a+b<c |
| C.K越大,A的转化率越大 |
| D.达到平衡后,增加少量D,平衡逆向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关合成氨工业的叙述,能够用勒·夏特列原理来解释的是
| A.加入催化剂可以提高单位时间氨的产量 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.500℃高温比室温更有利于合成氨的反应 |
| D.N2和H2按物质的量之比1:2.8混合,更有利于氨的合成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列关于工业生产过程的叙述正确的是( )
| A.联合制碱法中循环使用CO2和NH3,以提高原料利用率 |
| B.硫酸工业中,SO2氧化为SO3时采用常压,因为高压会降低SO2转化率 |
| C.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| D.炼钢是在高温下利用氧化剂把生铁中过多的碳和其他杂质氧化成气体或炉渣除去 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】化学是一门拥有国际通用科学语言的自然科学。下列化学用语使用错误的是


A.向I2的四氯化碳溶液中加入足量KI溶液,下层颜色变浅:I2+I-  |
B.苯酚浊液中加入碳酸钠液液后变澄清:2 + + →2 →2 +CO2↑+H2O +CO2↑+H2O |
| C.如图用原子轨道表示N2中化学键的形成 |
D.向硫酸铜和浓氨水的澄清混合液中加入95%乙醇出现深蓝色沉淀:[Cu(NH3)4]2++ +H2O=[Cu(NH3)4]SO4·H2O↓ +H2O=[Cu(NH3)4]SO4·H2O↓ |
您最近一年使用:0次

 制备无水氯化铝的反应为:
制备无水氯化铝的反应为:
 。下列分析正确的是
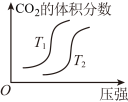
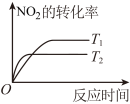
。下列分析正确的是 4CO2(g)+N2(g) ΔH=−1200 kJ∙mol−1,从而转化为无毒气体。温度不同(T2>T1)、其他条件相同时,下列图示变化关系不正确的是
4CO2(g)+N2(g) ΔH=−1200 kJ∙mol−1,从而转化为无毒气体。温度不同(T2>T1)、其他条件相同时,下列图示变化关系不正确的是