下列事实不能用勒夏特列原理解释的是
①溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
②工业合成氨反应N2(g)+3H2(g) 2NH3(g)△H<0,为提高氨的产率,实际生产中采取高温、高压的措施
2NH3(g)△H<0,为提高氨的产率,实际生产中采取高温、高压的措施
③反应2 NO2(g) N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅
N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅
④对于2HI(g) H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
⑤滴入酚酞的氨水加热,冷却后,溶液的颜色变浅或消失
⑥反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
①溴水中有下列平衡Br2+H2O
 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅②工业合成氨反应N2(g)+3H2(g)
 2NH3(g)△H<0,为提高氨的产率,实际生产中采取高温、高压的措施
2NH3(g)△H<0,为提高氨的产率,实际生产中采取高温、高压的措施③反应2 NO2(g)
 N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅
N2O4(g)达平衡后,缩小容器体积可使体系颜色先变深后变浅④对于2HI(g)
 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深⑤滴入酚酞的氨水加热,冷却后,溶液的颜色变浅或消失
⑥反应CO(g)+NO2(g)
 CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深| A.①⑤ | B.②③ | C.②④ | D.③④ |
更新时间:2020-10-29 14:33:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4制备CS2,在2L恒容密闭容器中发生反应 、
、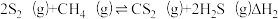 ,一定条件下,平衡时S2的体积分数、CH4的平衡转化率与温度的关系如图所示。下列说法正确的是
,一定条件下,平衡时S2的体积分数、CH4的平衡转化率与温度的关系如图所示。下列说法正确的是

 、
、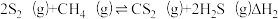 ,一定条件下,平衡时S2的体积分数、CH4的平衡转化率与温度的关系如图所示。下列说法正确的是
,一定条件下,平衡时S2的体积分数、CH4的平衡转化率与温度的关系如图所示。下列说法正确的是
| A.△H1<△H2 |
| B.增大S8(s)的用量,可提高甲烷的平衡转化率 |
C.若容器内只发生反应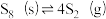 ,平衡后恒温压缩体积,S2(g)的平衡浓度不变 ,平衡后恒温压缩体积,S2(g)的平衡浓度不变 |
D.若起始加入2 molCH4,2min时甲烷转化率为30%,则0~2min内 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】图中曲线分别表示相同温度下,压强为P1、P2条件下发生可逆反应:mX(g)+nY(g) 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
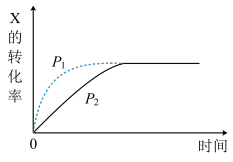
 2Z(g)+W(s)的过程。下列说法不正确的是( )
2Z(g)+W(s)的过程。下列说法不正确的是( )
| A.P1>P2 | B.m+n=2 |
| C.m+n=3 | D.P1、P2下平衡常数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实、现象或应用中,不能用勒夏特列原理解释的是
| A.CO中毒者应及时移至空气流通处,必要时应放入高压氧舱 |
B.工业上用钠制备钾: |
| C.工业上采用高温煅烧石灰石 |
D.工业上生产硫酸过程中,通入过量空气以提高 的转化率 的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不能用勒夏特列原理来解释的是
| A.工业合成氨在较高的压强下进行 |
| B.煤气中毒者转入高压氧舱缓解中毒状况 |
C. 的盐酸加水稀释10倍后 的盐酸加水稀释10倍后 |
| D.实验室制备氯气时,用排饱和氯化钠溶液收集氯气 |
您最近一年使用:0次



