I.Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_________ 。
(2)Li及其周期表中相邻元素的第一电离能(I1),I1(Li)> I1(Na),原因是_________ 。
Ⅱ.氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
(3)NH3BH3分子中,N—B化学键称为________ 键,其电子对由_______ 提供。氨硼烷在催化剂作用下水解释放氢气: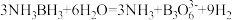 ,
,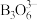 的结构如图所示:
的结构如图所示:
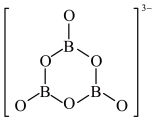
在该反应中,B原子的杂化轨道类型由________ 变为__________ 。
(4)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是__________ 。
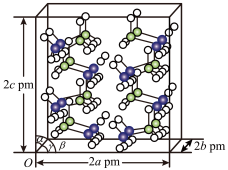
(5)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。氨硼烷晶体的密度ρ=______ g·cm−3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Li及其周期表中相邻元素的第一电离能(I1),I1(Li)> I1(Na),原因是
Ⅱ.氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
(3)NH3BH3分子中,N—B化学键称为
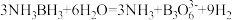 ,
,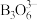 的结构如图所示:
的结构如图所示:
在该反应中,B原子的杂化轨道类型由
(4)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
(5)研究发现,氨硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。氨硼烷晶体的密度ρ=

更新时间:2020-11-02 17:33:27
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe2+的价电子排布式为_______ 。
(2)氮气、氨气、肼(N2H4)中氮原子孤电子对数之比为_______ ,氨分子的空间构型是______
(3)丙酮(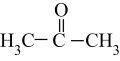 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是_____ ,1 mol 丙酮分子中含有σ键的数目为______ 。
(4)C、N、O三种元素的电负性由小到大的顺序为______ 。
(5)乙醇的沸点高于丙酮,这是因为_____ 。
(6)CN-与N2是等电子体,CN-的电子式为______ 。
(7)某FexNy的晶胞如图−1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示,其中更稳定的Cu替代型产物的化学式为___ ,若晶胞参数为a pm,则该晶胞的密度为____ g/cm3。

(1)Fe2+的价电子排布式为
(2)氮气、氨气、肼(N2H4)中氮原子孤电子对数之比为
(3)丙酮(
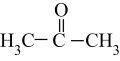 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(4)C、N、O三种元素的电负性由小到大的顺序为
(5)乙醇的沸点高于丙酮,这是因为
(6)CN-与N2是等电子体,CN-的电子式为
(7)某FexNy的晶胞如图−1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为__________________ 。
(2)SO42ˉ的立体构型是_____________ ,其中S原子的杂化轨道类型是___________ 。
(3)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子外围电子排布式为_____ 。一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为______ ,该晶体中,原子之间的作用力是_______ 。
(4)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如下图),该晶体储氢后的化学式应为______ ;假设在另一条件下,氢原子可进入到由Cu原子与Au原子构成的八面体空隙中心,该晶体储氢后的化学式为_____ 。(提示:查找四面体、八面体时,需假设Cu原子与Au原子等同;每个四面体、八面体内只填充一个氢原子)
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
(2)SO42ˉ的立体构型是
(3)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子外围电子排布式为
(4)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如下图),该晶体储氢后的化学式应为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铱( )属于铂系金属,铂系金属包括钌(
)属于铂系金属,铂系金属包括钌( )、锇(
)、锇( )、铑(
)、铑( )、铱(
)、铱( )、钯(
)、钯( )、铂(
)、铂( )六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
)六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
回答下列问题:
(1)基态铱原子的价层电子排布式为_____ 。
(2)实验室常用氯化钯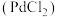 溶液检验
溶液检验 ,发生反应为
,发生反应为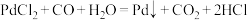 。
。
①在标准状况下,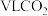 含
含 键数目为
键数目为_____ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
② 分子中
分子中 键类型是
键类型是_____ (填字母)。
A. B.
B. C.
C. D.
D.
(3)实验证明,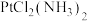 的结构有两种:
的结构有两种: 呈棕黄色,有极性,有抗癌活性,在水中的溶解度为
呈棕黄色,有极性,有抗癌活性,在水中的溶解度为 ,水解后能与草酸
,水解后能与草酸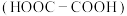 反应生成
反应生成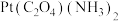 ;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为
;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为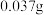 ,水解后不能与草酸反应。
,水解后不能与草酸反应。
①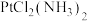 的空间构型是
的空间构型是_____ (填“四面体形”或“平面四边形”)。
②画出A的结构图示:_____ 。
③ 中碳原子的杂化类型是
中碳原子的杂化类型是_____ ,提供孤电子对的原子是_____ (填元素符号)。
 )属于铂系金属,铂系金属包括钌(
)属于铂系金属,铂系金属包括钌( )、锇(
)、锇( )、铑(
)、铑( )、铱(
)、铱( )、钯(
)、钯( )、铂(
)、铂( )六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
)六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。 |  |
 |  |
 |  |
(1)基态铱原子的价层电子排布式为
(2)实验室常用氯化钯
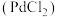 溶液检验
溶液检验 ,发生反应为
,发生反应为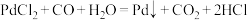 。
。①在标准状况下,
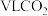 含
含 键数目为
键数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②
 分子中
分子中 键类型是
键类型是A.
 B.
B. C.
C. D.
D.
(3)实验证明,
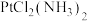 的结构有两种:
的结构有两种: 呈棕黄色,有极性,有抗癌活性,在水中的溶解度为
呈棕黄色,有极性,有抗癌活性,在水中的溶解度为 ,水解后能与草酸
,水解后能与草酸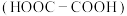 反应生成
反应生成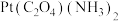 ;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为
;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为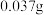 ,水解后不能与草酸反应。
,水解后不能与草酸反应。①
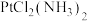 的空间构型是
的空间构型是②画出A的结构图示:
③
 中碳原子的杂化类型是
中碳原子的杂化类型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】研究元素周期表右上角区域元素,有利于研发新型绿色农药,如 等。
等。
 和
和 的混合气体经光解作用可生成一种新分子
的混合气体经光解作用可生成一种新分子
①
 中S
中S 键。
键。②下列分子中属于非极性分子的是
a. b.
b. c.
c. d.
d.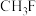 e.
e.
 、
、 中沸点较高的是
中沸点较高的是(3)下列物质变化,只与范德华力有关的是
A.干冰熔化 B.乙酸汽化 C.乙醇与HCHO混溶
D. 溶于水 E.碘溶于四氯化碳
溶于水 E.碘溶于四氯化碳
 。推测酸性:
。推测酸性:
 。
。(5)最近我国某科研团队用磷化钴纳米片催化合成氧化偶氯、偶氯、胺类芳香化合物,反应原理为
 。
。P与N属于同主族元素,但是 不能稳定存在的原因
不能稳定存在的原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】前四周期元素A、B、C、D、E、F原子序数依次增大,其相关性质如表所示:
回答下列问题:
(1)C元素基态原子核外电子有___________ 种空间运动状态。画出E元素基态原子的价电子排布图:___________ 。
(2)C和D可形成一种既含有共价键又含有离子键的化合物,该化合物的电子式为___________ 。
(3)A、B、C、D四种元素电负性由大到小的顺序为___________ (用元素符号表示)。
(4)写出一个化学方程式证明元素C和E的非金属性强弱:___________ 。
(5)检验某物质或某溶液中是否含D元素的方法是___________ ,该方法的原理是___________ 。
| A | 基态原子核外有2个未成对电子 |
| B | 同周期中,占据的能级数最多,但所用的电子数最少 |
| C | 基态原子核外有2个未成对电子 |
| D | 同周期元素中,原子半径最大(不考虑稀有气体) |
| E | C、E、F三种元素的价电子数相同 |
| F | 同周期元素中,基态原子的未成对电子数最多 |
(1)C元素基态原子核外电子有
(2)C和D可形成一种既含有共价键又含有离子键的化合物,该化合物的电子式为
(3)A、B、C、D四种元素电负性由大到小的顺序为
(4)写出一个化学方程式证明元素C和E的非金属性强弱:
(5)检验某物质或某溶液中是否含D元素的方法是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】N元素能形成多种化合物,它们之间可以发生相互转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与O的电负性较小的是_____ 。
(2)N的基态原子的电子排布中,有____ 个运动状态不同的未成对电子。
(3)HNO2原子的杂化类型是____ 。
(4)NO 与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:
与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:____ 。
(1)N与O的电负性较小的是
(2)N的基态原子的电子排布中,有
(3)HNO2原子的杂化类型是
(4)NO
 与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:
与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】(1)基态镍原子的价电子排布式___________ ;铁的基态原子核外未成对电子数为___________ 个。
(2)丁二酮肟(分子式为C4H8N2O2)所含的碳、氮、氧三种元素中第一电离能最大的是___________ (填元素符号)。在稀氨水介质中,Ni2+与丁二酮肟(分子式为C4H8N2O2)反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为___________  。
。

(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4.1个Fe(CO)5分子中含有σ键数目为__ ;已知Ni(CO)4分子为正四面体构型,下列溶剂能够溶解Ni(CO)4的是___ (填写字母)。
A.四氯化碳 B.苯 C.水 D.液氨
(4)经查氯化亚铁的熔点为674℃,沸点为1023℃;而氯化铁的熔点为306℃,沸点为315℃。从二者熔沸点差异较大可以初步判断:氯化亚铁为____ 晶体,三氯化铁为________ 晶体。
(5)氮化硼晶体有多种结构,其中立方氮化硼具有金刚石的结构(如图)。若晶胞边长为anm,晶胞中N原子位于B原子所形成的正四面体的体心,这种氮化硼晶体的密度为___________ g/cm3.(用含有a和NA的代数式表示)

(2)丁二酮肟(分子式为C4H8N2O2)所含的碳、氮、氧三种元素中第一电离能最大的是
 。
。
(3)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4.1个Fe(CO)5分子中含有σ键数目为
A.四氯化碳 B.苯 C.水 D.液氨
(4)经查氯化亚铁的熔点为674℃,沸点为1023℃;而氯化铁的熔点为306℃,沸点为315℃。从二者熔沸点差异较大可以初步判断:氯化亚铁为
(5)氮化硼晶体有多种结构,其中立方氮化硼具有金刚石的结构(如图)。若晶胞边长为anm,晶胞中N原子位于B原子所形成的正四面体的体心,这种氮化硼晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氮、磷、锌元素的单质和化合物在农药生产及工业制造等领域用途非常广泛。回答下列问题:
(1)基态P原子中,电子占据的最高能层具有的原子轨道数为_______ ,基态Zn原子的价电子排布式是________ 。
(2)2019年德国专家从硫酸铵中检测出一种组成为N4H4(SO4)2的物质,该物质在水中以 和
和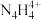 两种离子的形式存在。
两种离子的形式存在。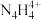 易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。
易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。
①N、O、S三元素第一电离能从小到大的顺序是_________ 。
②1个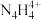 中含有
中含有_______ 个 键。
键。
(3)白磷在空气中缓慢氧化生成P4O6,其结构如图所示。P4O6中氧原子的杂化轨道类型为_______ ,每个P4O6分子中含孤电子对的数目为________ 。

(4)科学家合成了一种阳离子为“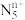 ”,其结构是对称的,5个N排成“V”形,含2个氮氮三键,且每个N原子都达到8电子稳定结构;此后又合成了一种含有“
”,其结构是对称的,5个N排成“V”形,含2个氮氮三键,且每个N原子都达到8电子稳定结构;此后又合成了一种含有“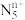 ”化学式为“N8”的离子晶体。“
”化学式为“N8”的离子晶体。“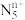 ”中位于角顶点上的N原子的杂化轨道类型是
”中位于角顶点上的N原子的杂化轨道类型是_______ ,“N8”中阴离子的空间构型为________ 。
(1)基态P原子中,电子占据的最高能层具有的原子轨道数为
(2)2019年德国专家从硫酸铵中检测出一种组成为N4H4(SO4)2的物质,该物质在水中以
 和
和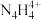 两种离子的形式存在。
两种离子的形式存在。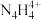 易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。
易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被植物吸收。①N、O、S三元素第一电离能从小到大的顺序是
②1个
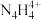 中含有
中含有 键。
键。(3)白磷在空气中缓慢氧化生成P4O6,其结构如图所示。P4O6中氧原子的杂化轨道类型为

(4)科学家合成了一种阳离子为“
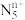 ”,其结构是对称的,5个N排成“V”形,含2个氮氮三键,且每个N原子都达到8电子稳定结构;此后又合成了一种含有“
”,其结构是对称的,5个N排成“V”形,含2个氮氮三键,且每个N原子都达到8电子稳定结构;此后又合成了一种含有“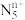 ”化学式为“N8”的离子晶体。“
”化学式为“N8”的离子晶体。“ ”中位于角顶点上的N原子的杂化轨道类型是
”中位于角顶点上的N原子的杂化轨道类型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】人们对含硼(元素符号为“B”)物质结构的研究,极大地推动了结构化学的发展。回答下列问题:
(1)基态B原子价层电子的电子排布式为_____ ,核外电子占据最高能层的符号是____ ,占据该能层未成对电子的电子云轮廓图形状为____ 。
(2)1923年化学家Lewis提出了酸碱电子理论。酸碱电子理论认为:凡是可以接受电子对的物质称为酸,凡是可以给出电子对的物质称为碱。已知BF3与F-反应可生成BF4-,则该反应中BF3属于____ (填“酸”或“碱”),原因是____ 。
(3)NaBH4是有机合成中常用的还原剂,NaBH4中的阴离子空间构型是_____ ,中心原子的杂化形式为____ ,NaBH4中存在____ (填标号)
a.离子键 b.金属键 c.σ键 d.π键 e.氢键
(4)请比较第一电离能:IB____ IBe(填“>”或“<”),原因是_______ 。
(5)六方氮化硼的结构与石墨类似,B—N共价单键的键长理论值为158pm,而六方氮化硼层内B、N原子间距的实测值为145 pm,造成这一差值的原因是____ 。高温高压下,六方氮化硼可转化为立方氮化硼,立方氮化硼的结构与金刚石类似,已知晶胞参数中边长为a=362 pm,则立方氮化硼的密度是____ g/cm3。

(1)基态B原子价层电子的电子排布式为
(2)1923年化学家Lewis提出了酸碱电子理论。酸碱电子理论认为:凡是可以接受电子对的物质称为酸,凡是可以给出电子对的物质称为碱。已知BF3与F-反应可生成BF4-,则该反应中BF3属于
(3)NaBH4是有机合成中常用的还原剂,NaBH4中的阴离子空间构型是
a.离子键 b.金属键 c.σ键 d.π键 e.氢键
(4)请比较第一电离能:IB
(5)六方氮化硼的结构与石墨类似,B—N共价单键的键长理论值为158pm,而六方氮化硼层内B、N原子间距的实测值为145 pm,造成这一差值的原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】第四周期第VIII族元素在古代和现代被广泛应用。回答下列问题:
(1)据古文献记载:宣德时期青花瓷使用的颜料“苏勃泥青”是从一种进口钴毒矿[主要成分:(FeCo)xAsS]中提取出来的。
①基态Co原子的价电子排布式为_______ 。
②无水CoCl2的熔点是735℃,沸点1049℃,CoCl2属于_______ 晶体;砷酸根离子(AsO )的空间构型为
)的空间构型为_______ 。
(2)下列状态的铁中,电离最外层一个电子所需能量最大的是_______ 。
A.[Ar]3d64s1 B.[Ar]3d64s2 C.[Ar]3d74s1 D.[Ar]3d6
(3)鉴定Ni2+的特征反应是将丁二酮肟加入Ni2+盐溶液中,生成鲜红色的螯合物M,M结构如图所示:

①组成M的五种元素中,电负性最大的是_______ 。
②图中各微粒间不存在的作用力有_______ (填标号)。
a.配位键 b.极性键 c.非极性键 d.π键 e.离子键 f.氢键
(4)K3[Fe(CN)6](铁氰化钾)可用于检验铁陨石中铁元素价态。与配体CN-原子总数相等的等电子体是_______ ,1mol[Fe(CN)6]3-中含有的σ键数目为_______ (设NA为阿伏加德罗常数的值)。
(5)一种铁氮化合物具有高磁导率,可用于制电子元件。该化合物密度为ρg·cm-3,其结构如图所示:

①该铁氮化合物的化学式为_______ 。
②计算Fe(II)构成正八面体的体积为_______ cm3。
(1)据古文献记载:宣德时期青花瓷使用的颜料“苏勃泥青”是从一种进口钴毒矿[主要成分:(FeCo)xAsS]中提取出来的。
①基态Co原子的价电子排布式为
②无水CoCl2的熔点是735℃,沸点1049℃,CoCl2属于
 )的空间构型为
)的空间构型为(2)下列状态的铁中,电离最外层一个电子所需能量最大的是
A.[Ar]3d64s1 B.[Ar]3d64s2 C.[Ar]3d74s1 D.[Ar]3d6
(3)鉴定Ni2+的特征反应是将丁二酮肟加入Ni2+盐溶液中,生成鲜红色的螯合物M,M结构如图所示:

①组成M的五种元素中,电负性最大的是
②图中各微粒间不存在的作用力有
a.配位键 b.极性键 c.非极性键 d.π键 e.离子键 f.氢键
(4)K3[Fe(CN)6](铁氰化钾)可用于检验铁陨石中铁元素价态。与配体CN-原子总数相等的等电子体是
(5)一种铁氮化合物具有高磁导率,可用于制电子元件。该化合物密度为ρg·cm-3,其结构如图所示:

①该铁氮化合物的化学式为
②计算Fe(II)构成正八面体的体积为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮、磷、氟是组成化合物的重要元素。请回答下列问题:
(1)基态磷原子的核外价电子排布图为_______ 。
(2)N、P、F三种元素的电负性由大到小的顺序为______ 。
(3)PF3分子的空间构型为______ 。
(4)N与F可形成化合物N2F2,下列有关N2F2的说法正确的是______ (填字母)。
a. 分子中氮原子的杂化轨道类型为sp2杂化
b. 其结构式为F-N=N-F
c. 其分子有两种不同的空间构型
d. 1 mol N2F2含有的σ键的数目为4NA(NA表示阿伏加 德罗常数的值)
(5)含氮元素的重要配离子[Cu(NH3)4]2+的结构示意图可表示为_______ 。
(6)农药中通常含有磷元素,AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃,其晶胞结构如图所示。
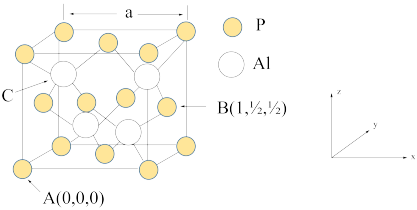
①磷化铝的晶体类型为_______ 。
②A、B点的原子坐标如图所示,则C点的原子坐标为______ 。
③磷化铝的晶胞参数a=546.35 pm(1 pm=10-12m),其密度为_____ g/cm3。(列出计算式即可,用NA表示阿伏加 德罗常数的值)
(1)基态磷原子的核外价电子排布图为
(2)N、P、F三种元素的电负性由大到小的顺序为
(3)PF3分子的空间构型为
(4)N与F可形成化合物N2F2,下列有关N2F2的说法正确的是
a. 分子中氮原子的杂化轨道类型为sp2杂化
b. 其结构式为F-N=N-F
c. 其分子有两种不同的空间构型
d. 1 mol N2F2含有的σ键的数目为4NA(NA表示阿伏加 德罗常数的值)
(5)含氮元素的重要配离子[Cu(NH3)4]2+的结构示意图可表示为
(6)农药中通常含有磷元素,AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃,其晶胞结构如图所示。

①磷化铝的晶体类型为
②A、B点的原子坐标如图所示,则C点的原子坐标为
③磷化铝的晶胞参数a=546.35 pm(1 pm=10-12m),其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】科技强国,我国科学家在诸多领域取得新突破。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂 、
、 及清洗剂
及清洗剂 。
。
①基态F原子核外电子有_____ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填标号)。
A. B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为__________ 。
③氟硼酸铵( )中B的杂化方式为
)中B的杂化方式为__________ , 的空间构型为
的空间构型为__________ 。
(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是__________ (填元素符号),Mn原子的配位数为__________ ,CH3CN中 键与
键与 键数目之比为
键数目之比为__________ 。
(3)超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为__________ (列出计算式即可) 。
。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂
 、
、 及清洗剂
及清洗剂 。
。①基态F原子核外电子有
A.
 B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为
③氟硼酸铵(
 )中B的杂化方式为
)中B的杂化方式为 的空间构型为
的空间构型为(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是
 键与
键与 键数目之比为
键数目之比为(3)超导材料
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为 。
。
您最近一年使用:0次



