下列事实不能用勒夏特列原理解释的是
| A.新制的氯水在光照条件下颜色变浅 |
| B.打开可乐瓶盖后看到有大量气泡逸出 |
| C.H2、I2、HI平衡时的混合气体加压后颜色变深 |
| D.工业上用氮气、氢气合成氨气的过程中,通过加压将氨气液化以增大转化率 |
更新时间:2020-11-03 08:43:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如图。
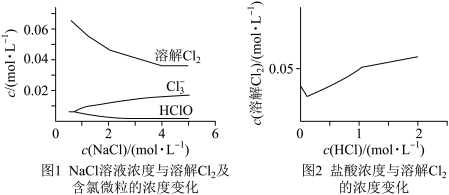
下列说法正确的是

下列说法正确的是
| A.由图1可知,Cl-的存在对Cl2的溶解只起到抑制作用 |
B.随NaCl溶液浓度增大,Cl2+H2O H++C1-+HC1O平衡正移,Cl2溶解度减小 H++C1-+HC1O平衡正移,Cl2溶解度减小 |
C.随盐酸浓度增加,Cl2与H2O的反应被抑制,生成 为主要反应从而促进Cl2溶解 为主要反应从而促进Cl2溶解 |
| D.由图2变化趋势可推测氯气在稀硫酸中溶解度大于在水中的溶解度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在373K时,把0.1mol 气体通入体积为1L的真空密闭容器中,立即出现红棕色。反应进行到60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法错误的是
气体通入体积为1L的真空密闭容器中,立即出现红棕色。反应进行到60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法错误的是
 气体通入体积为1L的真空密闭容器中,立即出现红棕色。反应进行到60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法错误的是
气体通入体积为1L的真空密闭容器中,立即出现红棕色。反应进行到60s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法错误的是| A.压缩容器,颜色加深 |
B.在平衡时体系内含 0.04mol 0.04mol |
C.以 浓度变化表示的平均反应速率为0.002 浓度变化表示的平均反应速率为0.002 |
D.平衡时,如果再充入一定量 ,则可提高 ,则可提高 的转化率 的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1 mol H2O(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
Ⅰ.

Ⅱ.

下列说法正确的是
Ⅰ.


Ⅱ.


下列说法正确的是
| A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动 |
| B.混合气体的密度保持不变时,说明反应体系已达到平衡 |
C.平衡时H2的体积分数可能大于 |
| D.将炭块粉碎,可以使Ⅰ平衡右移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CO和H2合成乙醇发生如下反应:
反应Ⅰ:2CO(g)+4H2(g)=CH3CH2OH(g)+H2O(g) ΔH1= −128.8 kJ·mol-1
反应Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2= −41.8 kJ·mol-1
向一恒容密闭容器中投入一定量的CO和H2发生上述反应,CO的平衡转化率与温度、投料比α[α = ]的关系如图所示。
]的关系如图所示。
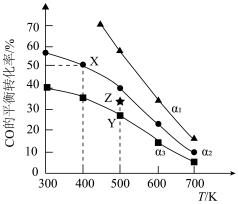
下列有关说法正确的是
反应Ⅰ:2CO(g)+4H2(g)=CH3CH2OH(g)+H2O(g) ΔH1= −128.8 kJ·mol-1
反应Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2= −41.8 kJ·mol-1
向一恒容密闭容器中投入一定量的CO和H2发生上述反应,CO的平衡转化率与温度、投料比α[α =
 ]的关系如图所示。
]的关系如图所示。
下列有关说法正确的是
| A.α1<α2 |
| B.在400 K、α2=2时,反应Ⅰ的平衡常数K=0.25 |
| C.在500 K、投料比为α3条件下,增大压强可使CO的平衡转化率从Y点到Z点 |
| D.为同时提高CO的平衡转化率和CH3CH2OH的产率可采用的反应条件为低温、低压 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.红棕色的NO2加压后颜色先变深后变浅 | B.温度过高对合成氨不利 |
| C.钢铁在潮湿的空气中容易生锈 | D.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实中,能用勒夏特列原理解释的是
A.对CO(g)+NO2(g) CO2(g) + NO(g)平衡体系增大压强可使顔色变深 CO2(g) + NO(g)平衡体系增大压强可使顔色变深 |
B.对2SO2+O2 2SO3 △H<0的反应,使用催化剂可加快反应的速率 2SO3 △H<0的反应,使用催化剂可加快反应的速率 |
| C.实验室可用浓氨水和氢氧化钠固体快速制取氨气 |
D.N2(g)+3H2(g) 2NH3(g) △H<0,500℃左右比室温更有利于合成NH3 2NH3(g) △H<0,500℃左右比室温更有利于合成NH3 |
您最近一年使用:0次

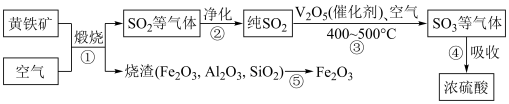
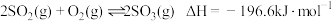
 的催化氧化反应
的催化氧化反应

