某学习小组使用氧化还原反应滴定法测定市售过氧化氢的含量。
I.实验原理:MnO +H2O2+H+=Mn2++H2O+O2↑(未配平)。
+H2O2+H+=Mn2++H2O+O2↑(未配平)。
II.实验步骤
(1)移取10.00mL过氧化氢溶液至250mL___ (填仪器名称)中,加水稀释至刻度,摇匀。
(2)移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
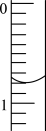
(3)读取盛有0.10mol·L-1酸性高锰酸钾标准溶液的酸式滴定管的初始读数。液面位置如图所示,则此时的读数为___ mL。
(4)滴定。本实验是否需要选定指示剂___ (填“是”或“否”),当___ 时,停止滴定,并记录酸性高锰酸钾标准溶液的最终读数。重复滴定3次。
III.实验记录
IV.数据处理与讨论
(5)某学习小组在处理数据时计算得:平均消耗的溶液的体积V=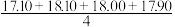 mL。请指出他们计算的不合理之处:
mL。请指出他们计算的不合理之处:___ 。
若数据处理合理,可得过氧化氢的浓度为___ mol·L-1。
(6)在本实验的滴定过程中,若滴定前尖嘴中有气泡,滴定后消失,则测定结果___ (“偏高”“偏低”或“不变”)。
I.实验原理:MnO
 +H2O2+H+=Mn2++H2O+O2↑(未配平)。
+H2O2+H+=Mn2++H2O+O2↑(未配平)。II.实验步骤
(1)移取10.00mL过氧化氢溶液至250mL
(2)移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(3)读取盛有0.10mol·L-1酸性高锰酸钾标准溶液的酸式滴定管的初始读数。液面位置如图所示,则此时的读数为

(4)滴定。本实验是否需要选定指示剂
III.实验记录
| 滴定次数 | 1 | 2 | 3 | 4 |
 (样品的体积)/mL (样品的体积)/mL | 25.00 | 25.00 | 25.00 | 25.00 |
 (KMnO (KMnO )/mL )/mL | 17.10 | 18.10 | 18.00 | 17.90 |
(5)某学习小组在处理数据时计算得:平均消耗的溶液的体积V=
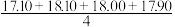 mL。请指出他们计算的不合理之处:
mL。请指出他们计算的不合理之处:若数据处理合理,可得过氧化氢的浓度为
(6)在本实验的滴定过程中,若滴定前尖嘴中有气泡,滴定后消失,则测定结果
更新时间:2020-11-06 08:46:02
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料: Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)反应釜中发生的反应是:2FeTiO3 + 7Cl2 + 6C 2X + 2TiCl4 + 6CO,X的化学式是
2X + 2TiCl4 + 6CO,X的化学式是___________ 。
(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的___________ 不同。
(4)写出合成器中反应的化学方程式___________ ,该反应___________ (填“是”或“不是”)氧化还原反应。
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ 。由金属钛的性质可知,除去这种杂质可以用___________ 。
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是___________ 。
资料: Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)反应釜中发生的反应是:2FeTiO3 + 7Cl2 + 6C
 2X + 2TiCl4 + 6CO,X的化学式是
2X + 2TiCl4 + 6CO,X的化学式是(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的
(4)写出合成器中反应的化学方程式
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】阅读下面科普信息,回答问题:
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有____ 性。下列不能实现上述转化的物质是____
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有____ 性。
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了____ 和____ 性。
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】海洋资源的利用具有广阔前景。回答下列问题:
(1)海带灰中富含以 形式存在的碘元素。从海带中提取
形式存在的碘元素。从海带中提取 的过程如图所示:
的过程如图所示:

①灼烧海带时不需用到下列仪器中的_______ (填字母)。
a.漏斗 b.酒精灯 c.坩埚 d.泥三角
②向滤液中加入稀硫酸和 溶液进行反应,写出该反应的离子方程式
溶液进行反应,写出该反应的离子方程式_______ 。
(2)如图是从海水中提取镁的简单流程。

①操作A的名称是_______ 。
②由无水 制取Mg的化学方程式为
制取Mg的化学方程式为_______ 。
(3)从海水中提取溴的方法为吹出法,主要流程如下:

①吸收塔中反应的化学方程式为_______ 。
②蒸馏塔中控制温度不超过100℃,原因是_______ 。
③经该方法处理后,1 海水最终得到38.4g
海水最终得到38.4g  ,若总提取率为60%,则原海水中溴的浓度是
,若总提取率为60%,则原海水中溴的浓度是_______ mg/L。
(4)聚四氟乙烯气态膜法提取溴的基本原理如图所示:

①经处理后的含 海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为
海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为_______ ,得到富集液后再加酸、精馏可得 。
。
②聚四氟乙烯气态膜法与吹出法相比,优点是_______ (写出一条)。
(1)海带灰中富含以
 形式存在的碘元素。从海带中提取
形式存在的碘元素。从海带中提取 的过程如图所示:
的过程如图所示:
①灼烧海带时不需用到下列仪器中的
a.漏斗 b.酒精灯 c.坩埚 d.泥三角
②向滤液中加入稀硫酸和
 溶液进行反应,写出该反应的离子方程式
溶液进行反应,写出该反应的离子方程式(2)如图是从海水中提取镁的简单流程。

①操作A的名称是
②由无水
 制取Mg的化学方程式为
制取Mg的化学方程式为(3)从海水中提取溴的方法为吹出法,主要流程如下:

①吸收塔中反应的化学方程式为
②蒸馏塔中控制温度不超过100℃,原因是
③经该方法处理后,1
 海水最终得到38.4g
海水最终得到38.4g  ,若总提取率为60%,则原海水中溴的浓度是
,若总提取率为60%,则原海水中溴的浓度是(4)聚四氟乙烯气态膜法提取溴的基本原理如图所示:

①经处理后的含
 海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为
海水透过膜孔与NaOH吸收液发生反应,该反应的离子方程式为 。
。②聚四氟乙烯气态膜法与吹出法相比,优点是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ ,直到因加入一滴盐酸后,溶液由_______ 色变为_______ 色,并_______ 为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______。
(3)滴定开始和结束时,滴定管中的液面如图,则所用盐酸溶液的体积为_______ mL。

(4)某学生根据3次实验分别记录有关数据如表:
依据表中数据列式求得该NaOH溶液的物质的量浓度_______ (保留2位小数)。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |

(4)某学生根据3次实验分别记录有关数据如表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1盐酸的体积/mL | ||
| 滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 25.11 | 25.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 25.31 | 25.09 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某学生用0.1000mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
①移取25.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
②用标准溶液润洗滴定管2-3次
③把盛有标准溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液
④取标准KOH溶液注入______至0刻度以上2-3cm
⑤调节液面至0或0刻度以下,记下读数
⑥把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
(1)正确操作的顺序是(用序号填写)___________
(2)步骤④中的滴定管是:___________ (填“酸式滴定管”或“碱式滴定管”)。
(3)当步骤⑥待测液由___________ 色变为___________ 色,且半分钟内不变化即达到终点,KOH溶液开始时读数及恰好反应时的读数见表。
请计算待测的盐酸的物质的量浓度___________ mol/l(小数点后面保留4位数字)。
(4)由于操作失误,使得上述所测盐酸溶液的浓度偏高的是___________。
①移取25.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
②用标准溶液润洗滴定管2-3次
③把盛有标准溶液的滴定管固定好,调节液面使滴定管尖嘴充满溶液
④取标准KOH溶液注入______至0刻度以上2-3cm
⑤调节液面至0或0刻度以下,记下读数
⑥把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
(1)正确操作的顺序是(用序号填写)
(2)步骤④中的滴定管是:
(3)当步骤⑥待测液由
| 实验编号 | 待测盐酸溶液体积(ml) | 滴定开始读数(ml) | 滴定结束读数(ml) |
| ① | 25.00 | 0.00 | 19.95 |
| ② | 25.00 | 1.10 | 18.30 |
| ③ | 25.00 | 0.20 | 20.25 |
(4)由于操作失误,使得上述所测盐酸溶液的浓度偏高的是___________。
| A.滴定达到终点时,俯视滴定管内液面读数 |
| B.碱式滴定管用蒸馏水洗净后立即取用氢氧化钾溶液进行滴定 |
| C.锥形瓶用蒸馏水洗净后未干燥就装入盐酸待测液 |
| D.滴定时碱式滴定管中氢氧化钾溶液洒落在锥形瓶外 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某学习小组欲测定市售橙汁饮料中维生素C的含量。每100克鲜榨橙汁中含有大约37.5毫克的维生素C。实验室可用碘量法测定橙汁饮料中维生素C的含量,反应的方程式为C6H8O6+I2==C6H6O6+2HI(维生素C化学式为C6H8O6,相对分子质量为176),其实验步骤及相关数据如下:
①标准溶液的稀释:移取浓度为0.0080 mol/L的碘标准溶液25.00 mL于250 mL容量瓶中,定容,摇匀备用。
②移取10.00 mL饮料样品(设密度为1.0 g/cm3)于250 mL锥形瓶中,加入50 mL蒸馏水,2 mL指示剂。
③在滴定管中装入稀释后的标准溶液,滴定至终点,读取并记录相关数据。
④重复测定3次,数据记录如下表。
回答下列问题:
(1)实验中盛装标准溶液应选择______ (填“酸式”或“碱式”)滴定管。
(2)步骤2中加入的指示剂是___________ ,判断滴定达到终点的现象是__________ 。
(3)实验中下列操作可能导致测定结果偏低的是_______ (填标号)。
A.稀释标准溶液定容时俯视刻度线
B.滴定结束时俯视读
C.在锥形瓶中加入样品后放置较长时间才开始滴定
D.滴定管尖嘴部分有气泡,滴定后消失
(4)计算该饮料样品中维生素C含量为________ mg/100 g。该含量______ (填“高于”或“低于”)鲜榨橙汁。
①标准溶液的稀释:移取浓度为0.0080 mol/L的碘标准溶液25.00 mL于250 mL容量瓶中,定容,摇匀备用。
②移取10.00 mL饮料样品(设密度为1.0 g/cm3)于250 mL锥形瓶中,加入50 mL蒸馏水,2 mL指示剂。
③在滴定管中装入稀释后的标准溶液,滴定至终点,读取并记录相关数据。
④重复测定3次,数据记录如下表。
| 第一次 | 第二次 | 第三次 | |
| 滴定前读数/mL | 0.00 | 0.44 | 1.33 |
| 滴定后读数/mL | 30.01 | 30.44 | 31.32 |
回答下列问题:
(1)实验中盛装标准溶液应选择
(2)步骤2中加入的指示剂是
(3)实验中下列操作可能导致测定结果偏低的是
A.稀释标准溶液定容时俯视刻度线
B.滴定结束时俯视读
C.在锥形瓶中加入样品后放置较长时间才开始滴定
D.滴定管尖嘴部分有气泡,滴定后消失
(4)计算该饮料样品中维生素C含量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】I.酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液。
该学生的实验操作如下:
a.用碱式滴定管取稀NaOH 25.00 mL,注入锥形瓶中,加入甲基橙作指示剂。
b.用待测定的溶液润洗碱式滴定管。
c.用蒸馏水洗干净滴定管。
d.取下酸式滴定管用标准HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3 cm,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
e.检查滴定管是否漏水。
f.另取锥形瓶,再重复操作一次。
g.把锥形瓶放在滴定管下,瓶下垫一白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是___________ 。
A.a、c、b、d、e、g、f B.e、c、b、a、g、d、f C.e、c、b、a、d、g、f
②某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:滴定后读数为___________ mL;

③在g操作中如何确定终点___________ 。
II.维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6,维生素C易被空气中的氧气氧化。在新鲜的水果,蔬菜,乳制品中都富含有维生素C,如新鲜橙汁中维生素C的含量为500mg·L-1左右。某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量,下面是测定分析的实验报告:
测定目的:测定XX牌软包装橙汁中维生素C的含量。
测定原理:C6H8O6+I2→C6H6O6+2H++2I-。
实验用品:①实验仪器:酸式滴定管,铁架台,锥形瓶,滴管等。
①试剂:指示剂___________ (填名称),7.5×10-3mol·L-1标准碘液,蒸馏水。
实验步骤:用酸式滴定管向锥形瓶中移入20.00mL待测橙汁……
②数据记录处理,若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量为___________ mg·L-1。
③误差分析:若在实验中存在下列操作,其中会使维生素C的含量偏高的是___________
A.量取待测橙汁的仪器水洗后未润洗
B.锥形瓶水洗后未用待测液润洗
C.滴定前尖嘴部分有一气泡,滴定终点时消失
D.滴定前仰视读数,滴定后俯视读数
该学生的实验操作如下:
a.用碱式滴定管取稀NaOH 25.00 mL,注入锥形瓶中,加入甲基橙作指示剂。
b.用待测定的溶液润洗碱式滴定管。
c.用蒸馏水洗干净滴定管。
d.取下酸式滴定管用标准HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3 cm,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
e.检查滴定管是否漏水。
f.另取锥形瓶,再重复操作一次。
g.把锥形瓶放在滴定管下,瓶下垫一白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是
A.a、c、b、d、e、g、f B.e、c、b、a、g、d、f C.e、c、b、a、d、g、f
②某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:滴定后读数为

③在g操作中如何确定终点
II.维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6,维生素C易被空气中的氧气氧化。在新鲜的水果,蔬菜,乳制品中都富含有维生素C,如新鲜橙汁中维生素C的含量为500mg·L-1左右。某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量,下面是测定分析的实验报告:
测定目的:测定XX牌软包装橙汁中维生素C的含量。
测定原理:C6H8O6+I2→C6H6O6+2H++2I-。
实验用品:①实验仪器:酸式滴定管,铁架台,锥形瓶,滴管等。
①试剂:指示剂
实验步骤:用酸式滴定管向锥形瓶中移入20.00mL待测橙汁……
②数据记录处理,若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量为
③误差分析:若在实验中存在下列操作,其中会使维生素C的含量偏高的是
A.量取待测橙汁的仪器水洗后未润洗
B.锥形瓶水洗后未用待测液润洗
C.滴定前尖嘴部分有一气泡,滴定终点时消失
D.滴定前仰视读数,滴定后俯视读数
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】中和滴定实验操作
(1)滴定前的准备
①滴定管:______ →______ →______ →______ →______ →______ 。
②锥形瓶:______ →______ →______ →______ 。
润洗时:滴定管要用所要盛装的溶液润洗______ 次,锥形瓶禁止用所装溶液润洗;
调液面时:一是调整液面至滴定管______ 处,二是调节活塞(或挤压玻璃球),赶走气泡使滴定管尖嘴部分充满溶液,并使液面处于______ 刻度以下某一刻度处。
记读数时:视线与______ 处相平,记录到0.01位。
加指示剂:加入2~3滴指示剂。
(2)滴定
______ 控制活塞,______ 不断摇动锥形瓶,眼睛注视______ 及滴定流速。
(3)终点判断
等到滴入最后半滴标准NaOH溶液,溶液由______ 变至______ 色且半分钟内不变色,视为滴定终点。
(4)记录刻度读数。
数据处理:c(HCl)=______ 。
(1)滴定前的准备
①滴定管:
②锥形瓶:
润洗时:滴定管要用所要盛装的溶液润洗
调液面时:一是调整液面至滴定管
记读数时:视线与
加指示剂:加入2~3滴指示剂。
(2)滴定
(3)终点判断
等到滴入最后半滴标准NaOH溶液,溶液由
(4)记录刻度读数。
数据处理:c(HCl)=
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】利用滴定法可以测定胆矾中铜的含量,原理如下:
①2Cu2+ + 4I–=2CuI↓+ I2 ②I2 +2 S2O32–=2I–+S4O62–
1.需加入的指示剂为___________ ;需要的物理量除胆矾晶体的质量外,还需要___________ ;判定滴定终点的方法为___________ 。
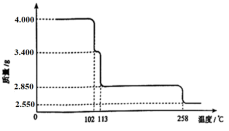
2.将制得的胆矾(CuSO4•5H2O)进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。试确定200℃时固体物质的化学式___________ 。(写出计算过程)
①2Cu2+ + 4I–=2CuI↓+ I2 ②I2 +2 S2O32–=2I–+S4O62–
1.需加入的指示剂为
2.将制得的胆矾(CuSO4•5H2O)进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。试确定200℃时固体物质的化学式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸。其具体实验步骤如下:
(1)取一支碱式滴定管(如图有两只滴定管,你选择哪一只?)_____ (填写对应字母),用少量标准NaOH溶液润洗2~3次水洗后的碱式滴定管,再加入标准的0.100mol/L的NaOH溶液并记录液面刻度读数;

(2)用酸式滴定管精确地放出25.00mL待测盐酸,置于用蒸馏水洗净的锥形瓶中。再加入酚酞试液2滴;
(3)滴定时,边滴边振荡,同时眼睛注视锥形瓶内溶液颜色的变化,当锥形瓶内溶液由
_________________ (填写颜色变化)且半分钟内不褪色时,即达到滴定终点;
(4)记录液面刻度读数。根据滴定管的两次读数得出消耗标准盐酸的体积,再重复测定两次,实验结果记录见下表:
测得未知稀盐酸的物质的量浓度为____________________ (保留小数点后3位)。
(5)如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果稀盐酸浓度的影响是________ (填“偏高”、“偏低”或“无影响”)。
(1)取一支碱式滴定管(如图有两只滴定管,你选择哪一只?)

(2)用酸式滴定管精确地放出25.00mL待测盐酸,置于用蒸馏水洗净的锥形瓶中。再加入酚酞试液2滴;
(3)滴定时,边滴边振荡,同时眼睛注视锥形瓶内溶液颜色的变化,当锥形瓶内溶液由
(4)记录液面刻度读数。根据滴定管的两次读数得出消耗标准盐酸的体积,再重复测定两次,实验结果记录见下表:
| 实验次数 | 起始滴定管读数 | 终点滴定管读数 |
| 1 | 0.00mL | 24.02mL |
| 2 | 0.50mL | 24.46mL |
| 3 | 1.00mL | 25.02mL |
(5)如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果稀盐酸浓度的影响是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.醋酸是一种常见的弱酸,回答下列问题:
(1)向100 mL0.1mol·L− 1的醋酸中加入VmL0.1mol·L−1的NaOH溶液完全反应后,溶液呈中性,则V___________ 100mL(填“>”“<”或“=”)。
(2)25℃时,pH=8的CH3COONa溶液中,水电离产生的OH−浓度c(OH−)水=___________ 。
Ⅱ.某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室的标准NaOH溶液对其进行滴定实验以测定它的准确浓度,操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”以下某一刻度,并记下读数
④经准确操作后,量取VmL待测液注入洁净的锥形瓶中,并加入3滴指示剂溶液
⑤用标准液滴定至终点,记下滴定管液面读数(完全反应时所得溶液的pH大致为9)
(3)以上步骤有错误的是___________ (填序号)。
Ⅲ.完成下列问题
(4)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为___________ mL;

(5)为减小实验误差,该实验最好选用_______ (填石蕊、酚酞或甲基橙)作指示剂;除此外该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为cmol·L−1,三次实验结果记录如下:
从表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是___________ 。
A.实验结束时,仰视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴无气泡,滴定结束尖嘴部分有气泡
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗
D.锥形瓶预先用食用白醋润洗过
(6)据②所得到的数据,写出计算该白醋中醋酸的物质的量浓度的表达式c=___________ mol·L−1(只代数据不必化简)。
(1)向100 mL0.1mol·L− 1的醋酸中加入VmL0.1mol·L−1的NaOH溶液完全反应后,溶液呈中性,则V
(2)25℃时,pH=8的CH3COONa溶液中,水电离产生的OH−浓度c(OH−)水=
Ⅱ.某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室的标准NaOH溶液对其进行滴定实验以测定它的准确浓度,操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”以下某一刻度,并记下读数
④经准确操作后,量取VmL待测液注入洁净的锥形瓶中,并加入3滴指示剂溶液
⑤用标准液滴定至终点,记下滴定管液面读数(完全反应时所得溶液的pH大致为9)
(3)以上步骤有错误的是
Ⅲ.完成下列问题
(4)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为

(5)为减小实验误差,该实验最好选用
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
A.实验结束时,仰视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴无气泡,滴定结束尖嘴部分有气泡
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗
D.锥形瓶预先用食用白醋润洗过
(6)据②所得到的数据,写出计算该白醋中醋酸的物质的量浓度的表达式c=
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某学生用0.1000mol·L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分为以下几步:
A.移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B.用标准NaOH溶液润洗滴定管2~3次
C.把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面至“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)图中属于碱式滴定管的_______ (选填:“甲”、“乙”)。

(2)正确的操作顺序是A、_______ 、_______ 、_______ 、_______ 、F(填字母序号)。
(3)判断到达滴定终点的实验现象是_______ 。
(4)在本实验的滴定过程中,下列操作会使实验结果偏大的是_______ (填写序号)。
a.A步操作之前,先用待测溶液润洗锥形瓶
b.锥形瓶在滴定时剧烈摇动,有少量液体溅出
c.锥形瓶中加入待测盐酸溶液后,再加少量水
d.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
(5)若平行实验三次,记录的数据如下表试计算待测盐酸的物质的量浓度_______ 。
A.移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B.用标准NaOH溶液润洗滴定管2~3次
C.把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面至“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)图中属于碱式滴定管的

(2)正确的操作顺序是A、
(3)判断到达滴定终点的实验现象是
(4)在本实验的滴定过程中,下列操作会使实验结果偏大的是
a.A步操作之前,先用待测溶液润洗锥形瓶
b.锥形瓶在滴定时剧烈摇动,有少量液体溅出
c.锥形瓶中加入待测盐酸溶液后,再加少量水
d.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
(5)若平行实验三次,记录的数据如下表试计算待测盐酸的物质的量浓度
| 滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
| 滴定前读数(/mL) | 滴定后读数(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
您最近一年使用:0次



