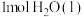工业合成氨原理反应总方程式为N2(g) + 3H2(g)⇌2NH3(g),包含多个基元反应,其反应机理如图所示,已知各物质在催化剂表面吸附放出能量。下列说法错误的是


| A.从充入反应物到A处,物质的能量降低,表示N2、H2在催化剂表面吸附过程放热,物质由气态转化为液态,该过程ΔS>0 |
| B.B→C过程决定了总反应的速率 |
| C.工业合成氨选择温度为700K,主要考虑催化剂在此温度下活性较高 |
| D.由图象可知氨气分解为吸热反应 |
更新时间:2020-11-07 17:25:40
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,气体M、N、P、Q之间存在如下转化关系:①M N+P;②M
N+P;②M N+Q,反应①的速率可表示为v1=k1c(M),反应②的速率可表示为v2=k2c(M)(k1、k2为速率常数),在容积为10L的密闭容器中,反应体系中组分M、P的物质的量随时间的变化如表所示:
N+Q,反应①的速率可表示为v1=k1c(M),反应②的速率可表示为v2=k2c(M)(k1、k2为速率常数),在容积为10L的密闭容器中,反应体系中组分M、P的物质的量随时间的变化如表所示:
下列说法正确的是
 N+P;②M
N+P;②M N+Q,反应①的速率可表示为v1=k1c(M),反应②的速率可表示为v2=k2c(M)(k1、k2为速率常数),在容积为10L的密闭容器中,反应体系中组分M、P的物质的量随时间的变化如表所示:
N+Q,反应①的速率可表示为v1=k1c(M),反应②的速率可表示为v2=k2c(M)(k1、k2为速率常数),在容积为10L的密闭容器中,反应体系中组分M、P的物质的量随时间的变化如表所示:| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| M(mol) | 1.00 | 0.76 | 0.56 | 0.40 | 0.36 | 0.36 | 0.36 |
| P(mol) | 0 | 0.06 | 0.11 | 0.15 | 0.16 | 0.16 | 0.16 |
| A.0~3min时间段内,Q的平均反应速率为0.15mol•L-1•min-1 |
| B.反应①的活化能比反应②的活化能低 |
| C.反应过程中P和Q的浓度之比逐渐减小 |
| D.平衡时M生成Q的转化率为48% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列对有关事实的解释不正确的是
| 编号 | 事实 | 解释 |
| ① | 锌与稀盐酸反应,加入氯化铜固体,速率加快 | 增大了氯离子浓度,反应速率加快 |
| ② | 锌与稀硫酸反应,滴入较多硫酸铜溶液,生成氢气的速率减慢 | 锌置换铜的反应干扰了锌置换氢的反应,致使生成氢气的速率变慢 |
| ③ | 5%的双氧水中加入二氧化锰粉末,分解速率迅速加快 | 降低了反应的焓变,活化分子数增多,有效碰撞增多,速率加快 |
| ④ | 面粉生产车间容易发生爆炸 | 固体表面积大,反应速率加快 |
| A.①④ | B.②③ | C.①②③ | D.①②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】苯乙烷( )与Cl2在光照条件下发生一氯取代,生成两种一取代物的速率如下图I,反应基本历程如下图II。下列说法不正确的是
)与Cl2在光照条件下发生一氯取代,生成两种一取代物的速率如下图I,反应基本历程如下图II。下列说法不正确的是

 )与Cl2在光照条件下发生一氯取代,生成两种一取代物的速率如下图I,反应基本历程如下图II。下列说法不正确的是
)与Cl2在光照条件下发生一氯取代,生成两种一取代物的速率如下图I,反应基本历程如下图II。下列说法不正确的是
| A.反应①②③的△H>0,反应④⑤⑥的△H<0 |
| B.光照条件下,得到等量的(A)和(B)时,生成(B)时需要能量更少 |
C.相同条件下,由苯乙烷分别制备等量的 和 和 的△H不相等 的△H不相等 |
| D.使用恰当的催化剂,可以使反应②的程度减小,反应③的程度增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】科研人员研究了通电条件下 在催化剂
在催化剂 (金)表面生成
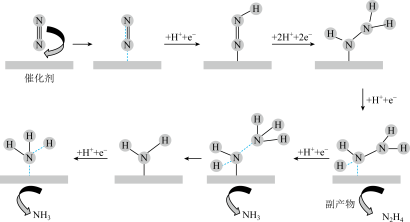
(金)表面生成 的反应,反应机理如图所示,下列说法不正确的是
的反应,反应机理如图所示,下列说法不正确的是
 在催化剂
在催化剂 (金)表面生成
(金)表面生成 的反应,反应机理如图所示,下列说法不正确的是
的反应,反应机理如图所示,下列说法不正确的是
| A.上述转化过程中涉及非极性键的断裂和极性键的生成 |
B.生成 的总电极反应式: 的总电极反应式: |
C.使用 作催化剂可以降低反应的活化能,从而提高化学反应速率 作催化剂可以降低反应的活化能,从而提高化学反应速率 |
D.当 在电解池的阴极发生反应时,可得到 在电解池的阴极发生反应时,可得到 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列变化的熵变大于零的是( )
| A.H2O(l)→H2O(g) | B.CO2(g)→CO2(s) |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O | D.NH3(g)+HCl(g)=NH4Cl(s) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将CO2转化为燃料甲醇是实现碳中和的途径之一、在恒温恒容密闭容器中进行反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ∆H,下列有关说法正确的是
CH3OH(g)+H2O(g) ∆H,下列有关说法正确的是
 CH3OH(g)+H2O(g) ∆H,下列有关说法正确的是
CH3OH(g)+H2O(g) ∆H,下列有关说法正确的是| A.若升高温度,反应逆向进行,则∆H<0 |
| B.正反应为熵增过程,∆S>0 |
| C.若混合气体的密度不随时间变化,可说明反应达到平衡 |
| D.加入催化剂,可提高CO2的平衡转化率 |
您最近一年使用:0次

 催化剂
催化剂
 和
和 合成甲醇,可以减少
合成甲醇,可以减少
 密闭容器中通入
密闭容器中通入 和
和 ,选择合适的催化剂反应,甲醇的选择率(生成甲醇的
,选择合适的催化剂反应,甲醇的选择率(生成甲醇的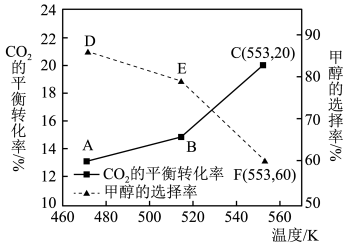
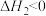
 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数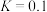
 的体积分数
的体积分数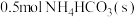 和
和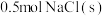 组成的混合物
组成的混合物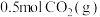 和
和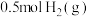 组成的混合物
组成的混合物