完成下列与水解有关的问题:
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是________ (填序号)。
A.甲学生:在醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是吸热的
B.乙学生:将硝酸铵晶体溶于水,水温下降,说明硝酸铵水解是吸热的
C.丙学生:在盐酸中加入同温度的氨水,混合液的温度下降,说明盐类水解是吸热的
D.丁学生:在醋酸钠溶液中加入醋酸钠晶体,溶液温度下降,说明盐类水解是吸热的
(2)现有 的纯碱溶液试用pH试纸测定溶液的pH,其正确的操作是
的纯碱溶液试用pH试纸测定溶液的pH,其正确的操作是_____________ ;纯碱溶液呈碱性的原因是________________ (用离子方程式表示)。
(3)在纯碱溶液中滴入酚酞试液,溶液变红色,若在该溶液中再滴入过量的 溶液,所观察到的现象是
溶液,所观察到的现象是________________ ;其原因是________________ 。
(4)向纯碱溶液中加入少量氯化铁溶液,观察到的现象是________________ ;原因是________________ 。
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是
A.甲学生:在醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是吸热的
B.乙学生:将硝酸铵晶体溶于水,水温下降,说明硝酸铵水解是吸热的
C.丙学生:在盐酸中加入同温度的氨水,混合液的温度下降,说明盐类水解是吸热的
D.丁学生:在醋酸钠溶液中加入醋酸钠晶体,溶液温度下降,说明盐类水解是吸热的
(2)现有
 的纯碱溶液试用pH试纸测定溶液的pH,其正确的操作是
的纯碱溶液试用pH试纸测定溶液的pH,其正确的操作是(3)在纯碱溶液中滴入酚酞试液,溶液变红色,若在该溶液中再滴入过量的
 溶液,所观察到的现象是
溶液,所观察到的现象是(4)向纯碱溶液中加入少量氯化铁溶液,观察到的现象是
19-20高二·全国·课时练习 查看更多[2]
鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时3 水解平衡的移动和水解原理的利用(已下线)3.3.2 影响盐类水解的主要因素(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
更新时间:2020-10-11 17:06:26
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】节假日双休日,去野炊实为一大快事。然而,在野炊的情趣之中,如果遇到下面一些问题,你该如何处理?
(1)对野炊有经验的人会告诉你,餐具最好是导热性好,不易破碎的材料制成,你准备带的餐具是用______ (填字母)制成的;
A.金属 B.陶瓷 C.无所谓
(2)野炊食谱如下:主食:馒头 配菜:红烧肉、豆腐汤、牛肉干。主食和配菜中主要含蛋白质、________ 、油脂、无机盐和水等营养素。
(3)用高锰酸钾制氧气时,收集到的氧气略显红色,可能的错误操作是_____________ 。
(4)用水将pH试纸润湿后,再测某稀盐酸的pH,结果_________________ (填“偏大”、“偏小”或“无影响”)。
(5)“低碳生活”是指生活作息时所耗用的能量要尽量少,减低二氧化碳排放量,从而减少大气污染,保护环境。下列做法符合“低碳生活”理念的是_______ (填序号)。
①节约使用天然气 ②提倡使用一次性木筷 ③大量砍伐森林树木
(1)对野炊有经验的人会告诉你,餐具最好是导热性好,不易破碎的材料制成,你准备带的餐具是用
A.金属 B.陶瓷 C.无所谓
(2)野炊食谱如下:主食:馒头 配菜:红烧肉、豆腐汤、牛肉干。主食和配菜中主要含蛋白质、
(3)用高锰酸钾制氧气时,收集到的氧气略显红色,可能的错误操作是
(4)用水将pH试纸润湿后,再测某稀盐酸的pH,结果
(5)“低碳生活”是指生活作息时所耗用的能量要尽量少,减低二氧化碳排放量,从而减少大气污染,保护环境。下列做法符合“低碳生活”理念的是
①节约使用天然气 ②提倡使用一次性木筷 ③大量砍伐森林树木
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据要求填空
(1)溶液pH可以用pH试纸测量,也可以用___________ 测量。
(2)Na2CO3溶液显碱性的原因是(用离子方程式说明)___________ 。
(3)根据碰撞理论解释温度升高化学反应速率加快的原因___________ 。
(1)溶液pH可以用pH试纸测量,也可以用
(2)Na2CO3溶液显碱性的原因是(用离子方程式说明)
(3)根据碰撞理论解释温度升高化学反应速率加快的原因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作________ (填“正确”或“错误”),该操作是否一定有误差?并说明原因_______________________ 。
(2)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的是_______ ,原因是__________________________ 。
(3)只从下列试剂中选择实验所需的试剂,你能否区分0.1mol∙L-1硫酸溶液和0.01mol∙L-1硫酸溶液?___________ ,简述操作过程:___________________________ 。
试剂:A.紫色石蕊试液 B.酚酞试液 C.甲基橙溶液 D.蒸馏水 E.氯化钡溶液 F.pH试纸
(1)该学生的操作
(2)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的是
(3)只从下列试剂中选择实验所需的试剂,你能否区分0.1mol∙L-1硫酸溶液和0.01mol∙L-1硫酸溶液?
试剂:A.紫色石蕊试液 B.酚酞试液 C.甲基橙溶液 D.蒸馏水 E.氯化钡溶液 F.pH试纸
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】酸、碱、盐在水溶液中的离子反应在生活和生产中有广泛的应用,请回答下列问题。
(1)洗涤剂中的 俗称“纯碱”的原因是
俗称“纯碱”的原因是___________ (用离子方程式表示),洗涤油腻餐具时,使用温水效果更佳,原因是___________ 。
(2) 时,相同
时,相同 的盐酸与
的盐酸与 溶液分别加水稀释100倍后,比较两溶液的
溶液分别加水稀释100倍后,比较两溶液的 大小:盐酸
大小:盐酸___________  溶液(填“>”、“=”或“<”)。
溶液(填“>”、“=”或“<”)。
(3)菠菜等植物中含有丰富的草酸( ),草酸对生命活动有重要影响。
),草酸对生命活动有重要影响。
①草酸是一种二元弱酸,写出它在水中的电离方程式___________ ,要使溶液中 的电离平衡正向移动且
的电离平衡正向移动且 增大,可以采取的措施有
增大,可以采取的措施有___________ 。
②已知 时,
时,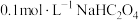 ,溶液的
,溶液的 ,则
,则 溶液中
溶液中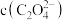 、
、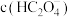 、
、 由小到大的顺序为
由小到大的顺序为___________ 。
(1)洗涤剂中的
 俗称“纯碱”的原因是
俗称“纯碱”的原因是(2)
 时,相同
时,相同 的盐酸与
的盐酸与 溶液分别加水稀释100倍后,比较两溶液的
溶液分别加水稀释100倍后,比较两溶液的 大小:盐酸
大小:盐酸 溶液(填“>”、“=”或“<”)。
溶液(填“>”、“=”或“<”)。(3)菠菜等植物中含有丰富的草酸(
 ),草酸对生命活动有重要影响。
),草酸对生命活动有重要影响。①草酸是一种二元弱酸,写出它在水中的电离方程式
 的电离平衡正向移动且
的电离平衡正向移动且 增大,可以采取的措施有
增大,可以采取的措施有②已知
 时,
时,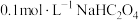 ,溶液的
,溶液的 ,则
,则 溶液中
溶液中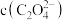 、
、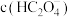 、
、 由小到大的顺序为
由小到大的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.根据表中数据(常温下),完成下列填空。
(1)常温下,NaCN溶液呈____ (填“酸”、“碱”或“中”)性,其原因是____ (用离子方程式表示)。
(2)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CH3COONa溶液,②NaCN溶液,③NaHCO3溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是____ (填序号)。
(3)常温下,向NaClO溶液中通入少量CO2,发生反应的离子方程式为____ 。
(4)常温下,Na2SO3溶液中c(OH-)−c(H+)=c(HSO )+
)+____ 。
II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10−12,Ksp(CdS)=8.0×10−27;回答下列问题:
(5)向某含镉废水中加入Na2S,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为____ mol∙L−1,此时是否符合生活饮用水卫生标准?____ (填“是”或“否”)。
(6)室温下,反应CdCO3(s)+S2−(aq) CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=____ (结果保留两位有效数字)
| 物质 | CH3COOH | NH3∙H2O | HCN | HClO | H2CO3 | H2SO3 |
| 电离常数(Ka) | 1.7×10−5 | 1.7×10−5 | 4.9×10−10 | 3×10−8 | Ka1=4.3×10−7 Ka2=5.6×10−11 | Ka1=1.5×10−2 Ka2=1.0×10−7 |
(2)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CH3COONa溶液,②NaCN溶液,③NaHCO3溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是
(3)常温下,向NaClO溶液中通入少量CO2,发生反应的离子方程式为
(4)常温下,Na2SO3溶液中c(OH-)−c(H+)=c(HSO
 )+
)+II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10−12,Ksp(CdS)=8.0×10−27;回答下列问题:
(5)向某含镉废水中加入Na2S,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为
(6)室温下,反应CdCO3(s)+S2−(aq)
 CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】生活中常常用到以下物品:A.纯碱 B.小苏打 C.食醋 D.食盐
(1)纯碱的化学式是____________ ;
(2)主要成分属于酸式盐的是____________ (填选项字母);
(3)纯碱溶液显碱性的原因(用离子方程式表示)__________________ ;
(4)0.1mol/L食盐溶液中离子浓度大小关系_________________________ ;
(5)能抑制水的电离的是____________ (填选项字母)。
(1)纯碱的化学式是
(2)主要成分属于酸式盐的是
(3)纯碱溶液显碱性的原因(用离子方程式表示)
(4)0.1mol/L食盐溶液中离子浓度大小关系
(5)能抑制水的电离的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如图所示三个烧瓶中分别装有含酚酞溶液的0.01mol/L 溶液,并分别放置在盛有水的烧杯中,然后向①中烧杯加入生石灰,向③中烧杯加入
溶液,并分别放置在盛有水的烧杯中,然后向①中烧杯加入生石灰,向③中烧杯加入 晶体,②中烧杯不加任何物质。
晶体,②中烧杯不加任何物质。
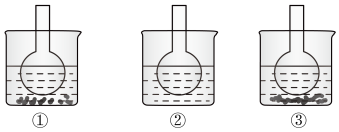
(1)含酚酞溶液的0.01mol/L 溶液显红色的原因为
溶液显红色的原因为____________________________________ 。
(2)实验过程中发现①中烧瓶内溶液红色变深,③中烧瓶内溶液红色变浅,则下列叙述正确的是______ (填标号,双选)。
A.水解反应为放热反应 B.水解反应为吸热反应
C. 溶于水时放出热量 D.
溶于水时放出热量 D. 溶于水时吸收热量
溶于水时吸收热量
(3)向0.01mol/L 溶液中分别加入少量NaOH固体、
溶液中分别加入少量NaOH固体、 固体,则
固体,则 的水解平衡移动的方向分别为
的水解平衡移动的方向分别为__________ 、__________ (填“向左”“向右”或“不移动”)。
 溶液,并分别放置在盛有水的烧杯中,然后向①中烧杯加入生石灰,向③中烧杯加入
溶液,并分别放置在盛有水的烧杯中,然后向①中烧杯加入生石灰,向③中烧杯加入 晶体,②中烧杯不加任何物质。
晶体,②中烧杯不加任何物质。
(1)含酚酞溶液的0.01mol/L
 溶液显红色的原因为
溶液显红色的原因为(2)实验过程中发现①中烧瓶内溶液红色变深,③中烧瓶内溶液红色变浅,则下列叙述正确的是
A.水解反应为放热反应 B.水解反应为吸热反应
C.
 溶于水时放出热量 D.
溶于水时放出热量 D. 溶于水时吸收热量
溶于水时吸收热量(3)向0.01mol/L
 溶液中分别加入少量NaOH固体、
溶液中分别加入少量NaOH固体、 固体,则
固体,则 的水解平衡移动的方向分别为
的水解平衡移动的方向分别为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】钛用途广泛,焦磷酸镁(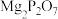 )不溶于水,是牙膏、牙粉的稳定剂。一种以含钛废料(主要成分为
)不溶于水,是牙膏、牙粉的稳定剂。一种以含钛废料(主要成分为 ,含少量
,含少量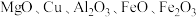 )为原料,分离提纯
)为原料,分离提纯 并制取少量焦磷酸镁的工艺流程如下:
并制取少量焦磷酸镁的工艺流程如下:
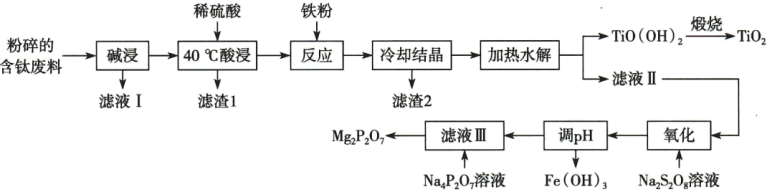
已知: 不与碱反应,与酸反应后以
不与碱反应,与酸反应后以 的形式存在。回答下列问题:
的形式存在。回答下列问题:
(1)“碱浸”和“酸浸”操作的目的是_______ 。
(2)适当升高温度可有效提高钛的浸出率,工业上“酸浸”时,温度选择 而不选择更高温度的原因是:
而不选择更高温度的原因是:_______ 。
 )不溶于水,是牙膏、牙粉的稳定剂。一种以含钛废料(主要成分为
)不溶于水,是牙膏、牙粉的稳定剂。一种以含钛废料(主要成分为 ,含少量
,含少量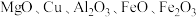 )为原料,分离提纯
)为原料,分离提纯 并制取少量焦磷酸镁的工艺流程如下:
并制取少量焦磷酸镁的工艺流程如下:
已知:
 不与碱反应,与酸反应后以
不与碱反应,与酸反应后以 的形式存在。回答下列问题:
的形式存在。回答下列问题:(1)“碱浸”和“酸浸”操作的目的是
(2)适当升高温度可有效提高钛的浸出率,工业上“酸浸”时,温度选择
 而不选择更高温度的原因是:
而不选择更高温度的原因是:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】【实验探究】
【实验1】在小烧杯中加入20 mL 0.1 mol·L-1 Fe(NO3)3溶液,用pH计测量该溶液的pH。
实验现象:溶液的pH___________ 7。实验结论与解释______________________ 。
【实验2】在另一只小烧杯中加入5 mL 0.1 mol·L-1 Fe(NO3)3溶液,加水稀释到50 mL,用pH计测量该溶液的pH。
实验现象:溶液的pH比稀释前___________ 。
实验结论与解释:稀释的过程中虽然FeCl3的水解平衡向正反应方向移动,但稀释对H+浓度的变化占主要优势,所以pH比稀释前大。
【实验3】在A、B、C三支试管中加入等体积0.1 mol·L-1Fe(NO3)3溶液。将A试管在酒精灯火焰上加热到溶液沸腾,向B试管中加入3滴6 mol·L-1 HNO3溶液。观察A、B试管中溶液的颜色,并与C试管中溶液的颜色比较。用化学平衡移动的原理解释上述实验现象。
实验现象:A与C比较颜色___________ ;B与C比较颜色___________ 。
实验结论与解释:加热时A中Fe(NO3)3的水解平衡向___________ 方向移动,Fe3+浓度___________ ,颜色___________ ;向B中加HNO3时,Fe(NO3)3的水解平衡向___________ 方向移动,Fe3+浓度___________ ,颜色___________ 。
【实验1】在小烧杯中加入20 mL 0.1 mol·L-1 Fe(NO3)3溶液,用pH计测量该溶液的pH。
实验现象:溶液的pH
【实验2】在另一只小烧杯中加入5 mL 0.1 mol·L-1 Fe(NO3)3溶液,加水稀释到50 mL,用pH计测量该溶液的pH。
实验现象:溶液的pH比稀释前
实验结论与解释:稀释的过程中虽然FeCl3的水解平衡向正反应方向移动,但稀释对H+浓度的变化占主要优势,所以pH比稀释前大。
【实验3】在A、B、C三支试管中加入等体积0.1 mol·L-1Fe(NO3)3溶液。将A试管在酒精灯火焰上加热到溶液沸腾,向B试管中加入3滴6 mol·L-1 HNO3溶液。观察A、B试管中溶液的颜色,并与C试管中溶液的颜色比较。用化学平衡移动的原理解释上述实验现象。
实验现象:A与C比较颜色
实验结论与解释:加热时A中Fe(NO3)3的水解平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1) 的水溶液呈
的水溶液呈________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示);实验室在配制 溶液时,常将
溶液时,常将 固体先溶于较浓的硝酸中,然后再用蒸馏水将其稀释到所需的浓度,以
固体先溶于较浓的硝酸中,然后再用蒸馏水将其稀释到所需的浓度,以_________ (填“促进”或“抑制”)其水解。
(2)明矾可用于净水,原因是___________ (用离子方程式表示)。将 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。
(3)纯碱可代替洗涤剂洗涤餐具,原因是__________ (用离子方程式表示)。
 的水溶液呈
的水溶液呈 溶液时,常将
溶液时,常将 固体先溶于较浓的硝酸中,然后再用蒸馏水将其稀释到所需的浓度,以
固体先溶于较浓的硝酸中,然后再用蒸馏水将其稀释到所需的浓度,以(2)明矾可用于净水,原因是
 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是(3)纯碱可代替洗涤剂洗涤餐具,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Na2CO3溶液中加入少量Ca(OH)2固体,CO32-的水解程度减小,溶液的pH减小。______
您最近一年使用:0次

 和
和 ,获得
,获得 的稀溶液。往
的稀溶液。往 的值将
的值将 填“变大”、“不变”或“变小”
填“变大”、“不变”或“变小”


