某化学小组研究盐酸被MnO2氧化的条件,进行如下实验。
(1)已知MnO2呈弱碱性。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是__ 。
(2)II中发生了分解反应,反应的化学方程式是__ 。
(3)III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:

将实验III、IV作对比,得出的结论是__ ;将i、ii作对比,得出的结论是__ 。
(4)由上述实验得出:盐酸能否被氧化与___ 、___ 有关。
实验 | 操作 | 现象 |
I | 常温下将MnO2和12mol·L-1浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 |
II | 将I中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
III | 加热MnO2和4mol·L-1稀盐酸混合物 | 无明显现象 |
(2)II中发生了分解反应,反应的化学方程式是
(3)III中无明显现象的原因,可能是c(H+)或c(Cl-)较低,设计实验IV进行探究:

将实验III、IV作对比,得出的结论是
(4)由上述实验得出:盐酸能否被氧化与
更新时间:2020-11-16 18:09:23
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是人体必需元素,同时在生产生活中有重要应用。
I.(1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力。药品美蓝是其有效的解毒剂,解毒时美蓝发生_______ (填“氧化”或“还原”)反应。
(2)设计简单的实验,检验某补铁口服液(主要成分为葡萄糖酸亚铁)是否已经氧化变质_______ ;
II. 碳酸亚铁(FeCO3)也可作为补血剂(片剂),利用某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)制备FeCO3的流程如下:

(3) “还原”时,FeS2与H2SO4不反应,Fe3+通过两个反应被还原,其中一个反应如下:FeS2+14Fe3++8H2O===15Fe2++2 +16H+,则另一个反应的离子方程式为
+16H+,则另一个反应的离子方程式为_________ 。
(4)化学社的同学欲用下图装置模拟“沉淀”步骤,操作如下:
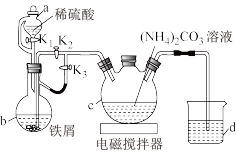
①打开a中K1、K3,关闭K2,
②一段时间后,_________ ,反应过程中生成的氢气的作用是________ 、_________ (至少写两条),d装置的作用是_________ ;
(5) 写出在空气中煅烧FeCO3制备高纯铁红的化学方程式:____________ 。
I.(1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力。药品美蓝是其有效的解毒剂,解毒时美蓝发生
(2)设计简单的实验,检验某补铁口服液(主要成分为葡萄糖酸亚铁)是否已经氧化变质
II. 碳酸亚铁(FeCO3)也可作为补血剂(片剂),利用某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)制备FeCO3的流程如下:

(3) “还原”时,FeS2与H2SO4不反应,Fe3+通过两个反应被还原,其中一个反应如下:FeS2+14Fe3++8H2O===15Fe2++2
 +16H+,则另一个反应的离子方程式为
+16H+,则另一个反应的离子方程式为(4)化学社的同学欲用下图装置模拟“沉淀”步骤,操作如下:

①打开a中K1、K3,关闭K2,
②一段时间后,
(5) 写出在空气中煅烧FeCO3制备高纯铁红的化学方程式:
您最近一年使用:0次
【推荐2】第IIB族元素(Zn、Cd、Hg)和第VIA族元素(S、Se、Te)组成的某些二元化合物常用作半导体材料,应用十分广泛。
(1)基态Se原子价电子排布式为____ ,有____ 个未成对电子。
(2)碲酸(H6TeO6)是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为____ 。
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:
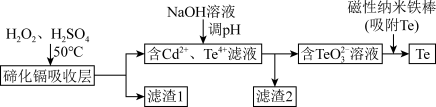
①碲化镉吸收层中的CdTe参与反应的化学方程式为____ ,滤渣1含有的一种单质是____ 。
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=____ 。(已知Ksp[Cd(OH)2]=5.3×10-15)。
(1)基态Se原子价电子排布式为
(2)碲酸(H6TeO6)是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】NaClO2是一种重要的杀菌消毒剂,其一种生产工艺如图:

(1)NaClO2中Cl的化合价为_______ 。
(2)写出“反应”步骤中生成ClO2的化学方程式_______ 。
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用单线桥表示电子转移方向和数目_______ 。
②此吸收反应中,氧化产物是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
③比较氧化性:ClO2_______ O2(填“>”、“<”或“=”)。

(1)NaClO2中Cl的化合价为
(2)写出“反应”步骤中生成ClO2的化学方程式
(3)“尾气吸收”是吸收“电解”过程排出的少量ClO2,发生如下反应:2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用单线桥表示电子转移方向和数目
②此吸收反应中,氧化产物是
③比较氧化性:ClO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+=I2+5SO42-+H2O,生成的I2可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
该实验的目的是_________ ;表中V2=_________ 。
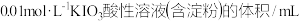 | 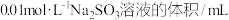 | 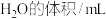 | 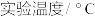 | 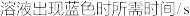 | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】回答下列问题:
Ⅰ.水体中过量氨氮(以NH3表示)会导致水体富营养化。
(1)用次氯酸钠除去氨氮的一种原理如图1所示。写出该图示的总反应化学方程式___________ 。该反应需控制温度,温度过高时氨氮去除率降低的原因是___________ 。

(2)取一定量的含氨氮废水,改变加入次氯酸钠的用量,反应一段时间后,溶液中氨氮去除率、总氮(溶液中所有可溶性的含氮化合物中氮元素的总量)去除率以及剩余次氯酸钠的含量随m(NaClO):m(NH3)的变化情况如图2所示。当m(NaClO):m(NH3)>7.6时,水体中总氮去除率反而下降,可能的原因是___________

Ⅱ.一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1: CO2(g)+H2(g) CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1
反应2: CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
反应3: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH3
CH3OH(g)+H2O(g) ΔH3
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图3所示。

(3)从题给信息分析中可知,ΔH3大于ΔH2,理由是_____ 。
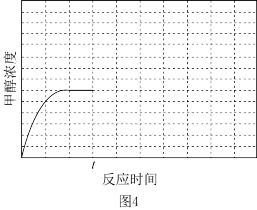
(4)在温度T1时,使体积比为3∶1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图4所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线_____ 。
Ⅰ.水体中过量氨氮(以NH3表示)会导致水体富营养化。
(1)用次氯酸钠除去氨氮的一种原理如图1所示。写出该图示的总反应化学方程式

(2)取一定量的含氨氮废水,改变加入次氯酸钠的用量,反应一段时间后,溶液中氨氮去除率、总氮(溶液中所有可溶性的含氮化合物中氮元素的总量)去除率以及剩余次氯酸钠的含量随m(NaClO):m(NH3)的变化情况如图2所示。当m(NaClO):m(NH3)>7.6时,水体中总氮去除率反而下降,可能的原因是

Ⅱ.一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1: CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1反应2: CO(g)+2H2(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2反应3: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH3
CH3OH(g)+H2O(g) ΔH3其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图3所示。

(3)从题给信息分析中可知,ΔH3大于ΔH2,理由是
(4)在温度T1时,使体积比为3∶1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图4所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组利用H2C2O4溶液与用硫酸酸化的KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
(1)a= _______ ,该实验是通过____________________ 来判断反应的快慢。
(2)已知H2C2O4被KMnO4(H+)氧化为CO2逸出,该反应的化学方程式为________ ,为了观察到实验现象从而判断反应的快慢,H2C2O4与KMnO4初始的物质的量需要满足的关系为:___ 。
(3)探究温度对化学反应速率影响的实验编号是_______ 和_______ (填编号,下同),可探究H2C2O4浓度对化学反应速率影响的实验编号是_______ 和_______ 。
(4)实验①测得反应所用的时间为20s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______ 。
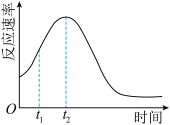
(5)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:_______ ,若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_______ (填序号)
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.氯化锰
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 蒸馏水 体积/ml | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | |||
| ① | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 25 |
| ② | 0.50 | 3.0 | 0.010 | 4.0 | a | 25 |
| ③ | 0.50 | 6.0 | 0.010 | 4.0 | 0 | 50 |
(2)已知H2C2O4被KMnO4(H+)氧化为CO2逸出,该反应的化学方程式为
(3)探究温度对化学反应速率影响的实验编号是
(4)实验①测得反应所用的时间为20s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=
(5)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:

A.硫酸钾 B.硫酸锰 C.稀硫酸 D.氯化锰
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】某研究性实验:
一、利用 溶液和酸
溶液和酸 溶液之间的反应(已知:
溶液之间的反应(已知: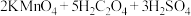
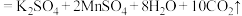 )来探寻“神奇神奇对化学实验的影响” ,出现:
)来探寻“神奇神奇对化学实验的影响” ,出现:
(1)通过实验A 、B ,可探索出______ 的改变对反应加速的影响,其中V 1 =_______ ,T 1 =_______ ,通过实验_______ 可探究温度变化对化学反应速度的影响。(填实验序号)
(2)若t 1<8 ,则可以由实验A 、B得出的结论是_______ ;利用实验B中数据计算,从反应开始到结束,用KMnO 4的浓度变化表示反应的速度为_______ (两个有效数字)。
二、利用以下不同的装置不同的化学条件下能转化为电能。请回答以下问题:

(3)当a为锌、电极为铜、电极溶液为硫酸时,正极的反应式为:_____ 。
(4)当a为Al电极、该电极为镁、该溶液为溶液时,形成原电池的能量为_______ 。
(5)现在电池的工作原理为燃料和燃料(如O2的出出的燃料)。光纤为天线入,则应用通_______ 极(填ab ,下同) ,有16个g或g的参与时,转移电子的参加当为_______ 。
一、利用
 溶液和酸
溶液和酸 溶液之间的反应(已知:
溶液之间的反应(已知: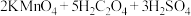
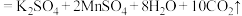 )来探寻“神奇神奇对化学实验的影响” ,出现:
)来探寻“神奇神奇对化学实验的影响” ,出现:| 实验序号 | 实验温度 |  解决方案 解决方案 |  解决方案 解决方案 |  | 溶液褪色时间 | ||
 | 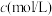 |  | 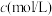 |  | 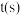 | ||
| 一种 | 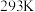 | 2 | 0.02 | 4 | 0.1 | 0 |  |
| 乙 |  | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 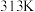 | 2 | 0.02 |  | 0.1 | 1 |  |
(2)若t 1<8 ,则可以由实验A 、B得出的结论是
二、利用以下不同的装置不同的化学条件下能转化为电能。请回答以下问题:

(3)当a为锌、电极为铜、电极溶液为硫酸时,正极的反应式为:
(4)当a为Al电极、该电极为镁、该溶液为溶液时,形成原电池的能量为
(5)现在电池的工作原理为燃料和燃料(如O2的出出的燃料)。光纤为天线入,则应用通
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室利用下列方案探究影响化学反应速率的因素。请回答相关问题:
(1)该实验是定性与定量研究影响化学反应速率的因素,运用的实验方法名称是___________ 。
(2)其他条件不变时,实验①和②是探究___________ 对化学反应速率的影响,实验②和③是探究___________ 对化学反应速率的影响。
(3)实验时,分别量取①、②、③中的H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定___________ 来判断反应的快慢。
(4)该实验中所发生反应的化学方程式___________ 。(提示:反应会生成一种气体,该气体能使澄清石灰水变浑浊)
(5)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是___________ 。
| 编号 | 温度/℃ | H2C2O4溶液 | 酸性KMnO4溶液 | ||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | ||
| ① | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| ② | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| ③ | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
(2)其他条件不变时,实验①和②是探究
(3)实验时,分别量取①、②、③中的H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定
(4)该实验中所发生反应的化学方程式
(5)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究性学习小组利用 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)通过实验_______ (填实验序号)可探究出温度变化对化学反应速率的影响,其中
_______ 。
(2)已知反应后 转化为
转化为 逸出,
逸出, 转化为
转化为 ,每消耗
,每消耗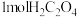 转移
转移_______ mol电子。
(3)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ 。忽略溶液体积的变化,利用实验B中0~8s内,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
_______ 。
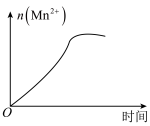
(4)该小组的一位同学通过查阅资料发现,上述实验过程中 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是_______ 。设计实验证明,分别取等体积等浓度的 和
和 混合,平均分成两份,一份中不加任何试剂,一份加入少量
混合,平均分成两份,一份中不加任何试剂,一份加入少量 固体,观察到两溶液都没有褪色,原因是:
固体,观察到两溶液都没有褪色,原因是:_______ 。
 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:| 实验序号 | 实验温度/K | 溶液颜色褪至无色所需时间/s | |||||
酸性 溶液 溶液 |  溶液 溶液 |  | |||||
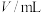 | 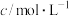 | 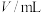 | 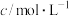 | 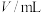 | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 |  |
| B | T | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 1 |  |
(1)通过实验

(2)已知反应后
 转化为
转化为 逸出,
逸出, 转化为
转化为 ,每消耗
,每消耗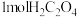 转移
转移(3)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率
的浓度变化表示的反应速率
(4)该小组的一位同学通过查阅资料发现,上述实验过程中
 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是 和
和 混合,平均分成两份,一份中不加任何试剂,一份加入少量
混合,平均分成两份,一份中不加任何试剂,一份加入少量 固体,观察到两溶液都没有褪色,原因是:
固体,观察到两溶液都没有褪色,原因是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硼泥主要由MgO组成,含有Na2B4O7、SiO2、CaO、Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:

已知某些氢氧化物沉淀的pH如下表所示:
(1)滤渣1除含有H3BO3外,还含有_______ 。加入硫酸时Na2B4O7发生反应的离子方程式为_______ 。向滤液1加入H2O2,发生反应的离子方程式为_______ 。
(2)向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为_______ 。
(3)洗涤滤渣3的方法是_______ 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为_______ 。
(5)若取m吨硼泥为原料,最后得到n吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为_______ (用含有m、n的代数式表示)。

已知某些氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | 开始沉淀的pH | 完全沉淀的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
(2)向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为
(3)洗涤滤渣3的方法是
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为
(5)若取m吨硼泥为原料,最后得到n吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】 又称次氯酸酐,是强氧化剂,极易溶于水,沸点为
又称次氯酸酐,是强氧化剂,极易溶于水,沸点为 ℃,42℃以上分解为
℃,42℃以上分解为 和
和 ,高浓度时易爆炸。某学习小组利用
,高浓度时易爆炸。某学习小组利用 和潮湿的碳酸钠反应生成
和潮湿的碳酸钠反应生成 ,再用水吸收
,再用水吸收 制备
制备 溶液,装置如下,请回答下列问题:
溶液,装置如下,请回答下列问题:
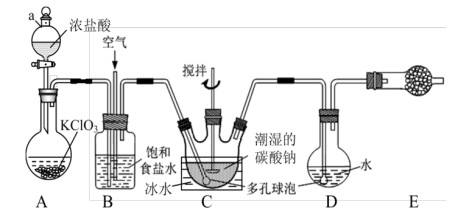
(1)仪器a的名称是___________ ,A中发生反应的离子方程式为___________ 。
(2)实验中须控制 与空气(不参与反应)的体积比为
与空气(不参与反应)的体积比为 ,装置B的作用是
,装置B的作用是___________ (答出两条即可)。
(3)装置C中生成 、
、 ,反应的化学方程式为
,反应的化学方程式为___________ ,为使反应充分进行,实验中采取的措施有___________ 。
(4)若装置C不冷却,则进入装置D中的 会大量减少,可能的原因是
会大量减少,可能的原因是___________ 。
(5)装置E所盛试剂是___________ ,作用是___________ 。
 又称次氯酸酐,是强氧化剂,极易溶于水,沸点为
又称次氯酸酐,是强氧化剂,极易溶于水,沸点为 ℃,42℃以上分解为
℃,42℃以上分解为 和
和 ,高浓度时易爆炸。某学习小组利用
,高浓度时易爆炸。某学习小组利用 和潮湿的碳酸钠反应生成
和潮湿的碳酸钠反应生成 ,再用水吸收
,再用水吸收 制备
制备 溶液,装置如下,请回答下列问题:
溶液,装置如下,请回答下列问题:
(1)仪器a的名称是
(2)实验中须控制
 与空气(不参与反应)的体积比为
与空气(不参与反应)的体积比为 ,装置B的作用是
,装置B的作用是(3)装置C中生成
 、
、 ,反应的化学方程式为
,反应的化学方程式为(4)若装置C不冷却,则进入装置D中的
 会大量减少,可能的原因是
会大量减少,可能的原因是(5)装置E所盛试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
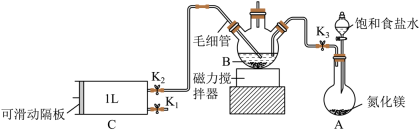
【推荐3】检验甲醛用银−Ferrozine法灵敏度较高。测定原理为甲醛与银氨溶液反应生成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设计如图装置,测定新装修居室内空气中甲醛的含量(夹持装置略去)。
回答下列问题:
(1)A装置中反应的化学方程式为______ ,用饱和食盐水代替水制备NH3的原因是_______ 。
(2)B中装有硝酸银溶液,仪器B的名称为_______ 。
(3)银氨溶液的制备。关闭K1、K2,打开K3,打开_______ ,使饱和食盐水慢慢滴入圆底烧瓶中,当观察到B中_______ ,停止通入NH3。
(4)甲醛与银氨溶液反应的产物中有一种正盐,其化学方程式为_______ 。
(5)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气,关闭K1;后续操作是_______ ;再重复上述操作3次。毛细管的作用是_______ 。
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成1.12mgFe2+,空气中甲醛的含量为_______ mg·L−1。
回答下列问题:
(1)A装置中反应的化学方程式为
(2)B中装有硝酸银溶液,仪器B的名称为
(3)银氨溶液的制备。关闭K1、K2,打开K3,打开
(4)甲醛与银氨溶液反应的产物中有一种正盐,其化学方程式为
(5)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气,关闭K1;后续操作是
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成1.12mgFe2+,空气中甲醛的含量为
您最近一年使用:0次



