已知室温时0.1mol/L某一元酸HA在水中有0.1%发生电离,叙述错误的是
| A.该溶液的pH=4 |
| B.升高温度,溶液的Kw增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.该溶液里不存在HA分子 |
更新时间:2020-11-17 13:12:29
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列关于水的电离不正确的是
| A.加酸或碱一定抑制水的电离 |
| B.常温下任何稀的酸、碱、盐水溶液中Kw=10-14 |
| C.升高温度,水的pH值变小 |
| D.加盐一定促进水的电离 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列各组溶液中,离子一定能大量共存的是
A.滴入KSCN(aq)显红色的溶液:K+、NH 、Cl-、I- 、Cl-、I- |
B.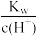 =0.1 mol·L-1的溶液:Na+、K+、SiO =0.1 mol·L-1的溶液:Na+、K+、SiO 、NO 、NO |
C.无色溶液:K+、Na+、SO 、MnO 、MnO |
D.含0.1mol/LAl2(SO4)3的溶液:K+、Ca2+、HCO 、Cl- 、Cl- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】水的电离平衡曲线如下图所示。下列说法正确的是
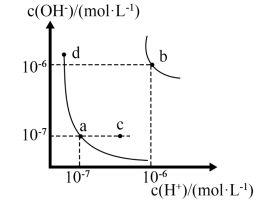

| A.图中对应点的温度关系为: a>b |
| B.水的电离常数KW大小关系为:b>d |
| C.温度不变,加入少量NaOH可使溶液从c点变到a点 |
| D.b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显酸性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
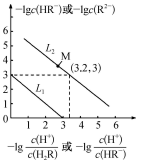
【推荐1】常温下,向Na2R溶液中缓慢通入氯化氢气体,溶液中-lgc(HR-)或-lgc(HR-)或-lgc(R2-)-lgc(R2-)分别与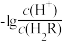 或
或 之间变化关系(曲线L1、L2)如图所示。下列说法中错误的是
之间变化关系(曲线L1、L2)如图所示。下列说法中错误的是
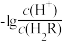 或
或 之间变化关系(曲线L1、L2)如图所示。下列说法中错误的是
之间变化关系(曲线L1、L2)如图所示。下列说法中错误的是
| A.Ka2(H2R)的数量级为10-7 |
| B.NaHR 溶液显酸性 |
| C.M点溶液中:c(H+ )+c(Na+ )=c(HR-)+2c(R2- )+c(OH- ) |
| D.Na2R溶液中: c(OH- ) >c(HR-)+ c(H2R) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25℃时,下列事实不能说明HF是弱酸的是
| A.0.1 mol·L-1的氢氟酸溶液pH>1 | B.升温,氢氟酸溶液的酸性明显增强 |
| C.氢氟酸溶液中含有HF分子 | D.稀氢氟酸溶液的导电能力弱 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】常温下,向 的
的 溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是
溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是

 的
的 溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是
溶液中滴入NaOH溶液,随着pH变化溶液中浓度最大的含磷微粒如图所示。下列说法正确的是
A. 时, 时, |
B. 时, 时, |
C. 时, 时, |
D.若用 的 的 溶液进行实验, 溶液进行实验, 将向左移动 将向左移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
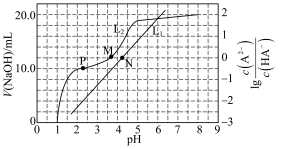
【推荐2】25℃时,用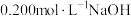 溶液滴定
溶液滴定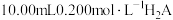 溶液,加入NaOH溶液的体积、
溶液,加入NaOH溶液的体积、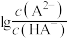 与pH的变化关系如图所示。下列说法正确的是
与pH的变化关系如图所示。下列说法正确的是
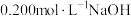 溶液滴定
溶液滴定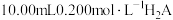 溶液,加入NaOH溶液的体积、
溶液,加入NaOH溶液的体积、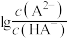 与pH的变化关系如图所示。下列说法正确的是
与pH的变化关系如图所示。下列说法正确的是
A. 表示加入NaOH溶液的体积与pH的变化关系 表示加入NaOH溶液的体积与pH的变化关系 |
B. 的第二步电离常数 的第二步电离常数 的数量级为 的数量级为 |
C.M点所处溶液中: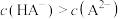 |
| D.第二滴定终点可以选择甲基橙做指示剂 |
您最近一年使用:0次


 2H++CO
2H++CO
 减小
减小 增大
增大 >1
>1 不变
不变

