三氧化二铋(Bi2O3)是黄色不溶于水的固体,俗称铋黄,可用于制作黄色颜料、耐火纸等。利用含铋废料(还含Cu、Pb、Zn的硫酸盐及CuS、Fe2O3)制备Bi2O3流程如下:
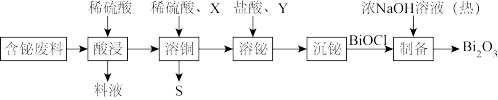
(1)“酸浸”后的固体中除含铋的化合物、CuS外,还含有___________ ;料液中含有多种成分,向料液中加入过量锌粉并充分搅拌,过滤后,滤液经过___________ 冷却结晶、过滤、洗涤、干燥即可制得ZnSO4·7H2O。
(2)“溶铜”时,试剂X可以是多种物质,分别使用O2、H2O2、MnO2三种氧化剂,氧化等物质的量同一种还原剂时,且得到相同氧化产物,消耗这三种氧化剂物质的量之比为___________ (MnO2转化为Mn2+);写出X为O2时,“溶铜”CuS反应的离子方程式:___________ 。
(3)其他条件相同时,溶液中c(Cl-)越大,铋的溶出率越大,仅从原料成本角度考虑,试剂Y是___________ 。
(4)写出“制备”步骤生成铋黄的离子方程式:___________ 。

(1)“酸浸”后的固体中除含铋的化合物、CuS外,还含有
(2)“溶铜”时,试剂X可以是多种物质,分别使用O2、H2O2、MnO2三种氧化剂,氧化等物质的量同一种还原剂时,且得到相同氧化产物,消耗这三种氧化剂物质的量之比为
(3)其他条件相同时,溶液中c(Cl-)越大,铋的溶出率越大,仅从原料成本角度考虑,试剂Y是
(4)写出“制备”步骤生成铋黄的离子方程式:
更新时间:2020-12-15 21:48:35
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】化合物A由四种常见元素组成。某同学为探究其组成进行了如图实验:
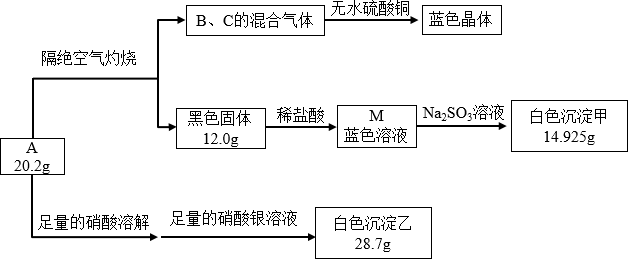
(1)已知A在隔绝空气灼烧时发生的是非氧化还原反应,黑色固体是______ (写化学式)。
(2)白色沉淀乙证明A中含______ 元素。(写元素符号)
(3)白色沉淀甲是一种氯化物,M溶液与Na2SO3溶液属于氧化还原反应,那么白色沉淀______ (写名称)。写出该反应的离子方程式______ ,得到白色沉淀的方法是______ 。检验硫酸根离子的操作______ 。
(4)A的化学式为______ 。

(1)已知A在隔绝空气灼烧时发生的是非氧化还原反应,黑色固体是
(2)白色沉淀乙证明A中含
(3)白色沉淀甲是一种氯化物,M溶液与Na2SO3溶液属于氧化还原反应,那么白色沉淀
(4)A的化学式为
您最近一年使用:0次
【推荐2】固体化合物由两种元素组成,某小组开展如下探究实验,其中气体A有刺激性气味,能使湿润的红色石蕊试纸变蓝。为探究X的组成,某研究小组进行如下实验:

(1)X的化学式是_______ ;刺激性气体分子电子式_______ ;
(2)X在纯氧中加强热的化学方程式_______ ;
(3)X与稀硫酸的离子反应方程式:_______ ;
(4)为探究固体丙是否是纯净物,请设计简单的实验方案:_______ 。

(1)X的化学式是
(2)X在纯氧中加强热的化学方程式
(3)X与稀硫酸的离子反应方程式:
(4)为探究固体丙是否是纯净物,请设计简单的实验方案:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】某兴趣小组对化合物X开展探究实验。
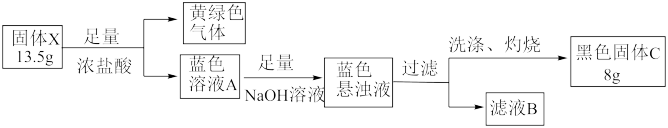
其中:X是一种难溶于水的黑色物质,含有3种元素:蓝色溶液A中只有一种酸根离子;滤液B的焰色呈紫色(透过蓝色钴玻璃片)。
请回答:
(1)组成化合物X的3种元素是___________ (填元素符号),滤液B中含有的溶质是___________ (用化学式表示)。
(2)X与浓盐酸反应的离子方程式是___________ 。
(3)蓝色悬浊液可用于医学上糖尿病的检测,该反应的化学方程式是___________ 。
(4) 在加热条件下与黑色固体C反应生成红色固体,设计方案探究红色固体的可能组成
在加热条件下与黑色固体C反应生成红色固体,设计方案探究红色固体的可能组成___________ 。

其中:X是一种难溶于水的黑色物质,含有3种元素:蓝色溶液A中只有一种酸根离子;滤液B的焰色呈紫色(透过蓝色钴玻璃片)。
请回答:
(1)组成化合物X的3种元素是
(2)X与浓盐酸反应的离子方程式是
(3)蓝色悬浊液可用于医学上糖尿病的检测,该反应的化学方程式是
(4)
 在加热条件下与黑色固体C反应生成红色固体,设计方案探究红色固体的可能组成
在加热条件下与黑色固体C反应生成红色固体,设计方案探究红色固体的可能组成
您最近一年使用:0次
【推荐1】从铜电解液(主要含Cu2+、Ni2+、Fe2+、Fe3+、Ca2+、Zn2+等)中提纯可得到粗硫酸镍晶体,某课题小组为了进一步精制纯化并回收胆矾晶体,设计了如图流程:
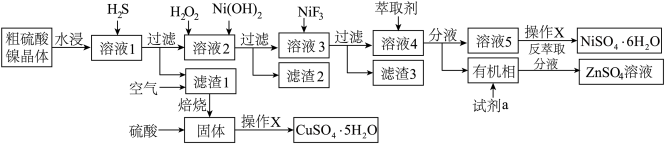
已知:相关离子浓度为0.1 mol· L-1时,形成氢氧化物沉淀的pH范围如下:
(1)为加快“水浸”时的浸出率,可采取的措施有 _______ ,“滤渣1”的主要成份是_______ 。
(2)为了使“溶液1”中的反应充分进行,需要通入稍过量的H2S,写出Fe3+与H2S发生反应的离子方程式______ 。
(3)解释向“溶液2”中加入Ni(OH)2的原因_______ 。
(4)“操作X”为在_______ (填仪器名称)中加热至_______ 冷却结晶过滤、洗涤、干燥后得到结晶水合物晶体。
(5)若“溶液3”中Ca2+的浓度为0.001 mol·L-1,取等体积的NiF2溶液与该溶液混合,要使反应结束时c(Ca2+)<10-5 mol· L-1,则所加NiF2溶液的浓度至少为_______ mol · L-1。[已知室温下Ksp(CaF2)=4×10-11]
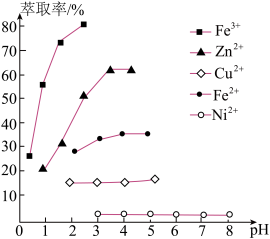
(6)室温下选择萃取剂P204(二乙基已基磷酸,用HR表示),其萃取原理为nHR +Mn+ MRn +nH+,试剂a为
MRn +nH+,试剂a为_____ (填化学式)。溶液pH对几种离子的萃取率的影响如图,则萃取锌时,应控制pH的范围为3~4,请解释原因_______ 。

已知:相关离子浓度为0.1 mol· L-1时,形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Cu2+ | Fe2+ | Fe3+ | Ca2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 4.2 | 6.3 | 1.5 | 11.8 | 6.2 | 6.9 |
| 沉淀完全的pH | 6.7 | 8.3 | 2.8 | 13.8 | 8.2 | 8.9 |
(2)为了使“溶液1”中的反应充分进行,需要通入稍过量的H2S,写出Fe3+与H2S发生反应的离子方程式
(3)解释向“溶液2”中加入Ni(OH)2的原因
(4)“操作X”为在
(5)若“溶液3”中Ca2+的浓度为0.001 mol·L-1,取等体积的NiF2溶液与该溶液混合,要使反应结束时c(Ca2+)<10-5 mol· L-1,则所加NiF2溶液的浓度至少为
(6)室温下选择萃取剂P204(二乙基已基磷酸,用HR表示),其萃取原理为nHR +Mn+
 MRn +nH+,试剂a为
MRn +nH+,试剂a为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铬铁矿的要紧成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如图所示。
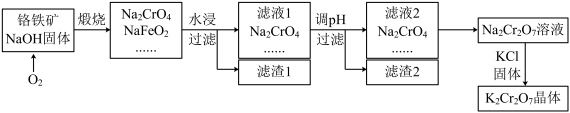
已知:①NaFeO2遇水强烈水解 。
②2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
请回答:
(1)K2Cr2O7中Cr元素的化合价是___ 。
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是___ 。
(3)滤渣1为红褐色的固体,滤渣1的成分是(填名称 )____ ,滤液1的成分除Na2CrO4、NaOH外,还含有___ (填化学式 )。
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是___ 。
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是___ 。
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、____ 、过滤、洗涤、干燥。

已知:①NaFeO2遇水
②2CrO42-+2H+
 Cr2O72-+H2O
Cr2O72-+H2O请回答:
(1)K2Cr2O7中Cr元素的化合价是
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
(3)滤渣1为红褐色的固体,滤渣1的成分是(填
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】硫酸亚铁晶体( )俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有
)俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有 、
、 的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
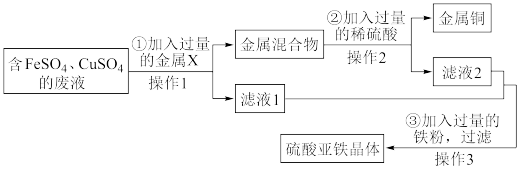
(1)步骤①中:
Ⅰ.金属X是__________ 。(填化学式)
Ⅱ.操作1的名称是__________ ,此操作中玻璃棒的作用是__________ 。
(2)步骤②中:
Ⅰ.加入过量稀硫酸的目的是__________ 。所得滤液2中含有的溶质是__________ 。(填化学式)
Ⅱ.洗涤金属铜的操作是__________ 。
Ⅲ.检验铜洗净的操作是_______________ 。
(3)操作3为蒸发浓缩、__________ 、过滤。
(4)若废液的体积为 ,废液中
,废液中 的浓度为
的浓度为 、
、 的浓度为
的浓度为 。
。
Ⅰ.理论上废液回收得到的金属铜的质量为__________ 。
Ⅱ.若整个过程中参与反应的铁共 ,
,__________ (填“能”或“不能”)计算出得到 的质量。若不能,写出原因;若能,写出计算过程和结果。
的质量。若不能,写出原因;若能,写出计算过程和结果。__________
 )俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有
)俗称绿矾,可用来制药,受热易分解失去结晶水。某兴趣小组从实验室收集到一桶含有 、
、 的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
的废液,想从中回收金属铜和硫酸亚铁晶体,设计的实验方案如下图,结合实验方案回答下列问题:
(1)步骤①中:
Ⅰ.金属X是
Ⅱ.操作1的名称是
(2)步骤②中:
Ⅰ.加入过量稀硫酸的目的是
Ⅱ.洗涤金属铜的操作是
Ⅲ.检验铜洗净的操作是
(3)操作3为蒸发浓缩、
(4)若废液的体积为
 ,废液中
,废液中 的浓度为
的浓度为 、
、 的浓度为
的浓度为 。
。Ⅰ.理论上废液回收得到的金属铜的质量为
Ⅱ.若整个过程中参与反应的铁共
 ,
, 的质量。若不能,写出原因;若能,写出计算过程和结果。
的质量。若不能,写出原因;若能,写出计算过程和结果。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。主要反应的化学方程式为NaCl+NH3+CO2+H2O =NaHCO3↓+NH4Cl。氨气为碱性气体。
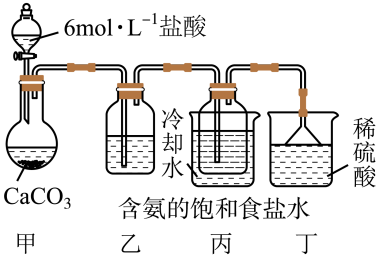
(1)某探究活动小组根据上述制碱原理,将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
试回答下列有关问题:
①乙装置中的试剂是_______ ;
②丁装置中稀硫酸的作用是_______ 。
(2)实验结束后用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有_______ 、洗涤固体、_______ 。第一步操作需要的主要玻璃仪器为_______ ,最后一步发生反应的化学方程式为_______ 。
(3)证明所得Na2CO3中可能含有未分解的NaHCO3晶体的方法是_______ 。
(1)某探究活动小组根据上述制碱原理,将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

试回答下列有关问题:
①乙装置中的试剂是
②丁装置中稀硫酸的作用是
(2)实验结束后用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
(3)证明所得Na2CO3中可能含有未分解的NaHCO3晶体的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】磷化氢( )常用于缩合催化剂、磷的有机化合物制备等。实验室用白磷(
)常用于缩合催化剂、磷的有机化合物制备等。实验室用白磷( )与浓
)与浓 (过量)加热制备
(过量)加热制备 同时得到次磷酸钠(
同时得到次磷酸钠( )装置如下图。
)装置如下图。
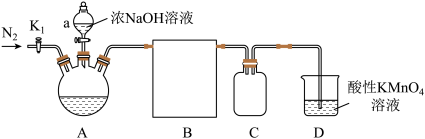
已知: 是无色有毒气体,有强还原性,易自燃。
是无色有毒气体,有强还原性,易自燃。
(1)仪器a的名称为_______ ,B应选用下图中装置_______ 。
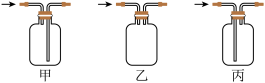
(2)实验操作有如下步骤:
①打开 ,通入
,通入 一段时间
一段时间
②检查装置气密性
③关闭 ,打开磁力加热搅拌器加热至50℃~60℃,滴加烧碱溶液
,打开磁力加热搅拌器加热至50℃~60℃,滴加烧碱溶液
④在A中加入丁醇和白磷。则正确的操作顺序是_______ 。
(3)装置A中发生反应的化学方程式为_______ ,已知 水溶液
水溶液 ,水溶液
,水溶液 的原因
的原因_______ 。
(4)反应结束后也要打开 ,继续通入
,继续通入 的目的是
的目的是_____ ,装置D的作用是_____ 。
(5)测定 纯度。
纯度。
提纯A中反应后的混合物,得到 (
(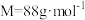 )粗品,取1.00g配成
)粗品,取1.00g配成 溶液,取
溶液,取 于锥形瓶中,酸化后加入
于锥形瓶中,酸化后加入
 碘水,充分反应,以淀粉溶液作指示剂,用
碘水,充分反应,以淀粉溶液作指示剂,用
 溶液滴定至终点,平均消耗
溶液滴定至终点,平均消耗 。则产品纯度为
。则产品纯度为_____ 。
用 溶液滴定时尖嘴处开始有气泡,达到滴定终点时无气泡,则测定结果
溶液滴定时尖嘴处开始有气泡,达到滴定终点时无气泡,则测定结果____ (“偏大”、“偏小”或“无影响”)。
(相关反应为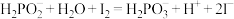 ,
, )
)
 )常用于缩合催化剂、磷的有机化合物制备等。实验室用白磷(
)常用于缩合催化剂、磷的有机化合物制备等。实验室用白磷( )与浓
)与浓 (过量)加热制备
(过量)加热制备 同时得到次磷酸钠(
同时得到次磷酸钠( )装置如下图。
)装置如下图。
已知:
 是无色有毒气体,有强还原性,易自燃。
是无色有毒气体,有强还原性,易自燃。(1)仪器a的名称为

(2)实验操作有如下步骤:
①打开
 ,通入
,通入 一段时间
一段时间②检查装置气密性
③关闭
 ,打开磁力加热搅拌器加热至50℃~60℃,滴加烧碱溶液
,打开磁力加热搅拌器加热至50℃~60℃,滴加烧碱溶液④在A中加入丁醇和白磷。则正确的操作顺序是
(3)装置A中发生反应的化学方程式为
 水溶液
水溶液 ,水溶液
,水溶液 的原因
的原因(4)反应结束后也要打开
 ,继续通入
,继续通入 的目的是
的目的是(5)测定
 纯度。
纯度。提纯A中反应后的混合物,得到
 (
(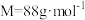 )粗品,取1.00g配成
)粗品,取1.00g配成 溶液,取
溶液,取 于锥形瓶中,酸化后加入
于锥形瓶中,酸化后加入
 碘水,充分反应,以淀粉溶液作指示剂,用
碘水,充分反应,以淀粉溶液作指示剂,用
 溶液滴定至终点,平均消耗
溶液滴定至终点,平均消耗 。则产品纯度为
。则产品纯度为用
 溶液滴定时尖嘴处开始有气泡,达到滴定终点时无气泡,则测定结果
溶液滴定时尖嘴处开始有气泡,达到滴定终点时无气泡,则测定结果(相关反应为
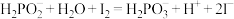 ,
, )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫酸亚铁铵又称摩尔盐,它在空气中比一般的亚铁铵盐稳定,可用作治疗缺铁性贫血的药物,化学式为 (摩尔质量为
(摩尔质量为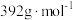 )。实验室利用废铁屑(含有少量
)。实验室利用废铁屑(含有少量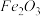 )制备摩尔盐晶体的步骤如下:
)制备摩尔盐晶体的步骤如下:
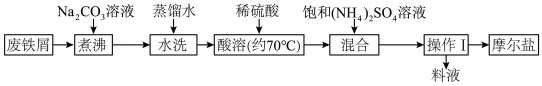
(1)煮沸的好处是___________ ,水洗的目的是___________ 。
(2)写出此过程中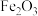 转化为
转化为 的总反应离子方程式
的总反应离子方程式___________ ,欲确定酸溶后溶液中有无 ,使用的检验试剂最好是
,使用的检验试剂最好是___________ 。
(3)为测量产品纯度,某同学称取 摩尔盐样品溶于蒸馏水中,然后用
摩尔盐样品溶于蒸馏水中,然后用 的酸性
的酸性 标准进行滴定,滴定终点时消耗
标准进行滴定,滴定终点时消耗 标准溶液。
标准溶液。
①下图中表示盛有标准溶液的滴定管滴定前排气泡,正确的是___________ 。
a.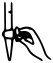 b.
b. c.
c. d.
d.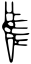
②所测样品中摩尔盐晶体的纯度是___________ (用含V的式子表示),若整个测量实验操作无误,实际消耗的标准溶液体积 ,则可以得出的与样品组成有关的结论是
,则可以得出的与样品组成有关的结论是___________ 。
 (摩尔质量为
(摩尔质量为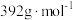 )。实验室利用废铁屑(含有少量
)。实验室利用废铁屑(含有少量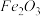 )制备摩尔盐晶体的步骤如下:
)制备摩尔盐晶体的步骤如下:
(1)煮沸的好处是
(2)写出此过程中
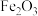 转化为
转化为 的总反应离子方程式
的总反应离子方程式 ,使用的检验试剂最好是
,使用的检验试剂最好是(3)为测量产品纯度,某同学称取
 摩尔盐样品溶于蒸馏水中,然后用
摩尔盐样品溶于蒸馏水中,然后用 的酸性
的酸性 标准进行滴定,滴定终点时消耗
标准进行滴定,滴定终点时消耗 标准溶液。
标准溶液。①下图中表示盛有标准溶液的滴定管滴定前排气泡,正确的是
a.
 b.
b. c.
c. d.
d.
②所测样品中摩尔盐晶体的纯度是
 ,则可以得出的与样品组成有关的结论是
,则可以得出的与样品组成有关的结论是
您最近一年使用:0次



