已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):Cu+2H2SO4(浓) CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。则A应该属于___________ (用字母代号填写)
A.酸 B.非电解质 C.盐 D. 酸性氧化物
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是___________ ,
(3)一定量的铜片与200mL18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为___________ mol,
(4)将反应后所得到的CuSO4溶液与足量Ba(OH)2溶液充分反应的离子方程式是___________
 CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O试通过计算和推理完成下面的问题:(1)A物质可以导致酸雨的形成。则A应该属于
A.酸 B.非电解质 C.盐 D. 酸性氧化物
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是
(3)一定量的铜片与200mL18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的CuSO4的物质的量为
(4)将反应后所得到的CuSO4溶液与足量Ba(OH)2溶液充分反应的离子方程式是
更新时间:2020-12-19 16:45:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】有以下几种物质:① ②稀盐酸 ③
②稀盐酸 ③ ④醋酸 ⑤熔融的氯化钠 ⑥
④醋酸 ⑤熔融的氯化钠 ⑥ 固体 ⑦
固体 ⑦ ⑧
⑧ ⑨酒精 ⑩
⑨酒精 ⑩ ,按要求进行分类
,按要求进行分类
(1)属于酸性氧化物的是_______ (填序号,下同)
(2)属于电解质的是_______ 。
(3)属于电解质又能导电的是_______ 。
(4)属于混合物的是_______ 。
 ②稀盐酸 ③
②稀盐酸 ③ ④醋酸 ⑤熔融的氯化钠 ⑥
④醋酸 ⑤熔融的氯化钠 ⑥ 固体 ⑦
固体 ⑦ ⑧
⑧ ⑨酒精 ⑩
⑨酒精 ⑩ ,按要求进行分类
,按要求进行分类(1)属于酸性氧化物的是
(2)属于电解质的是
(3)属于电解质又能导电的是
(4)属于混合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)下列各组物质均由分子组成的是 ________
①金刚石、氨气、氧气
②二氧化碳、二氧化硅、二氧化硫
③空气、冰、碘蒸气
④液氯、液氨、熔化的食盐
(2)直接由原子构成的是________ .
①二氧化硅②二氧化碳③钠 ④金刚石⑤单晶硅⑥白磷⑦硫⑧氨气⑨溴化氢⑩碘蒸气
①金刚石、氨气、氧气
②二氧化碳、二氧化硅、二氧化硫
③空气、冰、碘蒸气
④液氯、液氨、熔化的食盐
(2)直接由原子构成的是
①二氧化硅②二氧化碳③钠 ④金刚石⑤单晶硅⑥白磷⑦硫⑧氨气⑨溴化氢⑩碘蒸气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是_______ (填序号,下同);属于盐类的是_______ ;相互间能发生反应的是_______ 。
(2)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒的效果更好的_______ (填物质名称),该反应的离子方程式是1ClO-+1CO2+1H2O=_______+_______。_______
(1)厨房中的调味品①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中具有碱性的是
(2)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒的效果更好的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为__________ ,原子总数之比为__________ ,密度之比为__________ 。
(2)在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,所含分子数最多的是________ ,含原子数最多的是________ ,质量最大的是________ 。
(2)在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,所含分子数最多的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】淀粉是人类膳食中糖类的主要来源,在体内被酶水解为葡萄糖(C6H12O6)供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
(1)27g葡萄糖中含碳原子的物质的量为__ ,含氢原子数为__ 。
(2)0.5mol葡萄糖在人体内完全转化为二氧化碳的体积(标准状况)是___ 。
(3)该病人血清葡萄糖的物质的量浓度为___ 。
(4)把淀粉溶液溶于沸水中,制成淀粉胶体。鉴别葡萄糖溶液和淀粉胶体的方法是___ ,提纯、精制胶体的方法是___ 。
| ××医院化验单 | |||
| 姓名:××× | |||
| 项目 | 测定值 | 单位 | 参考范围 |
| 丙氨酸氨基转氨酶ALT | 35 | U/L | 9~50 |
| 血清葡萄糖GLU | 216↑ | mg/dl | 60~110 |
| 甘油三酯TG | 217↑ | mg/dl | 50~200 |
| 总胆固醇TCH | 179 | mg/dl | 150~220 |
| 注:1dl=100mL | |||
(1)27g葡萄糖中含碳原子的物质的量为
(2)0.5mol葡萄糖在人体内完全转化为二氧化碳的体积(标准状况)是
(3)该病人血清葡萄糖的物质的量浓度为
(4)把淀粉溶液溶于沸水中,制成淀粉胶体。鉴别葡萄糖溶液和淀粉胶体的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用相关知识填空。
(1)标准状况下11.2LNH3中含___________ 个氨分子,含___________ mol氢原子。
(2)等质量的SO2和SO3物质的量之比是___________ :所含的氧原子个数之比是___________ 。
(3)4.8gCH4中所含氢原子数与___________ g水所含氢原子数相等。
(4)已知A是一种金属,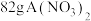 中含有
中含有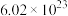 个硝酸根离子,则该硝酸盐的摩尔质量为
个硝酸根离子,则该硝酸盐的摩尔质量为___________ 。
(5)标况下,一定量的N2与22.4LCO所含电子的物质的量相等,则N2的质量是___________ 。
(6)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为___________ 。若此时压强为101kPa,则温度___________ 0℃ (填“高于”“低于”或“等于”)。
(7)有一种由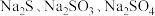 组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为
组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为___________ 。
(1)标准状况下11.2LNH3中含
(2)等质量的SO2和SO3物质的量之比是
(3)4.8gCH4中所含氢原子数与
(4)已知A是一种金属,
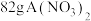 中含有
中含有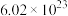 个硝酸根离子,则该硝酸盐的摩尔质量为
个硝酸根离子,则该硝酸盐的摩尔质量为(5)标况下,一定量的N2与22.4LCO所含电子的物质的量相等,则N2的质量是
(6)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为
(7)有一种由
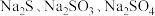 组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为
组成的混合物,经测定含硫25.6%,则混合物中含氧的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下列为元素周期表中的一部分,用化学用语回答下列问题。
(1)③的原子结构示意图为___________ ;
(2)11种元素中,化学性质最不活泼的是___________ ,原子半径最小的是___________ ,金属性最强的是___________ ,非金属性最强的是___________ 。
(3)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(4)②③④中形成的简单离子半径由大到小的顺序是___________ 。
(5)元素⑦的简单氢化物电子式为___________ 。
(6)①和⑨两元素形成化合物中化学键的类型为___________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为___________ 。
(7)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(8)⑧⑨⑪三种元素形成的气态氢化物中,最稳定的是___________ ,沸点___________ (填化学式)更高,原因是___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)③的原子结构示意图为
(2)11种元素中,化学性质最不活泼的是
(3)①②⑤中,最高价氧化物的水化物,碱性最强的是
(4)②③④中形成的简单离子半径由大到小的顺序是
(5)元素⑦的简单氢化物电子式为
(6)①和⑨两元素形成化合物中化学键的类型为
(7)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(8)⑧⑨⑪三种元素形成的气态氢化物中,最稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】描述下列反应的现象并写出反应的离子方程式。
(1)向FeCl3溶液中滴加NaOH溶液,现象:__________________ ,离子方程式:____________________
(2)向NaHCO3溶液中滴加稀H2SO4,现象:__________________ ,离子方程式:__________________
(3)稀HNO3和Ba(OH)2溶液混合,现象:__________________ ,离子方程式:____________________
(4)比较:上述三个离子反应发生的条件的不同点是______________________ ;相同点是________________
(1)向FeCl3溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀H2SO4,现象:
(3)稀HNO3和Ba(OH)2溶液混合,现象:
(4)比较:上述三个离子反应发生的条件的不同点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】人体必需的一些元素在周期表中的分布情况如下:___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
(4)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________ 。

(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(4)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是
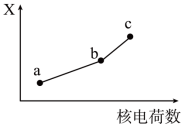
| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硝基苯(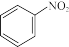 )是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。
)是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。
(1)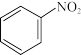 与Fe、盐酸反应生成可生物降解的苯胺(
与Fe、盐酸反应生成可生物降解的苯胺(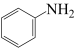 )、
)、 和
和 。
。
①理论上,1mol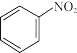 转化为
转化为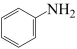 转移的电子的物质的量为
转移的电子的物质的量为_______ 。
②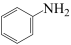 在水中的溶解度大于
在水中的溶解度大于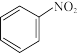 的原的原因是
的原的原因是_______ 。
(2)在酸性条件下,铁炭混合物处理污水中硝基苯时,硝基苯转化过程如下:
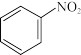

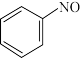

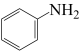
①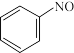 转化为
转化为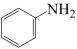 的电极反应式:
的电极反应式:_______ 。
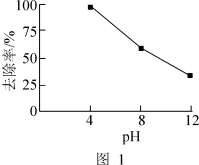
②在其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图1所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(3)向含 和苯胺(
和苯胺(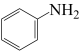 )的酸性溶液中加入双氧水,发生如下反应:
)的酸性溶液中加入双氧水,发生如下反应: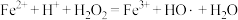
①HO·具有强氧化性,能将溶液中的苯胺氧化成 和
和 。该反应的离子方程式为
。该反应的离子方程式为_______ 。
② 也具有氧化性,设计验证苯胺是被HO·氧化而不是被
也具有氧化性,设计验证苯胺是被HO·氧化而不是被 氧化的实验方案:
氧化的实验方案:_______ 。
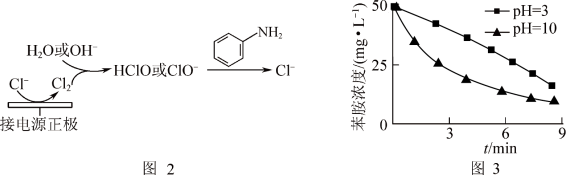
(4)利用电解原理也可以间接氧化处理含苯胺的污水,其原理如图2所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图3所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。(已知: 随着pH减小,氧化性增强)
随着pH减小,氧化性增强)
 )是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。
)是一种化学稳定性好、毒性高、难以生物降解的污染物。用化学方法降解水中硝基苯已成为污水处理领域的重要研究方向。(1)
 与Fe、盐酸反应生成可生物降解的苯胺(
与Fe、盐酸反应生成可生物降解的苯胺( )、
)、 和
和 。
。①理论上,1mol
 转化为
转化为 转移的电子的物质的量为
转移的电子的物质的量为②
 在水中的溶解度大于
在水中的溶解度大于 的原的原因是
的原的原因是(2)在酸性条件下,铁炭混合物处理污水中硝基苯时,硝基苯转化过程如下:





①
 转化为
转化为 的电极反应式:
的电极反应式:②在其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图1所示。pH越大,硝基苯的去除率越低的原因是

(3)向含
 和苯胺(
和苯胺( )的酸性溶液中加入双氧水,发生如下反应:
)的酸性溶液中加入双氧水,发生如下反应: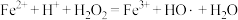
①HO·具有强氧化性,能将溶液中的苯胺氧化成
 和
和 。该反应的离子方程式为
。该反应的离子方程式为②
 也具有氧化性,设计验证苯胺是被HO·氧化而不是被
也具有氧化性,设计验证苯胺是被HO·氧化而不是被 氧化的实验方案:
氧化的实验方案:(4)利用电解原理也可以间接氧化处理含苯胺的污水,其原理如图2所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图3所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是
 随着pH减小,氧化性增强)
随着pH减小,氧化性增强)
您最近一年使用:0次
【推荐2】高铁酸钠(NaFeO4) 是一种新型绿色消毒剂,主要用于饮用水处理。工业上一种在碱性条件下制备高铁酸钠的方法的化学原理可用离子方程式表示为: ClO-+
ClO-+ Fe3++
Fe3++ _______=
_______= FeO
FeO +
+ _______+
_______+ H2O
H2O
(1)补全并配平该离子方程式,并用双线桥标注反应过程中的电子转移情况。________
(2)该反应中被还原的元素是_______ (填元素名称),还原剂是_______ (填离子符号),该条件下的氧化性 FeO
_______ ClO- (填“>”或“<”)。
(3)若用NaClO作为其中一种原料,当反应中有2 mol电子转移时,需要NaClO的质量为_______ 。
 ClO-+
ClO-+ Fe3++
Fe3++ _______=
_______= FeO
FeO +
+ _______+
_______+ H2O
H2O(1)补全并配平该离子方程式,并用双线桥标注反应过程中的电子转移情况。
(2)该反应中被还原的元素是

(3)若用NaClO作为其中一种原料,当反应中有2 mol电子转移时,需要NaClO的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下下列反应均可用于实验室制备氯气:
①MnO2+4HCl (浓) MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。
②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
回答下列问题:
(1)请将反应①改写为离子方程式:____________ 。
(2)用双线桥标出反应②的电子转移方向和数目:__________ 。
(3)用单线桥标出反应③的电子转移方向和数目:___________
(4)比较反应①②中氧化剂的氧化性强弱____________ 。
(5)上述反应中浓盐酸显示出来的性质是_________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)若反应①中有17.4 g纯MnO2被还原,则反应①中被氧化的氯化氢的质量为______ 。
(7)当反应①中生成3.01×1023个氯气分子时,则转移的电子数为_____ 。
(8)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式__________ ,其反应中被氧化的原子与被还原的原子个数之比为_____ 。
①MnO2+4HCl (浓)
 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
回答下列问题:
(1)请将反应①改写为离子方程式:
(2)用双线桥标出反应②的电子转移方向和数目:
(3)用单线桥标出反应③的电子转移方向和数目:
(4)比较反应①②中氧化剂的氧化性强弱
(5)上述反应中浓盐酸显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)若反应①中有17.4 g纯MnO2被还原,则反应①中被氧化的氯化氢的质量为
(7)当反应①中生成3.01×1023个氯气分子时,则转移的电子数为
(8)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
您最近一年使用:0次



