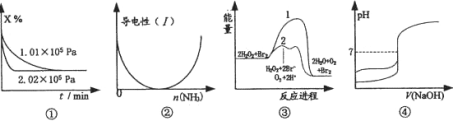
若用AG表示溶液的酸度,其表达式为:AG=lg[ ]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL 0.10 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL 0.10 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
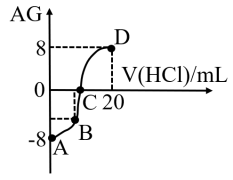
 ]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL 0.10 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.10mol/L的盐酸溶液滴定10 mL 0.10 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是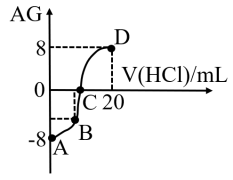
| A.该滴定过程可选择酚酞作为指示剂 |
| B.C点加入盐酸的体积小于10mL |
| C.若B点加入的盐酸溶液体积为5mL,所得溶液中:c(M+)+c(H+)=c(MOH)+2c(OH−) |
| D.滴定过程中从A点到D点溶液中水的电离程度逐渐增大 |
更新时间:2020-12-23 20:05:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学在实验报告中记录了下列数据,其中正确的是
A.用 量筒量取 量筒量取 盐酸 盐酸 |
B.用 试纸测出某溶液 试纸测出某溶液 为 为 |
C.可用 酸式滴定管量取 酸式滴定管量取 溶液 溶液 |
D.用酸式滴定管测出消耗盐酸的体积为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列装置不能正确完成相关实验是( )
| A | B | C | D | |
| 装置 | 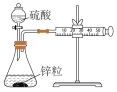 | 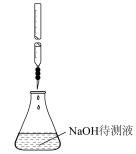 | 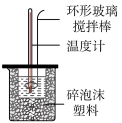 |  |
| 实验 | 结合秒表测量锌与 硫酸的反应速率 | 用标准盐酸溶液测 定NaOH溶液的浓度 | 测定中和热 | 铁的吸氧腐蚀实验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向 20 mL 0.1 mol·L-1CH3COOH溶液中滴加0.1 mol·L-1NaOH溶液。下列说法正确的是
| A.当溶液的pH=7时:c(Na+) = c(CH3COO-) + c(CH3COOH) |
| B.当加入10 mL 0.1 mol·L-1NaOH溶液时:c(CH3COO-) +2 c(OH-) = c(CH3COOH) + 2c(H+) |
| C.当加入20 mL 0.1 mol·L-1NaOH溶液时:c(Na+) >c(OH-) >c(CH3COO-) > c(H+) |
| D.滴定过程中可能有:c(CH3COOH) >c(H+) >c(CH3COO-) >c(Na+) >c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列对化学反应原理图象的分析及说法有明显错误的是
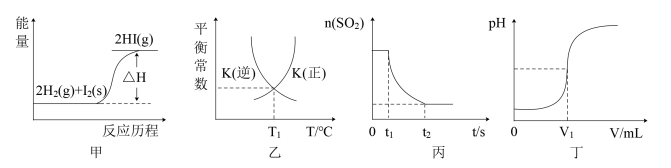

| A.图甲中的△H可利用H2、I2、HI等分子中共价键的键能计算 |
| B.图乙中表示的化学反应属于高温自发反应,当温度为T1时,K(正)=1 |
C.2SO2(g)+O2(g) 2SO3(g)达平衡后,图丙中t1时改变的条件可能是增大压强 2SO3(g)达平衡后,图丙中t1时改变的条件可能是增大压强 |
| D.图丁中,用NaOH溶液滴定盐酸,酚酞作指示剂,滴定终点时溶液pH>7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现用0.2000 mol/L的NaOH溶液滴定未知浓度的醋酸溶液,取25.00mL 醋酸溶液于锥形瓶中,实验结束后,测得消耗NaOH溶液的体积为15.60mL,则下列说法正确的是


| A.滴定前,盛装醋酸溶液的锥形瓶需先用水洗,再用醋酸溶液润洗 |
| B.盛装NaOH溶液的仪器如图所示 |
| C.应使用酚酞做指示剂,当溶液由无色变为粉红色,且半分钟不褪色,即达到滴定终点 |
| D.经计算,醋酸溶液的浓度为0.3205mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。用0.10mol·L-1NaOH溶液滴定0.10mol·L-1H2C2O4(草酸)溶液的滴定曲线如图所示。下列说法不正确的是

| A.H2C2O4属于二元弱酸 |
| B.若用NaOH标准溶液滴定NaHC2O4溶液,可用酚酞作指示剂 |
| C.图中①处: c(Na+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) |
| D.图中②处:c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】为了更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念:AG=lg 。常温下,用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1HCN溶液,溶液的酸度(AG)随滴入的NaOH溶液体积的变化如图所示(滴定过程中温度的变化忽略不计),已知100.8≈6.3,下列说法正确的是
。常温下,用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1HCN溶液,溶液的酸度(AG)随滴入的NaOH溶液体积的变化如图所示(滴定过程中温度的变化忽略不计),已知100.8≈6.3,下列说法正确的是

 。常温下,用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1HCN溶液,溶液的酸度(AG)随滴入的NaOH溶液体积的变化如图所示(滴定过程中温度的变化忽略不计),已知100.8≈6.3,下列说法正确的是
。常温下,用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1HCN溶液,溶液的酸度(AG)随滴入的NaOH溶液体积的变化如图所示(滴定过程中温度的变化忽略不计),已知100.8≈6.3,下列说法正确的是
A.滴定过程中 逐渐增大 逐渐增大 |
| B.常温下,HCN的电离常数Ka≈6.3×10-10 |
| C.滴定过程中水电离出c(H+)先减小后增大 |
| D.当V=10mL时,溶液中存在c(H+)+c(HCN)=c(OH-)+c(CN-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积VHCl的变化关系如图所示。已知B+的分布系数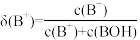 。下列叙述正确的是
。下列叙述正确的是

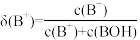 。下列叙述正确的是
。下列叙述正确的是
| A.BOH的电离常数Kb=1.0× 10-6 |
| B.滴定时,可以选择甲基橙作指示剂 |
| C.滴定过程中,水的电离程度: n<m<p |
| D.n点溶液中,粒子浓度大小为c(Cl-)>c(B+)> c(BOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:
随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数: ]
]

下列叙述正确的是
 随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:
随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数: ]
]
下列叙述正确的是
A.曲线①代表 ,曲线②代表 ,曲线②代表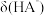 |
B.滴定终点时,溶液中 |
| C.HA−的电离常数Ka=1.0×10−5 |
| D.H2A溶液的浓度为0.1000 mol·L−1 |
您最近一年使用:0次