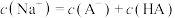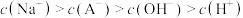电解质溶液的电导率与离子浓度成正比。用0.100 mol·L-1的NaOH溶液滴定体积均为10.00 mL、浓度均为0.100 mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
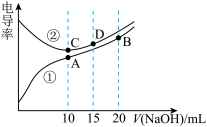

| A.在相同温度下,A、B、C三点溶液中水的电离程度:B<A=C |
| B.D点溶液中:c(Cl-)=2c(OH-)-2c(H+) |
| C.B点溶液中:c(CH3COOH)+c(CH3COO-)=c(Na+) |
| D.A点溶液中:c(CH3COOH)+c(Na+)<0.05 mol·L-1 |
更新时间:2021-01-14 20:06:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】中和滴定的误差要求小于0.1%,若用20.00 mL0.2000mol·L-1盐酸滴定20mL0.2000mol·L-1NaOH溶液,则中和滴定曲线中发生突变时的pH范围是(lg2=0.3)( )
| A.4.3~9.7 | B.3.7~10.3 | C.4.0~10.0 | D.无法确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.常温下,将pH =10的氨水稀释,溶液中所有离子浓度都减小 |
| B.常温下,反应2A (s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0 |
| C.用NaOH标准溶液滴定未知浓度的CH3COOH溶液时,使用甲基橙作指示剂 |
| D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关电解质溶液的说法正确的是
| A.25℃时,pH=3的H2SO4溶液和pH=10的NaOH溶液恰好完全中和,消耗酸和碱的体积比为1:10 |
B.将CH3COONa溶液从20 ℃升温至30 ℃,溶液中 增大 增大 |
C.K2CO3、CH3COOK 和KCl 的混合溶液中,一定满足:c(K+)+c(H+)=2c(CO )+c(HCO )+c(HCO )+c(OH-)+c(CH3COO-) )+c(OH-)+c(CH3COO-) |
| D.升高温度,水的电离平衡正向移动,故c(H+)增大, Kw增大,pH也随之增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知常温下CH3COOH的电离平衡常数为Ka,常温下,向20mL 0.1 mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是
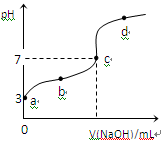

| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol·L-1 |
| B.b点表示的溶液c(CH3COO-)> c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中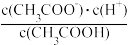 相等 相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.氨气、二氧化硫、二氧化碳的水溶液均可以导电,故它们都为电解质 |
B.向氨水中加入少量固体 , , 的电离平衡逆向移动, 的电离平衡逆向移动, 增大 增大 |
C.将浓度为 的 的 溶液加水稀释,则 溶液加水稀释,则 的值减小,电离平衡常数不变 的值减小,电离平衡常数不变 |
D.向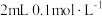 的 的 溶液中滴加 溶液中滴加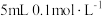 的 的 溶液至生成白色沉淀后向其中滴加4滴 溶液至生成白色沉淀后向其中滴加4滴 的 的 溶液,生成红褐色沉淀,可以说明 溶液,生成红褐色沉淀,可以说明 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,向20 mL b mol/LNaOH溶液中滴加0.1 mol/L HA溶液,混合溶液中水电离的c(OH-)与HA溶液体积(V)的关系如图,下列有关说法错误的是


| A.根据图可求出b=0.1 |
| B.B、D点溶液都为中性 |
| C.酸溶液的体积:V=20 |
D.25℃时,对E点溶液加水稀释, 一定不变 一定不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知HClO的Ka=2.98 ×10-8,CH3COOH的Ka=1.75 ×10-5,下列有关说法正确的是
| A.在pH=2的醋酸溶液中加入少量0.01 mol·L-1的稀盐酸,溶液的pH会变小 |
| B.等浓度等体积的CH3COONa和NaClO溶液,前者所含离子总数比后者大 |
| C.100 mL pH=2的新制氯水中:n(OH- )+ n(ClO- ) + n(HClO)=0.001 mol |
| D.将Cl2通入NaOH溶液中,若溶液呈中性,则溶液中存在6种微粒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,将2种一元酸HX和HY分别和NaOH溶液等体积混合,实验数据如下:下列说法正确的是
| 组别 | 混合前 | 混合后 | |
| 甲 | c(HX)=0.1mol•L-1 | c(NaOH)=0.1mol•L-1 | pH=9 |
| 乙 | c(HY)=0.1mol•L-1 | c(NaOH)=0.1mol•L-1 | pH=7 |
| A.HY为弱酸 | B.HX溶液的pH<1 |
| C.甲的混合液中c(X-)=c(Na+) | D.乙的混合液中c(Na+)=c(Y-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,在实验室中用0.1 mol·L-1的盐酸滴定10 mL 0.1 mol·L-1的ROH溶液,滴定曲线如图所示。下列有关叙述错误的是


| A.Kb(ROH)的数量级为10-5 |
| B.点②对应溶液中:c(R+)+2c(H+)=c(ROH)+2c(OH-) |
| C.水的电离程度:①<③<④ |
D.滴加盐酸的过程中 保持不变 保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,浓度均为0.1 mol·L-1的下列四种盐溶液,其pH测定如表所示,下列说法正确的是( )
| 序号 | ① | ② | ③ | ④ |
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
| A.四种溶液中,水的电离程度:①>②>④>③ |
| B.Na2CO3和NaHCO3溶液中,粒子种类不相同 |
| C.将等浓度的CH3COOH和HClO溶液比较,pH小的是HClO |
D.Na2CO3和NaHCO3溶液中分别加入NaOH固体,恢复到原温度,c( )均增大 )均增大 |
您最近一年使用:0次

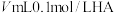 溶液中滴入
溶液中滴入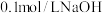 溶液,溶液中由水电离出的氢氧根离子浓度的负对数
溶液,溶液中由水电离出的氢氧根离子浓度的负对数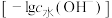 与所加
与所加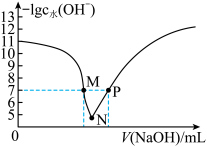
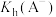 约为
约为