某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如图所示:
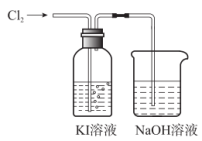
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是_______ ;
(2)KI溶液变为黄色说明氯气具有_______ 性,该反应的离子方程式是_______ ;
(3)已知 ,
, 、
、 在水中均呈黄色。为确定黄色溶液的成分,进行以下实验:
在水中均呈黄色。为确定黄色溶液的成分,进行以下实验:
①实验b的目的是_______ ;
②根据实验a可知,水层中含有的粒子有_______ ;
③用化学平衡原理解释实验a中水溶液颜色变浅的原因:_______ ;
(4)通入氯气,溶液由黄色变为无色,是因为氯气将 氧化。已知
氧化。已知 可氧化
可氧化 ,该反应的离子方程式是
,该反应的离子方程式是_______ ;
(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为_______ ;
(6)溶液最终变为浅黄绿色的原因是_______ 。

通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是
(2)KI溶液变为黄色说明氯气具有
(3)已知
 ,
, 、
、 在水中均呈黄色。为确定黄色溶液的成分,进行以下实验:
在水中均呈黄色。为确定黄色溶液的成分,进行以下实验:| 操作 | 实验现象 | |
| a | 取2~3mL黄色溶液,加入足量 ,振荡静置 ,振荡静置 |  层呈紫红色,水层显浅黄色 层呈紫红色,水层显浅黄色 |
| b | 取2~3mL饱和碘水,加入足量 ,振荡静置 ,振荡静置 |  层呈紫红色,水层几近无色 层呈紫红色,水层几近无色 |
②根据实验a可知,水层中含有的粒子有
③用化学平衡原理解释实验a中水溶液颜色变浅的原因:
(4)通入氯气,溶液由黄色变为无色,是因为氯气将
 氧化。已知
氧化。已知 可氧化
可氧化 ,该反应的离子方程式是
,该反应的离子方程式是(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为
(6)溶液最终变为浅黄绿色的原因是
21-22高三上·北京通州·期末 查看更多[2]
更新时间:2021-01-24 15:11:15
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下图所涉及的物质均为中学化学中的常见物质,其中C为空气中能够支持燃烧的气体单质、D为黄绿色气体单质、E为日常生活中最常见的金属单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。
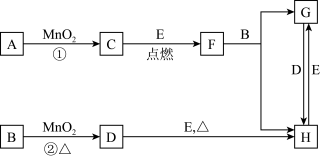
(1)写出有关物质的名称:B_______ ,F_______ 。
(2)若反应①是在加热条件下进行,则A是______ (填化学式);
若反应①是在常温条件下进行,则A是_____ (填化学式)。
(3)写出B与MnO2共热获得D的离子方程式_______________________ 。

(1)写出有关物质的名称:B
(2)若反应①是在加热条件下进行,则A是
若反应①是在常温条件下进行,则A是
(3)写出B与MnO2共热获得D的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:
①K2FeO4为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
②K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用。

(1)K2FeO4中铁元素的化合价为___________ 。
(2)A为氯气发生装置。发生反应的方程式为:KMnO4+HCl=MnCl2+Cl2↑+KCl+H2O,配平上述方程式______ ,并用单线桥分析该氧化还原反应的电子转移情况。
(3)装置B是为了除去Cl2中混有的HCl杂质,将除杂装置B补充完整并标明所用试剂_____ 。
(4)D中盛放的是___________ 溶液。
(5)C中得到紫色固体K2FeO4和溶液,请判断氧化性Cl2___________ K2FeO4(填“>”“=”或“<”)。C中通Cl2制得K2FeO4的化学方程式_______ ,同时还发生了另一个反应的离子方程式是_____ 。
(6)下列关于K2FeO4的说法中,正确的是___________ 。
A.是强氧化性的盐
B.固体保存需要防潮
C.其净水优点有:作用快、安全性好、无异味
(7)将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+( )H2O=( )Fe(OH)3(胶体)+( )_______+( )KOH,_________ 。
资料:
①K2FeO4为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
②K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用。

(1)K2FeO4中铁元素的化合价为
(2)A为氯气发生装置。发生反应的方程式为:KMnO4+HCl=MnCl2+Cl2↑+KCl+H2O,配平上述方程式
(3)装置B是为了除去Cl2中混有的HCl杂质,将除杂装置B补充完整并标明所用试剂
(4)D中盛放的是
(5)C中得到紫色固体K2FeO4和溶液,请判断氧化性Cl2
(6)下列关于K2FeO4的说法中,正确的是
A.是强氧化性的盐
B.固体保存需要防潮
C.其净水优点有:作用快、安全性好、无异味
(7)将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+( )H2O=( )Fe(OH)3(胶体)+( )_______+( )KOH,
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】水煤气变换[CO(g)+H2O(g)
 CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
标注。
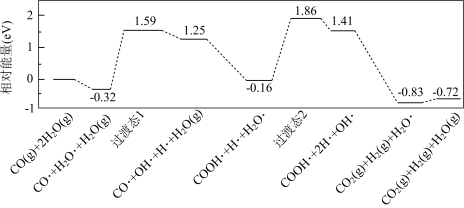
该历程中决速步骤的化学方程式为__ (方程式两边若有相同物料不用约简)。水煤气变换反应的热化学方程式为__ 。
(2)t1℃时,密闭容器中,通入一定量的CO和H2O,发生水煤气变换反应,容器中各物质浓度(单位:mol·L-1)变化如下表所示:
①一定处于平衡状态的时间段为__ 。
②5~6min时间段内,平衡移动方向为__ (填“向左移动”或“向右移动”),根据表中数据判断,平衡移动的原因是__ (填字母编号)。
a.增加了H2O(g)的量 b.增加氢气浓度 c.使用催化剂 d.降低温度
③t2℃时(t2>t1),在相同条件下发生上述反应,达平衡时,CO浓度__ c1(填“>”“<”或“=”)。
(3)已知反应Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:

①该反应是__ (填“吸热”或“放热”)反应。
②若T1时水煤气变换反应的平衡常数等于0.5,则T1时FeO(s)+H2(g) Fe(s)+H2O(g)的平衡常数为
Fe(s)+H2O(g)的平衡常数为__ 。
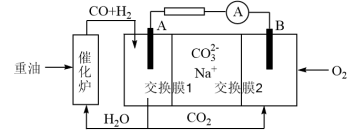
(4)水煤气可做燃料电池的燃料。一种熔融碳酸盐燃料电池的工作原理如图所示。电极A上H2参与的电极反应为__ 。假设催化炉产生的CO与H2物质的量之比为1︰2。电极A处产生的CO2有部分参与循环利用,其利用率为__ 。

 CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:(1)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用
 标注。
标注。
该历程中决速步骤的化学方程式为
(2)t1℃时,密闭容器中,通入一定量的CO和H2O,发生水煤气变换反应,容器中各物质浓度(单位:mol·L-1)变化如下表所示:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②5~6min时间段内,平衡移动方向为
a.增加了H2O(g)的量 b.增加氢气浓度 c.使用催化剂 d.降低温度
③t2℃时(t2>t1),在相同条件下发生上述反应,达平衡时,CO浓度
(3)已知反应Fe(s)+CO2(g)
 FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
①该反应是
②若T1时水煤气变换反应的平衡常数等于0.5,则T1时FeO(s)+H2(g)
 Fe(s)+H2O(g)的平衡常数为
Fe(s)+H2O(g)的平衡常数为(4)水煤气可做燃料电池的燃料。一种熔融碳酸盐燃料电池的工作原理如图所示。电极A上H2参与的电极反应为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】我国冶铅工艺迅猛发展,底吹炉烟灰中除含有主金属铅外,还含有锌、镉(Cd)等有价金属元素,一种对该烟灰中有价金属综合回收工艺研究如下:

已知:Ⅰ.
①As元素以砷酸盐( )形式存在;
)形式存在;
②Pb元素主要以PbO和PbSO4形式存在,不溶于水;
③Cd元素主要以CdSO4形式存在,CdSO4易溶于水。
Ⅱ.水浸液初始pH=2~3;滤渣①返回冶铅系统;滤渣②主要成分为FeAsO4。
回答下列问题:
(1)为提高“水浸”效率,可以采取的措施有_______ (任写一条)。
(2)为提高铅和镉的回收率,需综合分析浸出率、渣含金属、渣率。
根据以上实验数据选择合适的液固比和温度:_______ ,理由:_______ 。
(3)“中和除砷”阶段主要反应的离子方程式为_______ 。该工序最终需加入试剂①调节溶液pH=5,下列最合适的是_______ (填序号)。
A.NaOH B.NH3·H2O C.Zn2O D.H2SO4
(4)“电解”过程中阴极的电极反应式为_______ 。

已知:Ⅰ.
| 底吹炉含镉烟灰的主要化学成分 |  |  |  |  |  |  |
| 质量分数/% | 37.40 | 15.88 | 2.51 | 0.15 | 0.28 | 0.15 |
 )形式存在;
)形式存在;②Pb元素主要以PbO和PbSO4形式存在,不溶于水;
③Cd元素主要以CdSO4形式存在,CdSO4易溶于水。
Ⅱ.水浸液初始pH=2~3;滤渣①返回冶铅系统;滤渣②主要成分为FeAsO4。
回答下列问题:
(1)为提高“水浸”效率,可以采取的措施有
(2)为提高铅和镉的回收率,需综合分析浸出率、渣含金属、渣率。
| 温度/℃ | 浸出率/% | 渣含金属 | 渣率/℃ | |||
 |  |  |  |  | ||
| 25 | 86.06 | 65.48 | 55.48 | 3.27 | 1.28 | 67.69 |
| 45 | 84.19 | 63.95 | 54.63 | 3.69 | 1.33 | 68.04 |
| 65 | 85.51 | 62.45 | 55.63 | 3.37 | 1.38 | 68.30 |
| 85 | 84.15 | 65.08 | 54.70 | 3.82 | 1.33 | 65.90 |
| 液固比 | 浸出率/% | 渣含金属 | 渣率/℃ | |||
 |  |  |  |  | ||
| 1:1 | 75.22 | 54.65 | 51.26 | 5.29 | 1.53 | 74.39 |
| 2:1 | 80.59 | 58.62 | 53.98 | 4.28 | 1.47 | 70.66 |
| 3:1 | 85.51 | 62.45 | 55.63 | 3.37 | 1.38 | 68.30 |
| 4:1 | 86.82 | 65.02 | 57.06 | 3.14 | 1.32 | 66.52 |
(3)“中和除砷”阶段主要反应的离子方程式为
A.NaOH B.NH3·H2O C.Zn2O D.H2SO4
(4)“电解”过程中阴极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】甲烷水蒸气重整反应是工业制备氢气的重要方式,在催化剂(如镍)表面发生的主要反应有:
①
 kJ⋅mol-1
kJ⋅mol-1
②

副反应: ,
,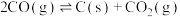 ,
,
Ⅰ.已知: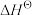 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其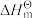 为零。
为零。
例如C(石墨)
 kJ·mol-1,则
kJ·mol-1,则 的标准生成焓为-393.5 kJ⋅mol-1。
的标准生成焓为-393.5 kJ⋅mol-1。
(1)
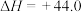 kJ⋅mol-1,结合表中数据计算反应
kJ⋅mol-1,结合表中数据计算反应
___________ 。
(2)在镍催化剂表面甲烷和水蒸气发生反应,最后生成CO、 和
和 ,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
a. ;
;
b.___________ ;
c. ;
;
d.___________ ;
e.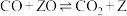
Ⅱ.在一体积可变的密闭容器中,投入一定量的 和
和 发生甲烷水蒸气重整反应。
发生甲烷水蒸气重整反应。
(3)下列有关说法正确的是___________。
(4)维持压强100 kPa,平衡时 、
、 、CO、
、CO、 的体积分数分别为a、b、c、d,反应①的平衡常数
的体积分数分别为a、b、c、d,反应①的平衡常数
___________  (用含字母的式子表示。
(用含字母的式子表示。 是以分压表示的平衡常数,分压=总压×体积分数)。
是以分压表示的平衡常数,分压=总压×体积分数)。
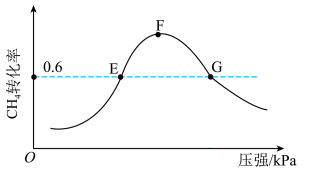
(5)500℃时,反应相同时间后测得 的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)___________ c(G)(填“>”“<”或“=”)。
(6)通过甲烷水蒸气重整反应的平衡含量计算,以及析碳条件的判断,该转化需适当增大水碳比[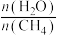 ],请分析可能的原因:
],请分析可能的原因:___________ 。
①

 kJ⋅mol-1
kJ⋅mol-1②


副反应:
 ,
,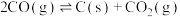 ,
,
Ⅰ.已知:
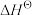 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其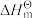 为零。
为零。例如C(石墨)

 kJ·mol-1,则
kJ·mol-1,则 的标准生成焓为-393.5 kJ⋅mol-1。
的标准生成焓为-393.5 kJ⋅mol-1。| 物质 |  |  | CO |
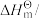 /kJ⋅mol-1 /kJ⋅mol-1 | -285.8 | -393.5 | -110.5 |

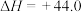 kJ⋅mol-1,结合表中数据计算反应
kJ⋅mol-1,结合表中数据计算反应
(2)在镍催化剂表面甲烷和水蒸气发生反应,最后生成CO、
 和
和 ,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。a.
 ;
; b.
c.
 ;
;d.
e.
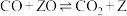
Ⅱ.在一体积可变的密闭容器中,投入一定量的
 和
和 发生甲烷水蒸气重整反应。
发生甲烷水蒸气重整反应。(3)下列有关说法正确的是___________。
A. 浓度不变,说明体系已达平衡状态 浓度不变,说明体系已达平衡状态 |
| B.反应②前后气体物质的量不变,所以此反应熵变为0 |
C.在催化剂表面, 、 、 分子中的化学键被削弱 分子中的化学键被削弱 |
D.在体系中通入适量的 ,有利于减少积碳,从而有利于反应进行 ,有利于减少积碳,从而有利于反应进行 |
 、
、 、CO、
、CO、 的体积分数分别为a、b、c、d,反应①的平衡常数
的体积分数分别为a、b、c、d,反应①的平衡常数
 (用含字母的式子表示。
(用含字母的式子表示。 是以分压表示的平衡常数,分压=总压×体积分数)。
是以分压表示的平衡常数,分压=总压×体积分数)。(5)500℃时,反应相同时间后测得
 的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
(6)通过甲烷水蒸气重整反应的平衡含量计算,以及析碳条件的判断,该转化需适当增大水碳比[
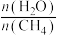 ],请分析可能的原因:
],请分析可能的原因:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】已知 在
在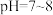 时溶解度最小。某工厂利用钒铬渣提取液(主要成分为
时溶解度最小。某工厂利用钒铬渣提取液(主要成分为 和
和 )制备
)制备 和
和 晶体,流程如下:
晶体,流程如下:
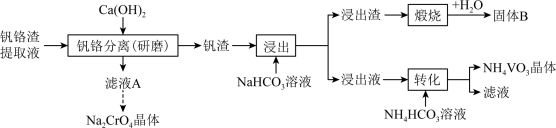
不同温度下相关物质的溶解度
(1)关于“钒铬分离”过程,下列说法正确的是_______。
(2)从滤液A中获取 晶体时,应采用的结晶方法为
晶体时,应采用的结晶方法为_______ ;残留的含铬废水不能直接排放,处理时需要经过“酸化→还原→沉降”三个步骤用 溶液还原时,还原产物为
溶液还原时,还原产物为 ,则反应的离子方程式
,则反应的离子方程式_______ 。
(3)钒渣成份是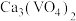 ,“浸出”过程中生成
,“浸出”过程中生成 的离子方程式为
的离子方程式为_______ 。
(4)“转化”过程中选用 溶液不选用
溶液不选用 溶液的可能原因为
溶液的可能原因为_______ 。(写一条原因即可)
(5)该流程中可循环利用的物质有_______ 。
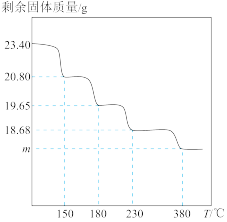
(6)研究表明 固体(固体的组成用
固体(固体的组成用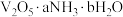 表示)热分解得到
表示)热分解得到 的过程可分为四步,每一步产生
的过程可分为四步,每一步产生 和
和 的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取
的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取 固体进行热重分析,剩余固体质量与温度关系如图,
固体进行热重分析,剩余固体质量与温度关系如图, 时剩余固体的组成可表示为:
时剩余固体的组成可表示为:_______ 。
 在
在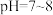 时溶解度最小。某工厂利用钒铬渣提取液(主要成分为
时溶解度最小。某工厂利用钒铬渣提取液(主要成分为 和
和 )制备
)制备 和
和 晶体,流程如下:
晶体,流程如下:
不同温度下相关物质的溶解度
 |  | 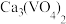 | 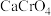 | |
 | 19.3 | 84.0 | 0.1 | 5.5 |
 | 22.5 | 96.5 | 0.09 | 2.49 |
 | 26.3 | 102 | 0.09 | 1.3 |
A.研磨可防止生成的沉淀覆在 表面,提高 表面,提高 利用率 利用率 |
| B.研磨减小了所得钒渣的粒径,提高了后续步骤中钒渣的浸出率 |
C.相对于 、 、 ,工业上更宜选用 ,工业上更宜选用 |
| D.该过程发生了氧化还原反应 |
 晶体时,应采用的结晶方法为
晶体时,应采用的结晶方法为 溶液还原时,还原产物为
溶液还原时,还原产物为 ,则反应的离子方程式
,则反应的离子方程式(3)钒渣成份是
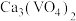 ,“浸出”过程中生成
,“浸出”过程中生成 的离子方程式为
的离子方程式为(4)“转化”过程中选用
 溶液不选用
溶液不选用 溶液的可能原因为
溶液的可能原因为
(5)该流程中可循环利用的物质有
(6)研究表明
 固体(固体的组成用
固体(固体的组成用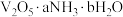 表示)热分解得到
表示)热分解得到 的过程可分为四步,每一步产生
的过程可分为四步,每一步产生 和
和 的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取
的物质的量之比依次为2∶1、3∶1、3∶2、3∶2,取 固体进行热重分析,剩余固体质量与温度关系如图,
固体进行热重分析,剩余固体质量与温度关系如图, 时剩余固体的组成可表示为:
时剩余固体的组成可表示为:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】王老师上课做了“木炭在氧气中燃烧”的实验:将点燃的木炭缓缓地伸入集满氧气的集气瓶中,将木炭取出后向集气瓶中倒入少量澄清石灰水后振荡,让大家观察。
请回答下列问题:
(1)老师“缓慢”地将木炭伸入集气瓶的原因是___________
(2)木炭伸入集气瓶中后所观察到的现象是:___________ ,大家根据___________ 现象,可判断木炭燃烧时生成了二氧化碳。
(3)小华看到老师实验时从集气瓶中取出的木炭已经熄灭,猜想实验时生成的气体中还有___________ 气体。下课后,小华将自己的想法说给老师听,在老师的帮助下,小华对集气瓶中的气体作如下探究:

实验中,当观察到___________ 现象,说明小华的猜想是正确的,请写出直玻璃管中发生反应的化学方程式:___________ 。
(4)从对此实验中生成物的分析可知:反应物的浓度对反应有的影响是___________ 。通过检验,集气瓶中还有氧气剩余,请设计实验进行验证___________ 。
请回答下列问题:
(1)老师“缓慢”地将木炭伸入集气瓶的原因是___________
| A.让同学们观察得更清楚 | B.让木炭与氧气充分反应 |
| C.保证实验时的安全 | D.老师的动作都很慢 |
(3)小华看到老师实验时从集气瓶中取出的木炭已经熄灭,猜想实验时生成的气体中还有

实验中,当观察到
(4)从对此实验中生成物的分析可知:反应物的浓度对反应有的影响是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】12-钨硅酸H4[SiW12O40]是一种环境友好型催化剂、碱性染料媒染剂。一种合成12-钨硅酸的步骤如下:
步骤1:称取25.0gNa2WO4·2H2O置于150mL烧杯中,加入50mL蒸馏水,剧烈搅拌至澄清。
步骤2:在强烈搅拌下继续向烧杯中缓慢加入1.9gNa2SiO3·9H2O使其充分溶解后,将烧杯盖上表面皿,然后将上述溶液加热至沸腾。
步骤3:在微沸和不断搅拌下从滴液漏斗中缓慢地向其中加入浓盐酸,调节pH为2~3.滤出析出的硅酸沉淀并将混合液冷却至室温。
步骤4:在通风橱中,将冷却后的溶液转移到分液漏斗中,加入乙醚,并逐滴加入浓盐酸。充分振荡,静置后分层,将下层油状的十二钨硅酸醚化合物分出于蒸发皿中。反复萃取直至下层不再有油状物分出。
步骤5:向蒸发皿中加入约3.0mL蒸馏水,在40°水浴上蒸醚,直到液体表面出现晶膜。抽滤,即可得到白色12-钨硅酸固体粉末。

已知:乙醚、四氯化碳、乙醇的沸点依次为34.5°C、77°C、78.3°C。
请回答下列问题:
(1)步骤1“搅拌”时使用的仪器名称是_____ 。
(2)步骤3采用如图1装置过滤,能否用烧杯替代锥形瓶?答:_____ (填“能”或“否”),理由是_____ 。
(3)步骤4中,用如图2装置萃取、分液。从下列选项选择合适操作(操作不重复使用)并排序:_____ 。
c→____→____→e→d→f→____。
a.检查旋塞、玻璃塞是否漏水
b.将溶液和乙醚转入分液漏斗并逐滴加入盐酸
c.涂凡士林
d.旋开旋塞放气
e.倒转分液漏斗,小心振荡
f.经几次振荡并放气后,将分液漏斗置于铁架台上静置
g.打开旋塞,向蒸发皿放出下层液体
h.打开旋塞,待下层液体完全流出后,关闭旋塞,将上层液体倒出其中,完成操作d时分液漏斗下端_____ (填“向下”或“向上”)倾斜。
(4)利用图3装置完成“抽滤”,安全瓶的主要作用是_____ ,洗涤产品的操作是_____ 。
(5)步骤5中加入3.0mL蒸馏水的目的是_____ 。
(6)实验中,不能用乙醇、四氯化碳替代乙醚作萃取剂的主要原因_____ 。
步骤1:称取25.0gNa2WO4·2H2O置于150mL烧杯中,加入50mL蒸馏水,剧烈搅拌至澄清。
步骤2:在强烈搅拌下继续向烧杯中缓慢加入1.9gNa2SiO3·9H2O使其充分溶解后,将烧杯盖上表面皿,然后将上述溶液加热至沸腾。
步骤3:在微沸和不断搅拌下从滴液漏斗中缓慢地向其中加入浓盐酸,调节pH为2~3.滤出析出的硅酸沉淀并将混合液冷却至室温。
步骤4:在通风橱中,将冷却后的溶液转移到分液漏斗中,加入乙醚,并逐滴加入浓盐酸。充分振荡,静置后分层,将下层油状的十二钨硅酸醚化合物分出于蒸发皿中。反复萃取直至下层不再有油状物分出。
步骤5:向蒸发皿中加入约3.0mL蒸馏水,在40°水浴上蒸醚,直到液体表面出现晶膜。抽滤,即可得到白色12-钨硅酸固体粉末。

已知:乙醚、四氯化碳、乙醇的沸点依次为34.5°C、77°C、78.3°C。
请回答下列问题:
(1)步骤1“搅拌”时使用的仪器名称是
(2)步骤3采用如图1装置过滤,能否用烧杯替代锥形瓶?答:
(3)步骤4中,用如图2装置萃取、分液。从下列选项选择合适操作(操作不重复使用)并排序:
c→____→____→e→d→f→____。
a.检查旋塞、玻璃塞是否漏水
b.将溶液和乙醚转入分液漏斗并逐滴加入盐酸
c.涂凡士林
d.旋开旋塞放气
e.倒转分液漏斗,小心振荡
f.经几次振荡并放气后,将分液漏斗置于铁架台上静置
g.打开旋塞,向蒸发皿放出下层液体
h.打开旋塞,待下层液体完全流出后,关闭旋塞,将上层液体倒出其中,完成操作d时分液漏斗下端
(4)利用图3装置完成“抽滤”,安全瓶的主要作用是
(5)步骤5中加入3.0mL蒸馏水的目的是
(6)实验中,不能用乙醇、四氯化碳替代乙醚作萃取剂的主要原因
您最近一年使用:0次



