下列事实中,能用平衡移动原理解释的是
A.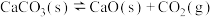 ,平衡时将容器的体积缩小至一半,新平衡的 ,平衡时将容器的体积缩小至一半,新平衡的 浓度与原平衡相同 浓度与原平衡相同 |
| B.实验室中常用排饱和食盐水的方式收集氯气 |
C. ,增大平衡体系的压强(压缩体积)可使体系颜色变深 ,增大平衡体系的压强(压缩体积)可使体系颜色变深 |
D.使用 可以加快 可以加快 的分解 的分解 |
更新时间:2021-02-17 14:23:17
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定温度下,向2L密闭容器中加入足量C(s)并充入2molH2O(g),发生反应C(s)+H2O(g) CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是
CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是
 CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是
CO(g)+H2(g),反应过程中测得如下数据,下列说法错误的是| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(H2)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 | …… |
| A.6min时,反应达到平衡状态,各组分的物质的量均不再改变 |
| B.6min~8min时间段内,υ(H2)=0mol·L-1·min-1 |
| C.该条件下,无论反应多长时间,c(H2)<1mol·L-1 |
| D.保持温度和体积不变,8min时向该容器中充入少量He(g),平衡将会发生移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中发生如下反应:xA(g)+yB(g) zC(g),达到平衡后测得A的浓度为0.20mol·L-1。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.45mol·L-1。下列说法正确的是
zC(g),达到平衡后测得A的浓度为0.20mol·L-1。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.45mol·L-1。下列说法正确的是
 zC(g),达到平衡后测得A的浓度为0.20mol·L-1。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.45mol·L-1。下列说法正确的是
zC(g),达到平衡后测得A的浓度为0.20mol·L-1。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.45mol·L-1。下列说法正确的是| A.x+y>z |
| B.B的转化率降低 |
| C.平衡向右移动 |
| D.C的体积分数提高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有机物1-溴丁烷是一种重要的精细化工产品,在有机合成中作烷基化试剂。实验室用浓硫酸、NaBr固体、1-丁醇和如图装置制备1-溴丁烷。下列说法错误的是


| A.气体吸收装置的作用是吸收HBr,防止其污染空气 |
| B.图中冷凝管中的冷凝水均为a口进b口出 |
| C.分液装置中要进行水洗分液、10%Na2CO3洗涤分液、水洗分液等操作除去杂质 |
| D.浓硫酸的作用包含制取HBr、吸水提高1-丁醇的转化率等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
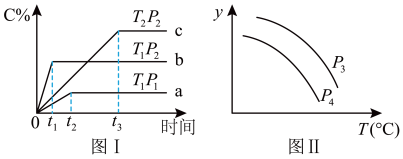
【推荐2】在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g) xC(g) 有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
xC(g) 有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
 xC(g) 有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
xC(g) 有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
| A.X=1,ΔH<0,P3<P4,y轴表示混合气体的密度 |
| B.X=2,ΔH>0,P3<P4,y轴表示B的体积分数 |
| C.X=1,ΔH<0,P3>P4,y轴表示B的转化率 |
| D.X=1,ΔH>0,P3>P4,y轴表示B的体积分数 |
您最近一年使用:0次

 (正反应放热)中反应条件为催化剂
(正反应放热)中反应条件为催化剂 的醋酸溶液稀释10倍,
的醋酸溶液稀释10倍,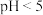
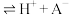 (黄色),向溶液中加入盐酸,溶液呈红色
(黄色),向溶液中加入盐酸,溶液呈红色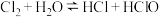 ,当加入
,当加入 溶液后溶液颜色变浅
溶液后溶液颜色变浅

