1100℃时,恒容密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g);ΔH=akJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法不正确的个数有
Fe(s)+CO2(g);ΔH=akJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法不正确的个数有
①达到化学平衡状态时,若c(CO)=0.100mol/L,则c(CO2)=0.0263mol/L
②若要提高CO的转化率,则可以加入过量FeO
③若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
④若生成28gFe,则吸收的热量大于0.5akJ
 Fe(s)+CO2(g);ΔH=akJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法不正确的个数有
Fe(s)+CO2(g);ΔH=akJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法不正确的个数有①达到化学平衡状态时,若c(CO)=0.100mol/L,则c(CO2)=0.0263mol/L
②若要提高CO的转化率,则可以加入过量FeO
③若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
④若生成28gFe,则吸收的热量大于0.5akJ
| A.1个 | B.2个 | C.3个 | D.4个 |
更新时间:2021-03-04 16:54:56
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量。下列表示该反应的热化学方程式中正确的是( )
A.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=-22.68kJ·mol-1 O2(g)=CO2(g)+2H2O(l) △H=-22.68kJ·mol-1 |
B.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=-725.8kJ O2(g)=CO2(g)+2H2O(l) △H=-725.8kJ |
C.CH3OH+ O2=CO2+2H2O △H=-725.8kJ·mol-1 O2=CO2+2H2O △H=-725.8kJ·mol-1 |
D.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=-725.8kJ·mol-1 O2(g)=CO2(g)+2H2O(l) △H=-725.8kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知常温常压下,N2(g)+3H2(g) 2NH3(g)ΔH=-Q1kJ/mol。在同温同压下向一密闭容器中通入0.5molN2和1.5molH2,反应完成时放出热量为Q2kJ,则下列关系正确的是
2NH3(g)ΔH=-Q1kJ/mol。在同温同压下向一密闭容器中通入0.5molN2和1.5molH2,反应完成时放出热量为Q2kJ,则下列关系正确的是
 2NH3(g)ΔH=-Q1kJ/mol。在同温同压下向一密闭容器中通入0.5molN2和1.5molH2,反应完成时放出热量为Q2kJ,则下列关系正确的是
2NH3(g)ΔH=-Q1kJ/mol。在同温同压下向一密闭容器中通入0.5molN2和1.5molH2,反应完成时放出热量为Q2kJ,则下列关系正确的是| A.Q1=Q2 | B.Q2=0.5Q1 | C.Q2<0.5Q1 | D.Q2>0.5Q1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】有关化学平衡的说法正确的是
| A.化学平衡不可以通过改变条件而改变 |
| B.到达化学平衡时反应也达到该条件下的最大速率 |
| C.当一个可逆反应进行到平衡状态时,反应的正反应速率和逆反应速率相等 |
| D.平衡状态是一种微观静止的状态,因为反应物和生成物的浓度已不再改变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.密闭容器中,氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| B.升高温度,NO2和N2O4混合气体的颜色加深 |
| C.Fe(SCN)3溶液中加入少量KSCN固体后颜色变深 |
| D.水垢中含有CaSO4,可先用Na2CO3溶液浸泡处理,而后用盐酸去除 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】在一定温度下的恒容密闭容器中,当下列条件不再改变时,表明反应A(s)+2B(g) C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是
 C(g)+D(g)已达到平衡状态的是
C(g)+D(g)已达到平衡状态的是| A.混合气体的压强 |
| B.混合气体的密度 |
| C.气体的总物质的量 |
| D.单位时间内生成nmolC的同时消耗2nmolB |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在2L密闭容器中发生以下反应:2A(g)+B(g) 2C(g)+D(g)。若最初加入的A和B都是4mol,在前10s,A的平均反应速率为0.12mol·L-1·s-1,则下列说法正确的是
2C(g)+D(g)。若最初加入的A和B都是4mol,在前10s,A的平均反应速率为0.12mol·L-1·s-1,则下列说法正确的是
 2C(g)+D(g)。若最初加入的A和B都是4mol,在前10s,A的平均反应速率为0.12mol·L-1·s-1,则下列说法正确的是
2C(g)+D(g)。若最初加入的A和B都是4mol,在前10s,A的平均反应速率为0.12mol·L-1·s-1,则下列说法正确的是| A.10s时,容器中B的物质的量浓度为1.6mol/L |
| B.2v(A)=v(D) |
| C.若10s时,c(A)∶c(B)∶c(C)∶c(D)=2∶1∶2∶1,则此时该反应达到平衡 |
| D.10s时,A的转化率为60% |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】在一密闭容器中通入A、B、C三种气体,保持一定温度,在t1~t4s时测得各物质的浓度如表,则下列判断正确的是
测定时刻/s 浓度 | t1 | t2 | t3 | t4 |
c(A)/(mol·L-1) | 6 | 3 | 2 | 2 |
c(B)/(mol·L-1) | 5 | 3.5 | 3 | 3 |
c(C)/(mol·L-1) | 1 | 2.5 | 3 | 3 |
| A.在t3s时反应已经停止 |
| B.t3~t4s内正、逆反应速率不相等 |
C.在容器中发生的反应为A(g)+B(g) C(g) C(g) |
D.在t2~t3s内A的平均反应速率为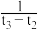 mol·L−1·s−1 mol·L−1·s−1 |
您最近一年使用:0次
【推荐1】常压下利用可逆反应Ni(s)+4CO(g)⇌Ni(CO)4(g)精炼镍。已知230℃时,该反应的平衡常数K=2×10-5(L/mol)3,Ni(CO)4的沸点为42.2℃,粗镍中固体杂质不参与反应。下列说法错误的是
| A.恒容体系下,增加c[Ni(CO)4],体系压强增大,平衡常数增大 |
| B.50℃时将粗镍与CO反应,可以获得相应的气态产物便于与粗镍杂质分离 |
| C.测量某温度下反应体系中Ni(CO)4体积分数不变时,反应达到平衡 |
| D.230℃,Ni(CO)4平衡分解率较高 |
您最近一年使用:0次
【推荐2】由γ-羟基丁酸( HOCH2CH2CH2COOH)生成γ-丁内酯(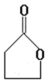 )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH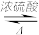
 + H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。
+ H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。
下列说法正确的是
 )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH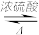
 + H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。
+ H2O,25 ℃时,溶液中γ-羟基丁酸的起始浓度为0.180 mol·L-1,测得γ-丁内酯的浓度随时间的变化如表所示。| t/ min | 21 | 50 | 80 | 100 | 120 | 160 | ∞ |
| c/( mol·L-1) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.132 |
A.50~ 100 min内,γ-丁内酯的反应速率为 mol·L-1 mol·L-1 |
B.在120 min时,γ-羟基丁酸的转化率为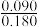 ×100% ×100% |
| C.控制温度、加压和分离产品都可以提高原料的转化率 |
D.25 ℃ 时,该反应的平衡常数为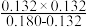 mol·L-1 mol·L-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】硫元素形成的化合物有着广泛的用途,其中过二硫酸 是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。氮、硫的氧化物无害化、再利用具有重要意义,可利用下面反应进行氮、硫的氧化物再利用:NO2(g)+SO2(g)
是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。氮、硫的氧化物无害化、再利用具有重要意义,可利用下面反应进行氮、硫的氧化物再利用:NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=-83.6 kJ∙mol−1。下面说法正确的是
SO3(g)+NO(g) ΔH=-83.6 kJ∙mol−1。下面说法正确的是
 是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。氮、硫的氧化物无害化、再利用具有重要意义,可利用下面反应进行氮、硫的氧化物再利用:NO2(g)+SO2(g)
是一种强氧化剂,可用作氧化剂和漂白剂,过二硫酸及其盐都是不稳定的,加热时分解,溶于水会发生一定程度的水解,电解硫酸钾溶液可得过二硫酸钾。氮、硫的氧化物无害化、再利用具有重要意义,可利用下面反应进行氮、硫的氧化物再利用:NO2(g)+SO2(g) SO3(g)+NO(g) ΔH=-83.6 kJ∙mol−1。下面说法正确的是
SO3(g)+NO(g) ΔH=-83.6 kJ∙mol−1。下面说法正确的是| A.NO2、SO2体积比保持不变可用来判定平衡状态 |
| B.加压可加快反应速率,使平衡时SO3产量提高 |
| C.恒容条件下,投料物质的量比为1:1,若NO2平衡转化率为60%,则平衡常数为2.25 |
| D.NO可直接用NaOH溶液吸收,制取NaNO2 |
您最近一年使用:0次

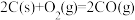
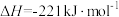
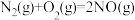

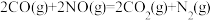

 完全燃烧所放出的热量为
完全燃烧所放出的热量为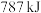




 ,并循环利用未反应完的
,并循环利用未反应完的 和
和


