单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。
(1)基态镍原子的核外电子排布式为___________ 。
(2)氧化镁载体及镍催化反应中涉及到 、
、 和
和 等物质。元素Mg、O和C的第一电离能由小到大排序为
等物质。元素Mg、O和C的第一电离能由小到大排序为 ___________ ;在上述三种物质的分子中碳原子杂化类型不同于其他两种的是 ___________ ,立体构型为正四面体的分子是 ___________ ,三种物质中沸点最高的是 ,其原因是
,其原因是 ___________ 。
(3)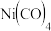 晶体类型是
晶体类型是 ___________ 。
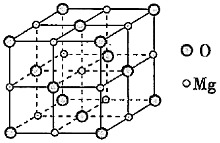
(4) 已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞边长为a nm
已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞边长为a nm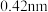 ,则MgO的密度为
,则MgO的密度为 ___________ g/cm3
(5)某短周期金属元素R的部分电离能如表所示:
该金属元素是___________ 。 填元素符号
填元素符号
(1)基态镍原子的核外电子排布式为
(2)氧化镁载体及镍催化反应中涉及到
 、
、 和
和 等物质。元素Mg、O和C的第一电离能由小到大排序为
等物质。元素Mg、O和C的第一电离能由小到大排序为  ,其原因是
,其原因是 (3)
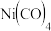 晶体类型是
晶体类型是 (4)
 已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞边长为a nm
已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞边长为a nm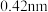 ,则MgO的密度为
,则MgO的密度为 
(5)某短周期金属元素R的部分电离能如表所示:
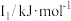 |  |  |  |  |
| 738 | 1451 | 7733 | 10540 | 13630 |
该金属元素是
 填元素符号
填元素符号
更新时间:2021-03-29 22:29:20
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】随着新能源汽车的发展,钾电池成为近些年来研究的热点、锂电池中一些金属的回收利用也是未来发展的一大方向。SiCl4是生产多晶硅的副产物。可以利用SiCl4对废弃的钾电池正极材料LiCoO2进行氯化处理、进而回收Li、Co等金属,工艺路线如图所示:

(1)Co的价电子排布式为___________ 。
(2)烧渣是LiCl、CoCl2和SiO2的混合物,“500℃焙烧”后剩余的SiCl4应先除去,否则水浸时会产生大量烟雾。用化学方程式表示其原因:___________ 。
(3)已知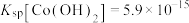 ,若“沉钴过滤”的pH控制为10.0,则溶液中Co2+的浓度为
,若“沉钴过滤”的pH控制为10.0,则溶液中Co2+的浓度为___________ mol·L-1。“850℃煅烧”时的化学方程式为___________ 。
(4)利用碳酸锂( )与
)与 按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电池正极材料
按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电池正极材料
 反应方程式为
反应方程式为___________ 。
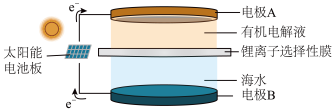
(5)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示。金属锂在电极______ (填“A”或“B”)上生成,阳极产生两种气体单质、电极反应式是________ 。

(1)Co的价电子排布式为
(2)烧渣是LiCl、CoCl2和SiO2的混合物,“500℃焙烧”后剩余的SiCl4应先除去,否则水浸时会产生大量烟雾。用化学方程式表示其原因:
(3)已知
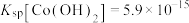 ,若“沉钴过滤”的pH控制为10.0,则溶液中Co2+的浓度为
,若“沉钴过滤”的pH控制为10.0,则溶液中Co2+的浓度为(4)利用碳酸锂(
 )与
)与 按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电池正极材料
按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电池正极材料
 反应方程式为
反应方程式为(5)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图所示。金属锂在电极

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D为四种原子序数依次增大的短周期元素,其中B、C、D位于同一周期,A、B形成的分子具有对称的正四面体结构,C的单质分子是NO+(亚硝酰离子)的等电子体,D是元素周期表中电负性最大的元素。根据上述,回答下列问题:
⑴B原子的核外电子排布式是______________ ;
⑵写出上述A、B所形成的分子的电子式:____________ ;
⑶NO+的结构中可能含____ 个σ键,含___ 个π键。
⑷写出B、C的氢化物的立体构型分别是________ 、_________ ;
⑸用氢键表示式写出D的氢化物溶液中存在的所有氢键______________ 。
⑴B原子的核外电子排布式是
⑵写出上述A、B所形成的分子的电子式:
⑶NO+的结构中可能含
⑷写出B、C的氢化物的立体构型分别是
⑸用氢键表示式写出D的氢化物溶液中存在的所有氢键
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】铜是重要的战略资源,云南是我国铜资源储量较高的省份之一,回答下列问题:
(1)铜在周期表中位于第______ 族(填族序数),属于______ 区。
(2)铜可以形成多种配合物。
① 的核外电子排布式是
的核外电子排布式是______ ,过渡金属离子与水分子形成配合物时,若d轨道全空或全满时,化合物无颜色,否则有颜色。据此判断,
______ (填“有”或“无”)颜色。
② 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是______ , 中N原子的杂化方式是
中N原子的杂化方式是______ ,空间构型是______ 。
(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是______ 。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为______ 。
(1)铜在周期表中位于第
(2)铜可以形成多种配合物。
①
 的核外电子排布式是
的核外电子排布式是
②
 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是 中N原子的杂化方式是
中N原子的杂化方式是(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且A原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满。回答下列问题:
(1)基态E原子价电子的轨道表达式_______ 。
(2)DA2分子的VSEPR模型是_______ 。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
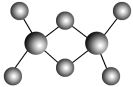
①C2Cl6属于_______ 晶体(填晶体类型),其中C原子的杂化轨道类型为_______ 杂化。
②[C(OH)4]-中存在的化学键有_______ 。
a.离子键 b.共价键 c.σ键 d.π键 e.配位键 f.氢键
(4)B、C的氟化物晶格能分别是2957 kJ/mol 、5492 kJ/mol,二者相差很大的原因_______ 。
(1)基态E原子价电子的轨道表达式
(2)DA2分子的VSEPR模型是
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。

①C2Cl6属于
②[C(OH)4]-中存在的化学键有
a.离子键 b.共价键 c.σ键 d.π键 e.配位键 f.氢键
(4)B、C的氟化物晶格能分别是2957 kJ/mol 、5492 kJ/mol,二者相差很大的原因
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】高温乃至室温超导一直是科学家不懈追求目标。科学家合成了一种高温超导材料,其晶胞结构如图所示(B和C原子均位于晶胞面上),该立方晶胞参数为apm。
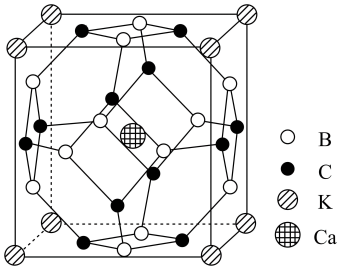
(1)该晶体的四种元素的电负性由大到小的顺序是___________ 。钙元素的焰色实验为砖红色,基于其原理可用于定性与定量分析,这种分析方法称为___________ 光谱。
(2)该晶体中,B原子的杂化轨道类型是_______ ,C原子的杂化轨道类型是________ 。
(3)该晶体中微粒间存在的化学键有_________ 、___________ 。
(4)该晶体的化学式为________ (化成最简整数比),密度为_________  (列出计算式,相对分子质量用M表示无需计算出数值)。
(列出计算式,相对分子质量用M表示无需计算出数值)。
(5)晶胞中B和C原子构成的多面体有_________ 个面
(6)比较 与
与 的沸点并解释原因
的沸点并解释原因_________ ;比较 与
与 的键角并解释原因
的键角并解释原因___________ 。

(1)该晶体的四种元素的电负性由大到小的顺序是
(2)该晶体中,B原子的杂化轨道类型是
(3)该晶体中微粒间存在的化学键有
(4)该晶体的化学式为
 (列出计算式,相对分子质量用M表示无需计算出数值)。
(列出计算式,相对分子质量用M表示无需计算出数值)。(5)晶胞中B和C原子构成的多面体有
(6)比较
 与
与 的沸点并解释原因
的沸点并解释原因 与
与 的键角并解释原因
的键角并解释原因
您最近半年使用:0次
【推荐3】按要求填空:
(1)基态K原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(2) 基态核外电子排布式为
基态核外电子排布式为_______ ,基态O原子的价层电子排布图为_______ 。
(3) 的空间结构是
的空间结构是_______ ,其中S原子的杂化轨道类型是_______ 。
(4) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______
(5)某元素 价离子的电子排布式为
价离子的电子排布式为 ,该元素在周期表中的位置
,该元素在周期表中的位置_______
(1)基态K原子中,核外电子占据最高能层的符号是
(2)
 基态核外电子排布式为
基态核外电子排布式为(3)
 的空间结构是
的空间结构是(4)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(5)某元素
 价离子的电子排布式为
价离子的电子排布式为 ,该元素在周期表中的位置
,该元素在周期表中的位置
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】短周期元素A、B、C、D的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4。
(1)基态B原子的价电子排布图 为______________ ;基态D原子核外电子占据最高能级的电子云轮廓图为_____________ 形。
(2)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp2杂化、空间结构为平面三角形的是_________ (填分子式,下同),属于极性分子的是_________ ,键角由大到小的顺序为_____________ 。
(3)(DC)4为热色性固体,且有色温效应,其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。(DC)4属于_______ 晶体,在淡黄色→橙黄色→深红色的转化中,破坏的作用力是___________ ;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是_________ 。
(4)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子)。已知:该晶体边长为a nm,NA代表阿伏加德罗常数的值。_______________ ,晶体性脆的原因是_______________ 。
②该晶体的密度为_____________ g·cm-3(不必化简)。
(1)基态B原子的
(2)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp2杂化、空间结构为平面三角形的是
(3)(DC)4为热色性固体,且有色温效应,其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。(DC)4属于
(4)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子)。已知:该晶体边长为a nm,NA代表阿伏加德罗常数的值。

②该晶体的密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
(1)X基态原子的核外电子排布式为_______ ,Y的原子结构示意图_______ 。
(2)X是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
① 1 mol苯分子中含有σ 键的数目为_______ mol。
② 异丙苯分子中碳原子轨道的杂化类型为_______ 。
(3)Y的氢化物沸点高于同族氢化物沸点的原因_______ 。
(4)XZ3易溶于水,熔点为960 ℃,熔融状态下能够导电,据此可判断XY3晶体属于_______ (填晶体类型)。
(5)元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为_______ 。
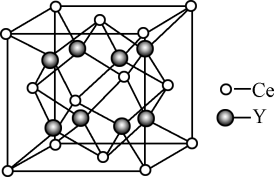
(1)X基态原子的核外电子排布式为
(2)X是石油化工中重要的催化剂之一,如催化异丙苯(
 )裂化生成苯和丙烯。
)裂化生成苯和丙烯。① 1 mol苯分子中含有σ 键的数目为
② 异丙苯分子中碳原子轨道的杂化类型为
(3)Y的氢化物沸点高于同族氢化物沸点的原因
(4)XZ3易溶于水,熔点为960 ℃,熔融状态下能够导电,据此可判断XY3晶体属于
(5)元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】 、
、 常用于制造农药等。磷在氯气中燃烧生成这两种卤化磷。请回答下列问题:
常用于制造农药等。磷在氯气中燃烧生成这两种卤化磷。请回答下列问题:
(1) 的VSEPR模型是
的VSEPR模型是______ 。已知 中P原子的d能级参与杂化,分子呈三角双锥形(如图甲),由此推知
中P原子的d能级参与杂化,分子呈三角双锥形(如图甲),由此推知 中P的杂化类型为
中P的杂化类型为______ (填标号)。 B.
B. C.
C.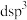 D.
D.
(2)已知,①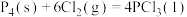
 kJ⋅mol
kJ⋅mol ,
,
②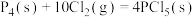
 kJ⋅mol
kJ⋅mol (
(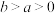 )。
)。
则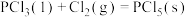

______ (用含a、b、c的式子表示)kJ⋅mol 。
。
(3)实验测得 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关),速率常数k与活化能的经验关系式为
(k为速率常数,只与温度、催化剂有关),速率常数k与活化能的经验关系式为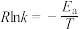 (R为常数,
(R为常数, 为活化能,T为绝对温度)。
为活化能,T为绝对温度)。 和
和 ,实验测得在催化剂Cat1、Cat2下
,实验测得在催化剂Cat1、Cat2下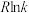 与
与 的关系如图乙所示。催化效能较高的是
的关系如图乙所示。催化效能较高的是______ (填“Cat1”或“Cat2”),判断依据是____________ 。
②将2n mol 和n mol
和n mol 充入体积不变的密闭容器中,一定条件下发生上述反应,达到平衡时,
充入体积不变的密闭容器中,一定条件下发生上述反应,达到平衡时, 为a mol,如果此时移走n mol
为a mol,如果此时移走n mol 和0.5n mol
和0.5n mol  ,在相同温度下再达到平衡时
,在相同温度下再达到平衡时 的物质的量为x,则x为
的物质的量为x,则x为______ (填标号)。
A. mol B.
mol B. mol C.
mol C. mol D.0.5a mol
mol D.0.5a mol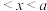 mol
mol
(4)向恒容密闭容器中投入0.2 mol 和0.2 mol
和0.2 mol  ,发生反应:
,发生反应: ,在不同条件下进行,反应体系总压强随时间的变化如图丙所示。
,在不同条件下进行,反应体系总压强随时间的变化如图丙所示。____________ ;曲线c改变的条件可能是____________ 。
②曲线b条件下,该反应平衡常数( )为
)为______ 。[提示:用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数。]
,分压=总压×物质的量分数。]
 、
、 常用于制造农药等。磷在氯气中燃烧生成这两种卤化磷。请回答下列问题:
常用于制造农药等。磷在氯气中燃烧生成这两种卤化磷。请回答下列问题:(1)
 的VSEPR模型是
的VSEPR模型是 中P原子的d能级参与杂化,分子呈三角双锥形(如图甲),由此推知
中P原子的d能级参与杂化,分子呈三角双锥形(如图甲),由此推知 中P的杂化类型为
中P的杂化类型为
 B.
B. C.
C.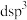 D.
D.
(2)已知,①
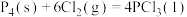
 kJ⋅mol
kJ⋅mol ,
,②
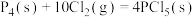
 kJ⋅mol
kJ⋅mol (
(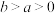 )。
)。则
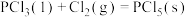

 。
。(3)实验测得
 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关),速率常数k与活化能的经验关系式为
(k为速率常数,只与温度、催化剂有关),速率常数k与活化能的经验关系式为 (R为常数,
(R为常数, 为活化能,T为绝对温度)。
为活化能,T为绝对温度)。
 和
和 ,实验测得在催化剂Cat1、Cat2下
,实验测得在催化剂Cat1、Cat2下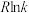 与
与 的关系如图乙所示。催化效能较高的是
的关系如图乙所示。催化效能较高的是②将2n mol
 和n mol
和n mol 充入体积不变的密闭容器中,一定条件下发生上述反应,达到平衡时,
充入体积不变的密闭容器中,一定条件下发生上述反应,达到平衡时, 为a mol,如果此时移走n mol
为a mol,如果此时移走n mol 和0.5n mol
和0.5n mol  ,在相同温度下再达到平衡时
,在相同温度下再达到平衡时 的物质的量为x,则x为
的物质的量为x,则x为A.
 mol B.
mol B. mol C.
mol C. mol D.0.5a mol
mol D.0.5a mol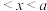 mol
mol(4)向恒容密闭容器中投入0.2 mol
 和0.2 mol
和0.2 mol  ,发生反应:
,发生反应: ,在不同条件下进行,反应体系总压强随时间的变化如图丙所示。
,在不同条件下进行,反应体系总压强随时间的变化如图丙所示。
②曲线b条件下,该反应平衡常数(
 )为
)为 ,分压=总压×物质的量分数。]
,分压=总压×物质的量分数。]
您最近半年使用:0次



