(1)基态Co原子的电子排布式为_______ 。
(2)BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:
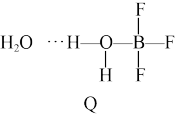
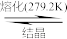
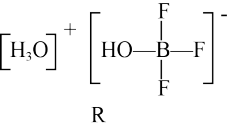
晶体Q中各种微粒间的作用力不涉及_______ (填序号)。
a.离子键 b.共价键 c. 配位键 d.金属键
(3)NaF和NaCl属于同一主族的钠盐,但NaF的硬度比NaCl大,原因是_______ 。
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为_______ 。
(5)第一电离能介于B、N之间的第二周期元素有_______ 种。S单质的常见形式为S8,其环状结构如图所示,该分子中S原子采用的轨道杂化方式是_______ 。
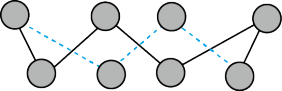
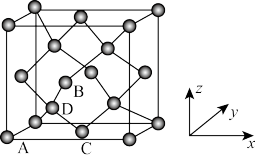
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,图为金刚石的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子坐标参数为
,0)。则D原子坐标参数为_______ 。②晶胞参数,描述晶胞的大小和形状,已知金刚石的晶胞参数a=356.89pm,其密度为_______ g•cm-3。(列出计算式即可,不必计算出结果)
(2)BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:

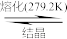

晶体Q中各种微粒间的作用力不涉及
a.离子键 b.共价键 c. 配位键 d.金属键
(3)NaF和NaCl属于同一主族的钠盐,但NaF的硬度比NaCl大,原因是
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
(5)第一电离能介于B、N之间的第二周期元素有

(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,图为金刚石的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子坐标参数为
,0)。则D原子坐标参数为
更新时间:2021-03-31 16:10:11
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】新型节能材料高温超导体的最先突破是从1987年新的钇钡铜氧材料的研究开始的。对钇钡铜氧材料的分析表明,其组成为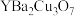 ;其中39号元素金属钇化合价为+3价,铜以常见的
;其中39号元素金属钇化合价为+3价,铜以常见的 和罕见的高价态形式存在。
和罕见的高价态形式存在。
(1)写出该物质中高价铜离子的核外价电子排布图___________ 。
(2)将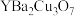 试样溶于稀酸,高价铜离子全部被还原为
试样溶于稀酸,高价铜离子全部被还原为 。写出试样在稀酸中溶解的离子反应方程式
。写出试样在稀酸中溶解的离子反应方程式___________ 。
(3) 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。若
。若 中两个
中两个 ,分别被
,分别被 取代,能得到(m)、(n)两种不同结构的
取代,能得到(m)、(n)两种不同结构的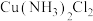 :
: 的空间构型是
的空间构型是___________ ;在水中的溶解度:(m)___________ (n)(填“>”、“=”或“<”)。
(4)锌、钴、镍可形成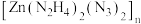 、
、 、
、 等配合物。
等配合物。
①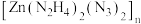 中
中 的配体是
的配体是___________ 。
②氯化钴(Ⅲ)的氨合物钴离子配位数为6,制备条件不同,所得晶体结构不同。有活性炭催化时,主要生成橙黄色晶体 ,已知
,已知 是以
是以 为中心的正八面体结构(如图所示),若其中2个
为中心的正八面体结构(如图所示),若其中2个 被
被 取代,则所形成的
取代,则所形成的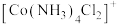 的空间结构有
的空间结构有___________ 种;没有活性炭时,所得主要产物是紫红色晶体,化学式为 ,向含0.1mol该晶体的水溶液中滴加
,向含0.1mol该晶体的水溶液中滴加 溶液,可得白色沉淀28.7g,该晶体配离子的化学式为
溶液,可得白色沉淀28.7g,该晶体配离子的化学式为___________ 。___________ 。
②钇钡铜氧晶体属四方晶系,晶胞参数如图所示,晶胞棱长夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。如原子分数坐标A为(0,0,0),B为 ( ,
, ,
, ),C为(
),C为( ,
, ,m),则D的原子分数坐标为
,m),则D的原子分数坐标为___________ 。
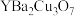 ;其中39号元素金属钇化合价为+3价,铜以常见的
;其中39号元素金属钇化合价为+3价,铜以常见的 和罕见的高价态形式存在。
和罕见的高价态形式存在。(1)写出该物质中高价铜离子的核外价电子排布图
(2)将
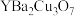 试样溶于稀酸,高价铜离子全部被还原为
试样溶于稀酸,高价铜离子全部被还原为 。写出试样在稀酸中溶解的离子反应方程式
。写出试样在稀酸中溶解的离子反应方程式(3)
 能与
能与 形成具有对称空间结构的
形成具有对称空间结构的 。若
。若 中两个
中两个 ,分别被
,分别被 取代,能得到(m)、(n)两种不同结构的
取代,能得到(m)、(n)两种不同结构的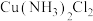 :
:
 的空间构型是
的空间构型是(4)锌、钴、镍可形成
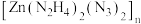 、
、 、
、 等配合物。
等配合物。①
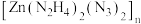 中
中 的配体是
的配体是②氯化钴(Ⅲ)的氨合物钴离子配位数为6,制备条件不同,所得晶体结构不同。有活性炭催化时,主要生成橙黄色晶体
 ,已知
,已知 是以
是以 为中心的正八面体结构(如图所示),若其中2个
为中心的正八面体结构(如图所示),若其中2个 被
被 取代,则所形成的
取代,则所形成的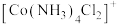 的空间结构有
的空间结构有 ,向含0.1mol该晶体的水溶液中滴加
,向含0.1mol该晶体的水溶液中滴加 溶液,可得白色沉淀28.7g,该晶体配离子的化学式为
溶液,可得白色沉淀28.7g,该晶体配离子的化学式为
②钇钡铜氧晶体属四方晶系,晶胞参数如图所示,晶胞棱长夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标。如原子分数坐标A为(0,0,0),B为 (
 ,
, ,
, ),C为(
),C为( ,
, ,m),则D的原子分数坐标为
,m),则D的原子分数坐标为
您最近一年使用:0次
【推荐2】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醇一定条件下直接脱氢可制甲醛,涉及的反应如下:
反应I:

反应II:

已知:①平衡状态下,甲醛选择性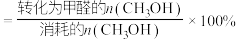 ;甲醛的收率
;甲醛的收率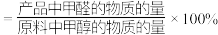 。
。
②几种物质的燃烧热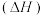 如下表:
如下表:
回答下列问题:
(1)
_______ ,HCHO的空间结构为_______ 形。
(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii: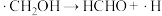
历程iii:
历程iv: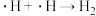
写出历程i的反应方程式:_______ 。
(3)将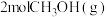 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示:_______ (填“I”或“II”),判断的依据是_______ 。
② ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为_______ ,
_______ ,反应I的平衡常数
_______  。
。
反应I:


反应II:


已知:①平衡状态下,甲醛选择性
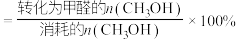 ;甲醛的收率
;甲醛的收率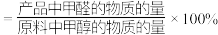 。
。②几种物质的燃烧热
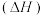 如下表:
如下表:| 物质 |  |  |  |  |
燃烧热 | -725.8 | -563.6 | -283.0 | -285.8 |
(1)

(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii:
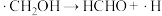
历程iii:

历程iv:
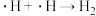
写出历程i的反应方程式:
(3)将
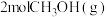 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示: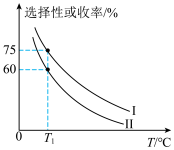
②
 ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为

 。
。
您最近一年使用:0次
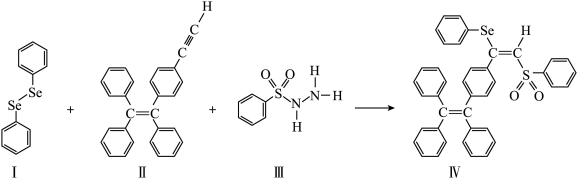
【推荐3】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子Ⅳ的合成路线如下:___________ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是___________ 。
(3)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有___________ 。
A.Ⅰ中有σ键和π键
B.Ⅰ中的 键为极性共价键
键为极性共价键
C.Ⅱ难溶于水
D.Ⅱ中原子的杂化轨道类型只有sp与
E.Ⅲ含有的元素中,N电负性最大
(4)Ⅳ中具有孤对电子的原子有___________ 。
(5)硒的两种含氧酸的酸性强弱为
___________  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(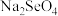 )可减轻重金属铊引起的中毒;
)可减轻重金属铊引起的中毒; 的立体构型为
的立体构型为___________ 。
(6)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示,其中原子坐标参数A为(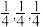 ),则C的原子坐标参数为
),则C的原子坐标参数为___________ 。
(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有
A.Ⅰ中有σ键和π键
B.Ⅰ中的
 键为极性共价键
键为极性共价键C.Ⅱ难溶于水
D.Ⅱ中原子的杂化轨道类型只有sp与

E.Ⅲ含有的元素中,N电负性最大
(4)Ⅳ中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(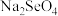 )可减轻重金属铊引起的中毒;
)可减轻重金属铊引起的中毒; 的立体构型为
的立体构型为(6)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示,其中原子坐标参数A为(
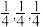 ),则C的原子坐标参数为
),则C的原子坐标参数为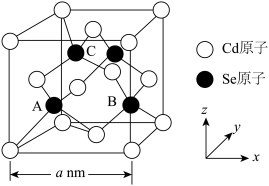
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】物质结构具有极强的几何美感,微粒间存在不同的作用力,从不同的堆积方式到五彩斑斓的晶体结构,我们感叹于大自然神奇的力量的同时创造着新物质,让生活变得更美好!
(1)-40℃时, 与冰反应生成HOF和HF。常温常压下,HOF为无色气体,固态HOF的晶体类型为
与冰反应生成HOF和HF。常温常压下,HOF为无色气体,固态HOF的晶体类型为_______ ,HOF水解反应的产物为_______ 。(填化学式)。
(2) 中心原子为Cl,
中心原子为Cl, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中Cl原子的轨道杂化方式
中Cl原子的轨道杂化方式_______ ;基态Cl原子中电子占据最高能级的电子云轮廓为_______ ;O―Cl―O键角_______ Cl―O―Cl键角(填“>”“<”或“=”)。比较 与
与 中Cl―O键的键长并说明原因
中Cl―O键的键长并说明原因_______ 。
(3)几种化学键的键能如下表所示:
由两种单质化合形成1mol ,焓变
,焓变
_______  。
。
(4)已知: 常温常压下为无色气体,熔点―129℃,沸点―207℃,
常温常压下为无色气体,熔点―129℃,沸点―207℃, 为黄色油状液体,熔点―40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点―40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
① 热稳定性高于
热稳定性高于 :
:_______ 。
② 熔、沸点高于
熔、沸点高于 :
:_______ 。
(5)过渡金属易与CO形成羰基配合物,如配合物 ,常温下为液态,易溶于
,常温下为液态,易溶于 、苯等有机溶剂。
、苯等有机溶剂。
① 固态时属于
固态时属于_______ 分子(填极性或非极性)。
② 中Ni与CO的
中Ni与CO的_______ 原子形成配位键。
③ 分子中
分子中 键和
键和 键个数比为
键个数比为_______ 。
(6) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。基态
反应制得。基态 的电子占据的最高能级符号为
的电子占据的最高能级符号为_______ ,该能级具有的原子轨道数为_______ , 的立体结构是
的立体结构是_______ 。
(7)某Ba-Ti-O晶体具有良好的电学性能,其晶胞为立方晶胞(如图)晶胞边长为a pm。设阿伏加德罗常数的值为 ,下列说法错误的是_______。
,下列说法错误的是_______。

(8)基态 原子的价层电子轨道表示式:
原子的价层电子轨道表示式:_______ 。
(9)硝酸乙基铵 是人类发现的第一种常温离子液体,其熔点为12℃,已知
是人类发现的第一种常温离子液体,其熔点为12℃,已知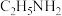 结合质子的能力比
结合质子的能力比 略强,下列有关硝酸乙基铵的说法正确的是_______。
略强,下列有关硝酸乙基铵的说法正确的是_______。
(1)-40℃时,
 与冰反应生成HOF和HF。常温常压下,HOF为无色气体,固态HOF的晶体类型为
与冰反应生成HOF和HF。常温常压下,HOF为无色气体,固态HOF的晶体类型为(2)
 中心原子为Cl,
中心原子为Cl, 中心原子为O,二者均为V形结构,但
中心原子为O,二者均为V形结构,但 中存在大
中存在大 键(
键( )。
)。 中Cl原子的轨道杂化方式
中Cl原子的轨道杂化方式 与
与 中Cl―O键的键长并说明原因
中Cl―O键的键长并说明原因(3)几种化学键的键能如下表所示:
| 化学键 | N≡N | F―F | N―F |
键能 | 941.6 | 154.8 | 283.0 |
 ,焓变
,焓变
 。
。(4)已知:
 常温常压下为无色气体,熔点―129℃,沸点―207℃,
常温常压下为无色气体,熔点―129℃,沸点―207℃, 为黄色油状液体,熔点―40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点―40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:①
 热稳定性高于
热稳定性高于 :
:②
 熔、沸点高于
熔、沸点高于 :
:(5)过渡金属易与CO形成羰基配合物,如配合物
 ,常温下为液态,易溶于
,常温下为液态,易溶于 、苯等有机溶剂。
、苯等有机溶剂。①
 固态时属于
固态时属于②
 中Ni与CO的
中Ni与CO的③
 分子中
分子中 键和
键和 键个数比为
键个数比为(6)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。基态
反应制得。基态 的电子占据的最高能级符号为
的电子占据的最高能级符号为 的立体结构是
的立体结构是(7)某Ba-Ti-O晶体具有良好的电学性能,其晶胞为立方晶胞(如图)晶胞边长为a pm。设阿伏加德罗常数的值为
 ,下列说法错误的是_______。
,下列说法错误的是_______。
A.化学式为 | B. 和 和 间的最短距离为 间的最短距离为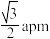 |
C.该晶胞中与 等距离且最近的 等距离且最近的 有4个 有4个 | D.晶体的密度为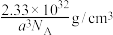 |
(8)基态
 原子的价层电子轨道表示式:
原子的价层电子轨道表示式:(9)硝酸乙基铵
 是人类发现的第一种常温离子液体,其熔点为12℃,已知
是人类发现的第一种常温离子液体,其熔点为12℃,已知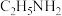 结合质子的能力比
结合质子的能力比 略强,下列有关硝酸乙基铵的说法正确的是_______。
略强,下列有关硝酸乙基铵的说法正确的是_______。| A.该离子液体不易挥发,可用作绿色溶剂 |
| B.该物质在常温下不能导电 |
| C.该离子液体阴阳离子体积很大,结构松散,作用力弱 |
| D.同温同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液相比前者的pH小 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】无水三氯化铬( )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应 制取
制取 的
的 (俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(1)上述装置的正确连接顺序为___________ (填字母,按气流方向从左到右)。
(2)装置A中所盛放的试剂是___________ ,装置A中竖直长玻璃管的作用是___________ 。装置D中n瓶的作用是___________ 。实验过程中为了避免装置A中长玻璃管中液面上升,可以采用的方法为___________ (填序号)。
①对m处导管进行加热 ②将m处导管加粗 ③持续通入氮气
(3)装置E中发生反应的离子方程式为___________ 。无水 的作用是
的作用是___________ 。
(4)已知 分子中各原子均满足最外层8电子稳定结构,则1mol
分子中各原子均满足最外层8电子稳定结构,则1mol 含有
含有 键的个数为
键的个数为___________ ( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5) 的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为___________ 。哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。则
___________ (填“能”或“不能”)催化双氧水分解。
 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应 制取
制取 的
的 (俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(1)上述装置的正确连接顺序为
(2)装置A中所盛放的试剂是
①对m处导管进行加热 ②将m处导管加粗 ③持续通入氮气
(3)装置E中发生反应的离子方程式为
 的作用是
的作用是(4)已知
 分子中各原子均满足最外层8电子稳定结构,则1mol
分子中各原子均满足最外层8电子稳定结构,则1mol 含有
含有 键的个数为
键的个数为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(5)
 的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有________ ,其中能量较高的是________ 。(填标号)
A. B.
B. C.
C.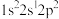 D.
D.
(2)基态Br原子的核外电子排布式为________ 。
(3) 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是________ ,中心离子的配位数为________ 。
(4)Kr是第四周期的稀有气体元素,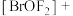 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为________ 。
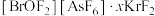 晶体中的微粒间作用力有
晶体中的微粒间作用力有________ (填标号)。
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在 形式,画出
形式,画出 的链状结构
的链状结构________ 。
(6)四氟乙烯 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为________ 和________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________ 。
(1)氟原子激发态的电子排布式有
A.
 B.
B. C.
C.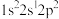 D.
D.
(2)基态Br原子的核外电子排布式为
(3)
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(4)Kr是第四周期的稀有气体元素,
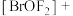 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为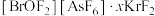 晶体中的微粒间作用力有
晶体中的微粒间作用力有a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在
 形式,画出
形式,画出 的链状结构
的链状结构(6)四氟乙烯
 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】铜及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)在元素周期表的分区中,铜属于_______ 区,与铜处于同一周期且最外层电子数相同的元素的基态原子共有_______ 种。
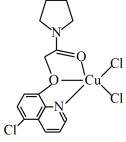
(2)CuCl2可与某有机多齿配体形成具有较强荧光性能的配合物,其结构简式如图所示。该配合物分子中N原子的杂化类型为_______ ,1mol该有机配体与Cu(II)形成的配位键为_______ mol。
(3)铜催化烯烃硝化反应时会产生NO 。键角:NO
。键角:NO
_______ NO (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。
(4)近期我国科学家合成了一种电化学性能优异的铜硒化合物,其晶胞结构如图所示。该铜硒化合物的化学式为_______ ,其中Cu元素以Cu+和Cu2+存在,则_______ (填“①”或“②”)为Cu2+,该晶体的密度为_______ g•cm-3(用含a和c的式子表示,设阿伏加德罗常数的值为NA,1nm=10-7cm)。

(1)在元素周期表的分区中,铜属于
(2)CuCl2可与某有机多齿配体形成具有较强荧光性能的配合物,其结构简式如图所示。该配合物分子中N原子的杂化类型为

(3)铜催化烯烃硝化反应时会产生NO
 。键角:NO
。键角:NO
 (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。(4)近期我国科学家合成了一种电化学性能优异的铜硒化合物,其晶胞结构如图所示。该铜硒化合物的化学式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】金属钨是重要的战略资源,由黑钨矿(主要成分为 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:

已知:常温下钨酸( )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。
回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第_____ 族。
(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先_____ ,“碱熔”过程 发生反应的化学方程式为
发生反应的化学方程式为_____ 。
(3)上述流程中加盐酸中和至 时,溶液中的杂质阴离子有
时,溶液中的杂质阴离子有 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为_____ 。
(4)沉钨过程中,判断 是否沉淀完全的方法是
是否沉淀完全的方法是_____ 。
(5)钨酸钙( ))和氢氧化钙都是微溶电解质。某温度下
))和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中,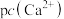 与pc(阴离子)的关系如图所示,已知:pc(离子)
与pc(阴离子)的关系如图所示,已知:pc(离子) (离子)。该温度下将
(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数
_____ 。

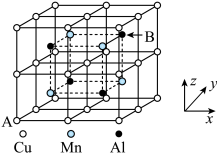
(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。该合金的化学式为_____ 。若A原子的坐标参数为 ,则B原子的坐标参数为
,则B原子的坐标参数为_____ 。
 、
、 ,含有少量Si、As的化合物)制取金属钨的流程如图所示:
,含有少量Si、As的化合物)制取金属钨的流程如图所示:
已知:常温下钨酸(
 )难溶于水,酸性很弱,其钠盐易溶于水。
)难溶于水,酸性很弱,其钠盐易溶于水。回答下列问题:
(1)已知元素周期表中74号元素钨与铬同族,钨在元素周期表中的位置是第六周期第
(2)“碱熔”步骤中为提高反应速率,可以将黑钨矿预先
 发生反应的化学方程式为
发生反应的化学方程式为(3)上述流程中加盐酸中和至
 时,溶液中的杂质阴离子有
时,溶液中的杂质阴离子有 、
、 、
、 等,则“氧化、净化”过程中,先加入
等,则“氧化、净化”过程中,先加入 发生反应的离子方程式为
发生反应的离子方程式为(4)沉钨过程中,判断
 是否沉淀完全的方法是
是否沉淀完全的方法是(5)钨酸钙(
 ))和氢氧化钙都是微溶电解质。某温度下
))和氢氧化钙都是微溶电解质。某温度下 和
和 的饱和溶液中,
的饱和溶液中,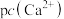 与pc(阴离子)的关系如图所示,已知:pc(离子)
与pc(阴离子)的关系如图所示,已知:pc(离子) (离子)。该温度下将
(离子)。该温度下将 溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数
溶液加入石灰乳中得到大量钨酸钙,该反应的平衡常数

(6)合金具有比金属单质更优越的性能,Cu-Mn-Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示。该合金的化学式为
 ,则B原子的坐标参数为
,则B原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钻可无限互溶,其固体为面心立方晶格。铂钻合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物CuF用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________________ 方法区分晶体、准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为________________ 。
(3) [H2F]+[SbF6]ˉ (氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______________ ,与[H2F]+具有相同空间构型且中心原子与F原子同周期的分子是_____________ 。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中心原子的杂化类型是
中心原子的杂化类型是____________ ;氟化铵中存在_______________ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
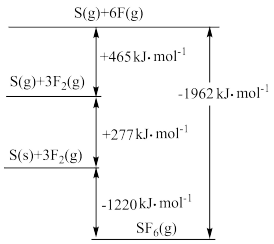
(5)SF4被广泛用作高压电气设备的绝缘介质。SF4是一种共价化合物,可通过类似于Bom-Haber循环能量构建能量图计算相关键能。则F-F键的键能为_____ kJ/mol,S-F键的键能为______ kJ/mol。
(6)CuCl的熔点为326℃,能升华,熔化呈液态时不导电;CuF的熔点为1008℃,熔化呈液态时能导电。
①CuF中Cu+的基态价电子排布式________ 铜元素位于元素周期________ 区,金属Cu的堆积模型为__________________ 。
②CuF的熔点比CuCl的高,原因是______________
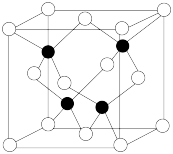
③已知NA为阿伏加 德罗常数的值,CuF的密度为7.1g/cm3,晶胞结构如图所示,则CuF的晶胞参数a=_______ nm(列出计算式)
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态F原子的价层电子排布图(轨道表达式)为
(3) [H2F]+[SbF6]ˉ (氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。
 中心原子的杂化类型是
中心原子的杂化类型是A.离子键 B.σ键 C.π键 D.氢键
(5)SF4被广泛用作高压电气设备的绝缘介质。SF4是一种共价化合物,可通过类似于Bom-Haber循环能量构建能量图计算相关键能。则F-F键的键能为

(6)CuCl的熔点为326℃,能升华,熔化呈液态时不导电;CuF的熔点为1008℃,熔化呈液态时能导电。
①CuF中Cu+的基态价电子排布式
②CuF的熔点比CuCl的高,原因是
③已知NA为阿伏加 德罗常数的值,CuF的密度为7.1g/cm3,晶胞结构如图所示,则CuF的晶胞参数a=

您最近一年使用:0次



