化学的特征之一是从微观的层面认识物质。通过结合元素周期表与周期律,建立“位置一结构一性质”思维模型,我们可以更好地认识物质世界。
(一)X、Y、Z、M、W、Q、R是分布在周期表中三个短周期的主族元素,已知其原子半径及主要化合价如下:
(1)X在周期表中的位置是_______ ;Y、Q各自形成的简单离子中,半径较大的是_______ (填离子符号)。W和R按原子个数比1:4构成的阳离子中所含的化学键类型为_______ 。
(2)M与Z相比,非金属性较强的是_______ (填元素名称),两元素最高价氧化物的水化物中,酸性较强的是_______ (填化学式)。
(二)周期表中位于斜对角线(左上与右下)的两种元素性质十分相似,称为对角线法则。如锂与镁、铍与铝等,其单质或化合物的性质可参照对角线法则进行认识。
(3)锂在空气中燃烧主要产物的电子式是_______ 。
(4)下列关于铍的判断正确的是( )
A.氧化铍的化学式为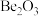 B.
B. 易溶于水
易溶于水
C. 是离子化合物 D.
是离子化合物 D.  具有两性
具有两性
(5) 和
和 可用试剂
可用试剂_______ 鉴别。
(一)X、Y、Z、M、W、Q、R是分布在周期表中三个短周期的主族元素,已知其原子半径及主要化合价如下:
| 元素代号 | X | Y(铝) | Z | M | W | Q | R |
| 原子半径/nm | 0.186 | 0.143 | 0.102 | 0.099 | 0.070 | 0.074 | 0.037 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
(2)M与Z相比,非金属性较强的是
(二)周期表中位于斜对角线(左上与右下)的两种元素性质十分相似,称为对角线法则。如锂与镁、铍与铝等,其单质或化合物的性质可参照对角线法则进行认识。
(3)锂在空气中燃烧主要产物的电子式是
(4)下列关于铍的判断正确的是
A.氧化铍的化学式为
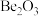 B.
B. 易溶于水
易溶于水C.
 是离子化合物 D.
是离子化合物 D.  具有两性
具有两性(5)
 和
和 可用试剂
可用试剂
更新时间:2021-04-01 14:19:32
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F为六种短周期主族元素,它们的原子序数依次增大;A元素的原子半径最小;B元素原子的最外层电子数是次外层电子数的3倍;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,D既可与C的最高价氧化物的水化物反应,也可与E的最高价氧化物的水化物反应,均有A元素的单质生成。请回答下列问题:
(1)写出F元素原子结构示意图_______ ,元素B在周期表中的位置______ 。
(2)判断C、D、E原子半径的大小顺序_____ (填写元素符号,下同),比较B和E的气态氢化物的稳定性大小____ 。
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式____ 。
(4)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式____ 。
(1)写出F元素原子结构示意图
(2)判断C、D、E原子半径的大小顺序
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式
(4)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E是原子序数依次增大的前四周期元素。
(1)写出下列元素的元素符号:A___________ ;E___________ 。
(2)B元素在周期表中的位置为___________ ,属于周期表的___________ 区。
(3)E元素基态原子的电子排布式:___________ 。
(4)B、C、D三种元素的电负性:___________ >___________ >___________ (填元素符号)。
| 元素 | 原子结构(基态)等 |
| A | 宇宙中含量最多的元素 |
| B | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| D | 原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对 |
| E | 前四周期元素中未成对电子数最多 |
(2)B元素在周期表中的位置为
(3)E元素基态原子的电子排布式:
(4)B、C、D三种元素的电负性:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)元素:A为___________ B为___________ C为___________ D为___________
(2)D在周期表中的位置第______ 周期,第________ 族;它的最高价氧化物对应的水化物:___________
(3)C与水反应的化学方程式是_________________________________ ,所得溶液显___________ (“酸性”或“碱性”)
(1)元素:A为
(2)D在周期表中的位置第
(3)C与水反应的化学方程式是
您最近一年使用:0次
【推荐1】中国科学院化学研究所有机固体院重点实验室合成了适用于非卤溶剂加工的“巨分子受体”,对于推动聚合物太阳电池受体光伏材料的发展具有重要意义。目前可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1) 在元素周期表中的位置为
在元素周期表中的位置为_______ ,其基态原子有_______ 种不同运动状态的电子。
(2)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为_______ ,其核外电子占据的最高能级的电子云轮廓图为_______ 。
(3)第一电子亲和能 是指基态的气态原子得到一个电子形成气态
是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
_______ (填“ ”或“
”或“ ”)
”)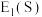 。
。
(4) 和
和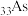 (与
(与 同主族)两种元素中第一电离能较大的是
同主族)两种元素中第一电离能较大的是_______ (填元素符号),试解释其原因:_______ 。
(5)根据对角线规则可知, 与铝在性质上具有相似性。已知
与铝在性质上具有相似性。已知 ,
, 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
(1)
 在元素周期表中的位置为
在元素周期表中的位置为(2)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为
(3)第一电子亲和能
 是指基态的气态原子得到一个电子形成气态
是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
 ”或“
”或“ ”)
”)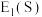 。
。(4)
 和
和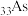 (与
(与 同主族)两种元素中第一电离能较大的是
同主族)两种元素中第一电离能较大的是(5)根据对角线规则可知,
 与铝在性质上具有相似性。已知
与铝在性质上具有相似性。已知 ,
, 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
(1)写出基态时J的价层电子排布式_____ ,L的原子序数为____ ,K的+2离子的价层电子的轨道表示式_____ 。
(2)下列关于元素在元素周期表中的位置的叙述正确的是_____。
(3)G元素最高价氧化物的水化物与E元素最高价氧化物的水化物的溶液反应的离子方程式是______ 。
(4)根据对角线规则及已知元素性质,推测A元素的单质与氧气在点燃时反应生成的物质为_______ (填化学式)。
(5)D的简单气态氢化物的 构型为
构型为______ ,它极易溶于水,原因是_______ 。
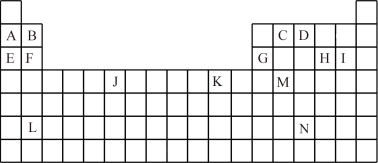
(1)写出基态时J的价层电子排布式
(2)下列关于元素在元素周期表中的位置的叙述正确的是_____。
| A.M位于元素周期表中第四周期ⅥA族,属于p区元素 |
| B.J位于元素周期表中第四周期ⅣB族,属于d区元素 |
| C.F位于元素周期表中第三周期ⅡA族,属于s区元素 |
| D.I位于元素周期表中第三周期ⅦA族,属于ds区元素 |
(3)G元素最高价氧化物的水化物与E元素最高价氧化物的水化物的溶液反应的离子方程式是
(4)根据对角线规则及已知元素性质,推测A元素的单质与氧气在点燃时反应生成的物质为
(5)D的简单气态氢化物的
 构型为
构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题。
(1)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质,下面给出14种元素的电负性。
①判断下列化合物中属于离子化合物的是________ (填字母);
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
②已知PCl3、NCl3均能发生水解反应,PCl3水解反应的化学方程式为__________________________ ;NCl3水解产物为____________________ 。
(2)观察Li、Be、Mg、Al在元素周期表中的位置回答:
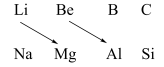
①铍的最高价氧化物的水化物是________ (填“酸性”、“碱性”或“两性”)化合物,证明这一结论的有关离子方程式是_____________________________________________________ ;
②根据Mg在空气中的燃烧情况,Li在空气中燃烧生成产物为__________ (用化学式表示)。
(3)现有核电荷数小于20的元素A,其电离能数据如下:(I1表示原子失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:1×102kJ·mol-1)
①外层电子离核越远,能量越高,电离能越__________ (填“大”或“小”);阳离子电荷数越高,失去电子时,电离能越________ (填“大”或“小”);
②上述11个电子分属________ 个电子层;
③失去了11个电子后,该元素还有________ 个电子;
④该元素最高价氧化物对应水化物的化学式是______________________________________ 。
(1)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质,下面给出14种元素的电负性。
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
①判断下列化合物中属于离子化合物的是
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
②已知PCl3、NCl3均能发生水解反应,PCl3水解反应的化学方程式为
(2)观察Li、Be、Mg、Al在元素周期表中的位置回答:

①铍的最高价氧化物的水化物是
②根据Mg在空气中的燃烧情况,Li在空气中燃烧生成产物为
(3)现有核电荷数小于20的元素A,其电离能数据如下:(I1表示原子失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:1×102kJ·mol-1)
| 序号 | I1 | I2 | I3 | I4 | I5 | I6 |
| 电离能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 |
| 序号 | I7 | I8 | I9 | I10 | I11 | …… |
| 电离能 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | …… |
①外层电子离核越远,能量越高,电离能越
②上述11个电子分属
③失去了11个电子后,该元素还有
④该元素最高价氧化物对应水化物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种短周期元素,A、B同主族,C、D同周期,B、E同周期。气体A2与气体C2混合后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B、C、E简单离子的核外电子排布相同。E的最高价氧化物可与B的最高价氧化物的水化物反应生成一种易溶于水的的盐,D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B两种元素的元素名称:A________ 、B________ 写出D的最高价氧化物的电子式__________ 。
(2)写出由B和C两元素形成的原子个数比为1:1的化合物F的电子式_________ ,其存在的化学键是_____ 。
(3)写出F和A2C反应的离子方程式:____________________ 。
(4)用电子式表示B2C形成的过程:______________________ 。
(1)写出A、B两种元素的元素名称:A
(2)写出由B和C两元素形成的原子个数比为1:1的化合物F的电子式
(3)写出F和A2C反应的离子方程式:
(4)用电子式表示B2C形成的过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示:
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)X单质分子的结构式是___________ ,Z元素原子最外层共有_____ 种不同运动状态的电子。
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是___________ 。
(3)常温时,W的硫酸盐溶液的pH_______ 7(填“=”、“>”或“<”),理由是:__________________________ (用离子方程式表示)。
(4)25℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6 kJ的热量,写出该反应的热化学方程式________________ 。
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X单质分子的结构式是
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是
(3)常温时,W的硫酸盐溶液的pH
(4)25℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6 kJ的热量,写出该反应的热化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】短周期元素 d、e、f、g、h、x 都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
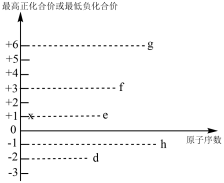
(1)由 x、e、d 三种元素组成的离子化合物的电子式为___________ 。
(2)d、e、f、g 元素形成的简单离子中半径由大到小的顺序是___________ (用化学式离子符号表示)。
(3)d 和 g 形成的简单氢化物中,沸点较高的是:___________ ,原因是:___________ 。
(4)x 和 d 组成的化合物中,既含有极性共价键又含有非极性共价键的是___________ (填 化学式),此化合物可将碱性工业废水中CN-氧化,生成碳酸盐和氨气,相应的 离子方程式为___________ 。

(1)由 x、e、d 三种元素组成的离子化合物的电子式为
(2)d、e、f、g 元素形成的简单离子中半径由大到小的顺序是
(3)d 和 g 形成的简单氢化物中,沸点较高的是:
(4)x 和 d 组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①______ ,⑥______ ,⑦______ 。
(2)画出原子的结构示意图:④________________ ,⑧_________________ 。
(3)在①~ 元素中,金属性最强的元素是
元素中,金属性最强的元素是_____ ,非金属性最强的元素是______ ,最不活泼的元素是_______ (均填元素名称)。
(4)元素③、⑩、 的氢氧化物碱性由强到弱的顺序
的氢氧化物碱性由强到弱的顺序________________ ;元素⑥、⑦、⑧的氢化物稳定性由弱到强的顺序______________________ (均用化学式填空)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |  |  |
(2)画出原子的结构示意图:④
(3)在①~
 元素中,金属性最强的元素是
元素中,金属性最强的元素是(4)元素③、⑩、
 的氢氧化物碱性由强到弱的顺序
的氢氧化物碱性由强到弱的顺序
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C三种短周期元素的简单离子A+、B3+、C2-具有相同的电子层结构,回答下列问题:
(1)C在元素周期表中的位置为____________ 。
(2)A+、B3+、C2-离子半径由大到小的顺序为_________________ (用离子符号表示)。
(3)A、B的最高价氧化物对应的水化物中,碱性较强的是____________ (填化学式);A、C的单质在加热条件下反应,所得产物与CO2反应的化学方程式为_____________________________ 。
(1)C在元素周期表中的位置为
(2)A+、B3+、C2-离子半径由大到小的顺序为
(3)A、B的最高价氧化物对应的水化物中,碱性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同,A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)B元素 在周期表中的位置___________ ,写出E最高价氧化物对应水化物的化学式___________ 。
(2)由B、C两种元素形成的含共价键的化合物的电子式为___________ ,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目___________
(3)写出E单质与A、B、C三种元素形成的化合物反应的离子方程式___________ 。
(4)A、B、C、D、E常见离子半径由大到小的顺序为___________ (用离子符号表示)。
(1)B元素 在周期表中的位置
(2)由B、C两种元素形成的含共价键的化合物的电子式为
(3)写出E单质与A、B、C三种元素形成的化合物反应的离子方程式
(4)A、B、C、D、E常见离子半径由大到小的顺序为
您最近一年使用:0次



