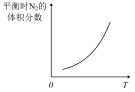
一定条件下,6H2(g)+2CO2(g)⇌C2H5OH(g)+3H2O(g),CO2平衡转化率随温度变化图所示。对a、b、c三点对应情况的分析,合理的是
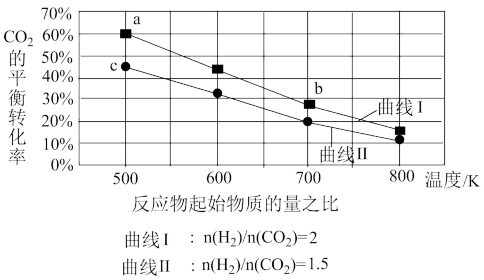

| A.CO2物质的量分数:a>b | B.C2H5OH物质的量分数:a<c |
| C.平衡常数:Ka>Kc>Kb | D.反应速率:va(CO2)<vb(CO2) |
更新时间:2021-04-01 23:09:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】T0温度下,向2L真空密闭容器中加入N2O3固体,发生反应:N2O3(s) NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是
NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是
 NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是
NO2(g)+X(g) (未配平),反应过程如图,下列说法正确的是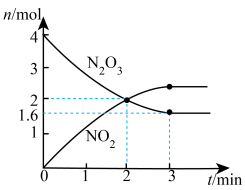
| A.X可能为N2 |
| B.0~2 min用N2O3表示的反应速率为1mol·min-1 |
| C.第2min时逆反应速率大于第4min时逆反应速率 |
| D.第4min时,保持温度和容积不变,向容器中再加入N2O3,混合气体颜色加深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】实验小组为探究反应: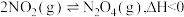 进行如下操作:在T℃(各物质均为气态)时,将一定量的
进行如下操作:在T℃(各物质均为气态)时,将一定量的 充入注射器中后封口,图乙是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列有关说法错误的是
充入注射器中后封口,图乙是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列有关说法错误的是

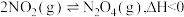 进行如下操作:在T℃(各物质均为气态)时,将一定量的
进行如下操作:在T℃(各物质均为气态)时,将一定量的 充入注射器中后封口,图乙是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列有关说法错误的是
充入注射器中后封口,图乙是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列有关说法错误的是
A.d点处: |
| B.由图乙可知注射器的移动轨迹为N→P→M |
C.若注射器隔热导致反应温度发生变化,则b、c两点的平衡常数 |
D.平衡时维持体积不变,再充入一定量 ,则 ,则 的物质的量分数比原来小 的物质的量分数比原来小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在容积为2L的刚性密闭容器中加入1molCO2和3molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。在其他条件不变的情况下,温度对反应的影响如图所示(注:T1、T2均大于300℃)。下列说法正确的是
CH3OH(g)+H2O(g)。在其他条件不变的情况下,温度对反应的影响如图所示(注:T1、T2均大于300℃)。下列说法正确的是

 CH3OH(g)+H2O(g)。在其他条件不变的情况下,温度对反应的影响如图所示(注:T1、T2均大于300℃)。下列说法正确的是
CH3OH(g)+H2O(g)。在其他条件不变的情况下,温度对反应的影响如图所示(注:T1、T2均大于300℃)。下列说法正确的是
| A.该反应在T1时的平衡常数比在T2时的小 |
B.处于A点的反应体系从T1变到T2,达到平衡时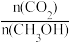 减小 减小 |
C.T2时,反应达到平衡时生成甲醇的反应速率v(CH3OH)=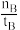 mol·L-1·min-1 mol·L-1·min-1 |
| D.T1时,若反应达到平衡后CO2的转化率为x,则容器内的压强与起始压强之比为(2-x)∶2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在t℃下,某反应达到平衡,平衡常数K=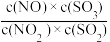 ,恒容时,温度升高,NO浓度减小。下列说法正确的是
,恒容时,温度升高,NO浓度减小。下列说法正确的是
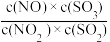 ,恒容时,温度升高,NO浓度减小。下列说法正确的是
,恒容时,温度升高,NO浓度减小。下列说法正确的是| A.该反应的焓变为正值 |
| B.K表达式中,c(SO3)指反应在该条件下达到化学平衡时SO3的物质的量浓度 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为:NO+SO3 NO2+SO2 NO2+SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在催化剂作用下,以 、
、 为原料合成
为原料合成 ,其主要反应有:
,其主要反应有:
反应1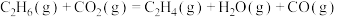
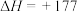 kJ·mol
kJ·mol
反应2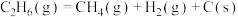
 kJ·mol
kJ·mol
将体积比为1∶1的 、
、 混合气体按一定流速通过催化反应管,测得
混合气体按一定流速通过催化反应管,测得 、
、 的转化率随温度变化的关系如图所示。
的转化率随温度变化的关系如图所示。 的选择性
的选择性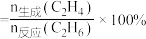
下列说法正确的是
 、
、 为原料合成
为原料合成 ,其主要反应有:
,其主要反应有:反应1
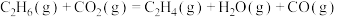
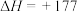 kJ·mol
kJ·mol
反应2
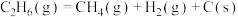
 kJ·mol
kJ·mol
将体积比为1∶1的
 、
、 混合气体按一定流速通过催化反应管,测得
混合气体按一定流速通过催化反应管,测得 、
、 的转化率随温度变化的关系如图所示。
的转化率随温度变化的关系如图所示。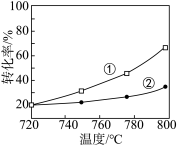
 的选择性
的选择性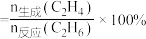
下列说法正确的是
A.图中曲线①表示 转化率随温度的变化 转化率随温度的变化 |
B.720~800℃范围内,随温度的升高,出口处 及 及 的量均增大 的量均增大 |
C.720~800℃范围内,随温度的升高, 的选择性不断增大 的选择性不断增大 |
D.其他条件不变,加入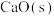 或选用高效催化剂,均能提高平衡时 或选用高效催化剂,均能提高平衡时 产率 产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于可逆反应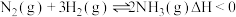 ,下列研究目的和示意图相符的是
,下列研究目的和示意图相符的是
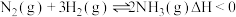 ,下列研究目的和示意图相符的是
,下列研究目的和示意图相符的是A | B | C | D | |
研究目的 | 压强(p)对反应的影响 | 压强(p)对平衡常数的影响 | 温度(T)对反应的影响 | 温度(T)对反应的影 |
示意图 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在20 L的密闭容器中按物质的量之比1∶2充入CO和H2,发生:CO(g)+2H2(g)  CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
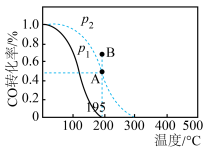
p2和 195℃时,n(H2)
 CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
p2和 195℃时,n(H2)
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
| A.0~3 min,平均速率v(CH3OH)=0.8 mol·L-1·min-1 |
| B.p1<p2,ΔH>0 |
| C.在p2和195 ℃时,该反应的平衡常数为25( mol·L-1)-2 |
| D.在B点时,v正>v逆 |
您最近一年使用:0次


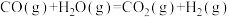 ,10 min后到达平衡,已知该温度下反应平衡常数是1.0,下列叙述正确的是
,10 min后到达平衡,已知该温度下反应平衡常数是1.0,下列叙述正确的是
 的物质的量分数小于12.5%
的物质的量分数小于12.5% ,重新达到平衡后K>1.0
,重新达到平衡后K>1.0