某兴趣小组对84消毒液的组成、性质与使用进行探究。所用试剂:84 消毒液(NaClO 浓度为 )、医用酒精(乙醇体积分数为
)、医用酒精(乙醇体积分数为 )
)
Ⅰ:探究84 消毒液的成分
(1)NaClO 溶液呈碱性的原因是_______ (用离子方程式表示)。
(2)常温下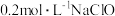 溶液的pH范围是
溶液的pH范围是_______ (填标号)。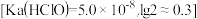
A.7.0~8.0 B.10.0~11.0 C.13.0~14.0
(3)实测该84消毒液 ,在瓶口能闻到刺激性气味。则该 84消毒液成分中,除了NaCl、NaClO,还含有
,在瓶口能闻到刺激性气味。则该 84消毒液成分中,除了NaCl、NaClO,还含有_______ (填化学式)。
(4)84消毒液露置于空气中,消毒效果先增强后降低。消毒效果增强的原因是_______ 。
Ⅱ:探究 84 消毒液能否与医用酒精混用 实验装置如图所示。

(5)导管 a 的作用是_______ 。
(6)①实验ⅰ的目的是_______ 。
②判断实验ⅱ中生成了 的依据是
的依据是_______ 。
(7)需补充以下实验ⅲ,才能说明反应中是否有 NaOH 生成。填写表中空白完成实验设计。
结论:医用酒精可与84消毒液发生反应并有少量 和NaOH 生成,二者不可混用。
和NaOH 生成,二者不可混用。
 )、医用酒精(乙醇体积分数为
)、医用酒精(乙醇体积分数为 )
)Ⅰ:探究84 消毒液的成分
(1)NaClO 溶液呈碱性的原因是
(2)常温下
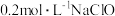 溶液的pH范围是
溶液的pH范围是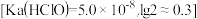
A.7.0~8.0 B.10.0~11.0 C.13.0~14.0
(3)实测该84消毒液
 ,在瓶口能闻到刺激性气味。则该 84消毒液成分中,除了NaCl、NaClO,还含有
,在瓶口能闻到刺激性气味。则该 84消毒液成分中,除了NaCl、NaClO,还含有(4)84消毒液露置于空气中,消毒效果先增强后降低。消毒效果增强的原因是
Ⅱ:探究 84 消毒液能否与医用酒精混用 实验装置如图所示。

| 序号 | 液体A | 液体B | 现象 |
| ⅰ |  ( (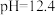 )的84消毒液 )的84消毒液 |  蒸馏水 蒸馏水 | 溶液中无明显现象;溶液 变为12.0; 变为12.0;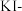 淀粉试纸在 淀粉试纸在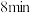 时变蓝, 时变蓝, 时蓝色完全褪去 时蓝色完全褪去 |
| ⅰ |  ( (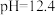 )的84消毒液 )的84消毒液 |  医用酒精 医用酒精 | 产生气泡,颜色无明显变化;溶液 升高到13.1, 升高到13.1,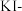 淀粉试纸在 淀粉试纸在 时变蓝, 时变蓝, 时蓝色完全褪去 时蓝色完全褪去 |
(6)①实验ⅰ的目的是
②判断实验ⅱ中生成了
 的依据是
的依据是(7)需补充以下实验ⅲ,才能说明反应中是否有 NaOH 生成。填写表中空白完成实验设计。
| 序号 | 液体A | 液体B | 现象 |
| ⅲ |  医用酒精 医用酒精 | 溶液 升高到12.6 升高到12.6 |
 和NaOH 生成,二者不可混用。
和NaOH 生成,二者不可混用。
2021·福建三明·二模 查看更多[2]
更新时间:2021-05-08 14:00:09
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】在25 ℃、100kPa时,在1L水中可溶解0.09mol氯气,实验测得溶于水的Cl2约有三分之一与水反应,假定溶液体积仍为1L。请回答下列问题:
(1)该反应的离子方程式为______________________________ ;
(2)该反应平衡常数的数值K约为____________________ ;估算所得氯水的pH =__________ (保留2位小数。已知lg3 ≈ 0.48)
(3)在上述平衡体系中加入少量NaOH固体,平衡将向________ 移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将______ 、溶液的pH将______ 、漂白性将_________ 。(填“增大”、“减小”或“不变”)
(1)该反应的离子方程式为
(2)该反应平衡常数的数值K约为
(3)在上述平衡体系中加入少量NaOH固体,平衡将向
(4)如果增大氯气的压强,氯气在水中的溶解度将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】利用所学化学反应原理,解决以下问题:
(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、NH4+、Cl一四种离子,且c(NH4+)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是_____________ 。
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:______________________ 。
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是_____________ 。
(4)以石墨电极电解100 mL 0.1 mol·L-1CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为__________ g。
(5)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如右图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=_______ mol·L-1.

(6)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+I2(g) 2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达到平衡时的数据如下表:
2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达到平衡时的数据如下表:

下列说法正确的是_______________ 。
(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、NH4+、Cl一四种离子,且c(NH4+)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是
(2)0.1 mol·L-1的氨水与0.05 mol·L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:
(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是
(4)以石墨电极电解100 mL 0.1 mol·L-1CuSO4溶液。若阳极上产生气体的物质的量为0.01 mol,则阴极上析出Cu的质量为
(5)向20 mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如右图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=

(6)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+I2(g)
 2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达到平衡时的数据如下表:
2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下,测得反应达到平衡时的数据如下表:
下列说法正确的是
A. + + =1 =1 | B.2 = = | C.a+b=14.9 | D.c1=c2=c3 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】实验室中有6瓶失去标签的白色固体:纯碱、氢氧化镁、氯化钡、硫酸铝、硫酸氢钠、氯化钾。除蒸馏水和试管、胶头滴管外,无其它任何试剂和仪器。某学生通过以下实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,观察到的现象以及被检出的一种物质是:______ ;
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三物质的化学式依次是______ ;
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为:______ ;
③在两两混合时,能确定BE成分的实验现象及结论是:______ ;
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式及其溶液显酸性的原因是______ 。
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,观察到的现象以及被检出的一种物质是:
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三物质的化学式依次是
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为:
③在两两混合时,能确定BE成分的实验现象及结论是:
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式及其溶液显酸性的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】铬及其化合物在催化、金属防腐等方面具有重要应用。
(1)催化剂 可由
可由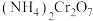 加热分解制备,反应同时生成无污染气体。
加热分解制备,反应同时生成无污染气体。
①完成化学方程式: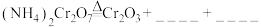 。
。______
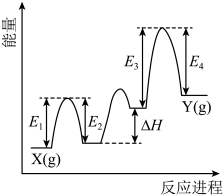
②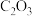 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为_______ (列式表示)。
③ 可用于
可用于 的催化氧化。设计从
的催化氧化。设计从 出发经过3步反应制备
出发经过3步反应制备 的路线
的路线_______ (用“→”表示含氮物质间的转化,例如 ,并在箭头上标注其他反应物):其中一个有颜色变化的反应的化学方程式为
,并在箭头上标注其他反应物):其中一个有颜色变化的反应的化学方程式为_______ 。
(2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(ⅰ) Cr2O (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq)
(aq)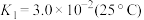
(ⅱ) HCr O (aq)
(aq)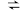 Cr O
Cr O (aq)+H+(aq)
(aq)+H+(aq)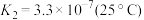
①下列有关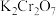 溶液的说法正确的有
溶液的说法正确的有________
A.加入少量硫酸,溶液的 不变
不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量 溶液,反应(ⅰ)的平衡逆向移动
溶液,反应(ⅰ)的平衡逆向移动
D.加入少量 固体,平衡时
固体,平衡时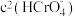 与
与 的比值保持不变
的比值保持不变
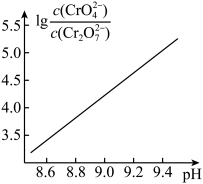
② 时,
时,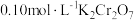 ,溶液中
,溶液中 随
随 的变化关系如图。当
的变化关系如图。当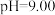 时,设
时,设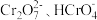 与
与 的平衡浓度分别为
的平衡浓度分别为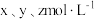 ,则x、y、z之间的关系式为
,则x、y、z之间的关系式为_______ =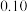 。
。
(1)催化剂
 可由
可由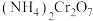 加热分解制备,反应同时生成无污染气体。
加热分解制备,反应同时生成无污染气体。①完成化学方程式:
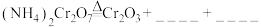 。
。②
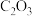 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为
③
 可用于
可用于 的催化氧化。设计从
的催化氧化。设计从 出发经过3步反应制备
出发经过3步反应制备 的路线
的路线 ,并在箭头上标注其他反应物):其中一个有颜色变化的反应的化学方程式为
,并在箭头上标注其他反应物):其中一个有颜色变化的反应的化学方程式为(2)
 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:(ⅰ) Cr2O
 (aq)+H2O(l)
(aq)+H2O(l) 2HCrO
2HCrO (aq)
(aq)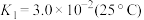
(ⅱ) HCr O
 (aq)
(aq)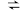 Cr O
Cr O (aq)+H+(aq)
(aq)+H+(aq)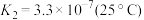
①下列有关
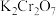 溶液的说法正确的有
溶液的说法正确的有A.加入少量硫酸,溶液的
 不变
不变B.加入少量水稀释,溶液中离子总数增加
C.加入少量
 溶液,反应(ⅰ)的平衡逆向移动
溶液,反应(ⅰ)的平衡逆向移动D.加入少量
 固体,平衡时
固体,平衡时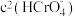 与
与 的比值保持不变
的比值保持不变②
 时,
时,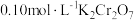 ,溶液中
,溶液中 随
随 的变化关系如图。当
的变化关系如图。当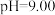 时,设
时,设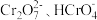 与
与 的平衡浓度分别为
的平衡浓度分别为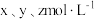 ,则x、y、z之间的关系式为
,则x、y、z之间的关系式为 。
。
您最近一年使用:0次



