实验室中有6瓶失去标签的白色固体:纯碱、氢氧化镁、氯化钡、硫酸铝、硫酸氢钠、氯化钾。除蒸馏水和试管、胶头滴管外,无其它任何试剂和仪器。某学生通过以下实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,观察到的现象以及被检出的一种物质是:______ ;
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三物质的化学式依次是______ ;
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为:______ ;
③在两两混合时,能确定BE成分的实验现象及结论是:______ ;
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式及其溶液显酸性的原因是______ 。
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,观察到的现象以及被检出的一种物质是:
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三物质的化学式依次是
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为:
③在两两混合时,能确定BE成分的实验现象及结论是:
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式及其溶液显酸性的原因是
11-12高三上·广东茂名·期末 查看更多[1]
(已下线)2011届广东省高州市大井中学高三上学期期末考试(理综)化学部分
更新时间:2016/12/09 01:28:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D四种化合物,分别由K+、Ba2+、SO 、CO
、CO 、OH-中两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D、E的化学式。
A____________ ;B_____________ ;C_____________ ;D______________ ;E______________ ;
(2)写出下列反应的离子方程式。
D与硫酸反应_____________ 。
B与盐酸反应_____________ ;
C与硫酸反应_____________ ;
 、CO
、CO 、OH-中两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(1)推断A、B、C、D、E的化学式。
A
(2)写出下列反应的离子方程式。
D与硫酸反应
B与盐酸反应
C与硫酸反应
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】四只试剂瓶中分别盛有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,就如何检验这四种溶液分别解答下列各题。在四支试管中分别取四种溶液各1mL,做下列实验。
(1)在四支试管中分别滴入___________ ,出现__________ (现象)的是____________ ,离子方程式是_____________ 。
(2)在剩余三支试管中分别滴入___________ ,出现__________ (现象)的是____________ ,离子方程式是______________ 。
(3)在剩余两支试管中分别滴入___________ ,出现__________ (现象)的是____________ ,离子方程式是___________ 。
(4)三次实验中都没有明显现象的是____________ 。
(1)在四支试管中分别滴入
(2)在剩余三支试管中分别滴入
(3)在剩余两支试管中分别滴入
(4)三次实验中都没有明显现象的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。请回答:
(1)写出化学式:A__________ ; C________ ;D_________ ;
(2)写出下列反应的离子方程式。
B与盐酸反应__________ ;
E与过量的澄清石灰水反应__________ 。
(1)写出化学式:A
(2)写出下列反应的离子方程式。
B与盐酸反应
E与过量的澄清石灰水反应
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】在一定条件下,单质B、C、D、E都能与A单质发生化合反应,转化关系如图所示。已知:①G是黑色晶体,能吸附B单质;②H能与氢氧化钠溶液或盐酸反应;③实验时在G和C的混合物表面加入某强氧化剂粉末,在表面上插入一根除去氧化膜的E片,点燃E引发G与C的反应;④I是绿色植物光合作用的原料,温室中常用它作肥料。根据上述信息,回答下列问题:
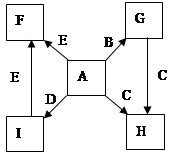

(1)I的电子式为____________ ,G的俗名是_____________ 。
(2)以C和E为电极在NaOH溶液中构成原电池,该原电池的负极反应式为________ 。
(3)根据E和A反应的能量变化图像写出热化学方程式:_______________ 。
(4)两种常见含C元素的盐,一种pH>7,另一种pH<7,写出这两种溶液混合时发生反应的离子方程式:____________________ ;
(5)写出B在高温下和水蒸气反应的化学方程式并标出电子转移方向和总数________ 。
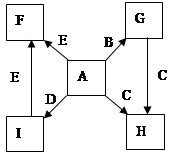

(1)I的电子式为
(2)以C和E为电极在NaOH溶液中构成原电池,该原电池的负极反应式为
(3)根据E和A反应的能量变化图像写出热化学方程式:
(4)两种常见含C元素的盐,一种pH>7,另一种pH<7,写出这两种溶液混合时发生反应的离子方程式:
(5)写出B在高温下和水蒸气反应的化学方程式并标出电子转移方向和总数
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】正盐A、B均含有三种元素。且所含元素种类相同。24.5g的A在加热条件下发生如图变化。已知:生成的标况下2.24L的气体D,能使得火星的水条复燃。透过蓝色钴玻璃,A、B、C的焰色实验均为紫色,往C的溶液中加入AgNO3溶液,出现白色沉淀。再加入稀硝酸,沉淀不溶解,且质量称得为14.35g。请回答:

(1)D的物质的量为____________ mol,C的化学式为____________ 。
(2)写出A分解的化学方程式______________ 。

(1)D的物质的量为
(2)写出A分解的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有X、Y、Z三种物质,它们之间存在如下转化关系:
(1)若X、Y、Z三种物质的焰色反应均为黄色,三个反应均为化合反应,则Y的化学式为_________ ,Z的电子式为_________ ;Y、Z两种物质相比,相同的化学键类型为__________ ,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为________ 。
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1 mol/L的三种物质的溶液pH:Y>X>Z>7,则①的化学方程式为___________________ ,③的离子方程式为__________________ 。
(3)若X、Y、Z三种物质均含有同一种金属元素,X是单质,Y是日常生活中最重要的盐,②的反应条件为电解,则②的化学方程式为_________________ ,③的离子方程式为________ 。
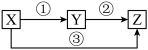
(1)若X、Y、Z三种物质的焰色反应均为黄色,三个反应均为化合反应,则Y的化学式为
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1 mol/L的三种物质的溶液pH:Y>X>Z>7,则①的化学方程式为
(3)若X、Y、Z三种物质均含有同一种金属元素,X是单质,Y是日常生活中最重要的盐,②的反应条件为电解,则②的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
Ⅰ.室温下,用 的
的 溶液分别滴定均为
溶液分别滴定均为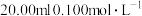 的
的 溶液和醋酸溶液,滴定曲线如图所示。
溶液和醋酸溶液,滴定曲线如图所示。
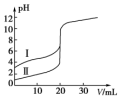
(1)在滴加过程中,稀醋酸溶液中水的电离程度_______ (填“增大”、“减小”、“不变”、“先增大后减小”或“先减小后增大”)。
(2) 和醋酸的酸性强弱为:
和醋酸的酸性强弱为:
_______  (填“强于”、“弱于”)。
(填“强于”、“弱于”)。
(3)用等式表示滴定过程中曲线Ⅱ溶液中所有离子的浓度关系_______ 。
Ⅱ.氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用 '酸性
'酸性 ,溶液滴定未知浓度的无色
,溶液滴定未知浓度的无色 溶液。请完成下列问题:
溶液。请完成下列问题:
(1)请写出酸性 溶液与
溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(2)该滴定实验所需仪器为下列中的_______ (填字母)。
A.酸式滴定管( ) B.碱式滴定管(
) B.碱式滴定管( ) C.量筒(
) C.量筒( ) D.锥形瓶 E.铁架台 F.滴定管夹G.烧杯 H.白纸 I.胶头滴管 J.漏斗
) D.锥形瓶 E.铁架台 F.滴定管夹G.烧杯 H.白纸 I.胶头滴管 J.漏斗
(3)不用_______ (填“酸”或“碱”)式滴定管盛放高锰酸钾溶液,原因是_______ 。
(4)该实验选何种指示剂,说明理由:_______ 。
(5)滴定前平视 溶液液面,刻度为
溶液液面,刻度为 ,滴定后俯视液面刻度为
,滴定后俯视液面刻度为 ,则
,则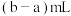 比实际消耗
比实际消耗 溶液体积
溶液体积_______ (填“大”或“小”)。根据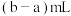 计算得到的待测溶液浓度比实际浓度
计算得到的待测溶液浓度比实际浓度_______ (填“大”或“小”)。
Ⅰ.室温下,用
 的
的 溶液分别滴定均为
溶液分别滴定均为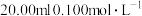 的
的 溶液和醋酸溶液,滴定曲线如图所示。
溶液和醋酸溶液,滴定曲线如图所示。 
(1)在滴加过程中,稀醋酸溶液中水的电离程度
(2)
 和醋酸的酸性强弱为:
和醋酸的酸性强弱为:
 (填“强于”、“弱于”)。
(填“强于”、“弱于”)。(3)用等式表示滴定过程中曲线Ⅱ溶液中所有离子的浓度关系
Ⅱ.氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用
 '酸性
'酸性 ,溶液滴定未知浓度的无色
,溶液滴定未知浓度的无色 溶液。请完成下列问题:
溶液。请完成下列问题: (1)请写出酸性
 溶液与
溶液与 溶液反应的离子方程式:
溶液反应的离子方程式:(2)该滴定实验所需仪器为下列中的
A.酸式滴定管(
 ) B.碱式滴定管(
) B.碱式滴定管( ) C.量筒(
) C.量筒( ) D.锥形瓶 E.铁架台 F.滴定管夹G.烧杯 H.白纸 I.胶头滴管 J.漏斗
) D.锥形瓶 E.铁架台 F.滴定管夹G.烧杯 H.白纸 I.胶头滴管 J.漏斗(3)不用
(4)该实验选何种指示剂,说明理由:
(5)滴定前平视
 溶液液面,刻度为
溶液液面,刻度为 ,滴定后俯视液面刻度为
,滴定后俯视液面刻度为 ,则
,则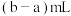 比实际消耗
比实际消耗 溶液体积
溶液体积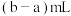 计算得到的待测溶液浓度比实际浓度
计算得到的待测溶液浓度比实际浓度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】研究电解质在水溶液中的离子反应与平衡有重要的意义。常温下,用0.1 mol/L NaOH溶液滴定10 mL 0.1 mol/L CH3COOH溶液的滴定曲线如图所示。
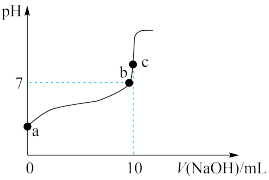
(1)a点溶液的pH________ 1(填“>”、“<”或“=”)。醋酸的电离平衡常数 表达式为___________________________ 。
(2)现有0.1 mol/L NaOH溶液,该溶液中c(OH-)≈_______________ ,其中水电离产生的c(H+)=_______________ ,水电离产生的c(OH-)=____________ ,该溶液的pH为__________ 。
(3)b点溶液中,存在的电荷守恒关系式为______________ ,因此时混合液pH=7,则溶液中c(H+)为______________ ,其中c(Na+) ________ c(CH3COO−)(填“>”、“<”或“=”)。
(4)c点溶液中,c(Na+)________ [c(CH3COO−) + c(CH3COOH)](填“>”、“<”或“=”,下同),此时溶液中c(H+)_____________ c(OH-)。
(5)比较a、c两点水的电离程度:a___ c,并分别解释原因 a:__________ ,c__________ 。

(1)a点溶液的pH
(2)现有0.1 mol/L NaOH溶液,该溶液中c(OH-)≈
(3)b点溶液中,存在的电荷守恒关系式为
(4)c点溶液中,c(Na+)
(5)比较a、c两点水的电离程度:a
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】填空。
(1)某温度时,水的Kw=1×10-15,则该温度_______ (填“低于”“高于”或“等于”)25℃。该温度下,c(H+)=1×10-7mol·L-1的溶液呈_______ (填“酸性”“碱性”或“中性”);将pH=2的硫酸与pH=14的KOH溶液混合后溶液pH=13,需氢氧化钾和硫酸的体积比为_______ 。
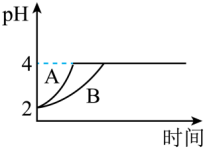
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量Zn粒,反应过程中两溶液pH变化如图,图中表示醋酸溶液中pH变化曲线_______ (填“A”或“B”);设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1_______ m2(选填“<”、“=”、“>”)。
(3)实验表明,液态时纯硫酸的电离能力强于纯硝酸,纯硫酸的导电性也显著强于纯水。又知液态纯酸都像水那样进行自身电离(H2O+H2O H3O++OH—)而建立平衡,且在一定温度下都有各自的离子积常数。据此回答:
H3O++OH—)而建立平衡,且在一定温度下都有各自的离子积常数。据此回答:
①纯硫酸在液态时自身电离的方程式是_______ 。
②25℃时,液态纯硫酸的离子积常数K(H2SO4)_______ (填“>”“<”或“=”)1×10-14。
③在纯硫酸与纯硝酸的液态混合酸中,存在最多的阴离子是_______ 。
(4)25℃时不断将水滴入0.1 mol/L的氨水中,下列图像变化合理的是_______。
(5)常温下,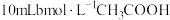 溶液与
溶液与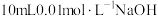 溶液充分反应后,溶液
溶液充分反应后,溶液 ,则
,则 的电离常数Ka=
的电离常数Ka=________ (用含 的代数式表示)。
的代数式表示)。
(1)某温度时,水的Kw=1×10-15,则该温度
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量Zn粒,反应过程中两溶液pH变化如图,图中表示醋酸溶液中pH变化曲线

(3)实验表明,液态时纯硫酸的电离能力强于纯硝酸,纯硫酸的导电性也显著强于纯水。又知液态纯酸都像水那样进行自身电离(H2O+H2O
 H3O++OH—)而建立平衡,且在一定温度下都有各自的离子积常数。据此回答:
H3O++OH—)而建立平衡,且在一定温度下都有各自的离子积常数。据此回答:①纯硫酸在液态时自身电离的方程式是
②25℃时,液态纯硫酸的离子积常数K(H2SO4)
③在纯硫酸与纯硝酸的液态混合酸中,存在最多的阴离子是
(4)25℃时不断将水滴入0.1 mol/L的氨水中,下列图像变化合理的是_______。
A.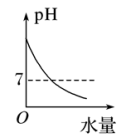 | B.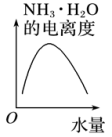 | C.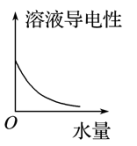 | D.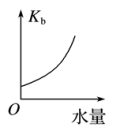 |
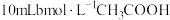 溶液与
溶液与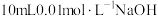 溶液充分反应后,溶液
溶液充分反应后,溶液 ,则
,则 的电离常数Ka=
的电离常数Ka= 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在:钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)工艺流程如下:
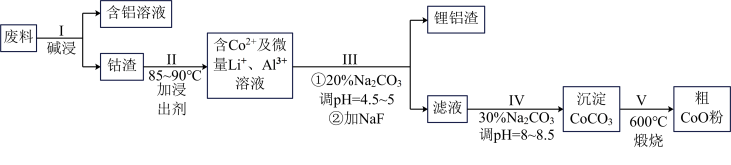
(1)过程Ⅰ中采用NaOH溶液溶出废料中的Al,反应的离子方程式为_________________ 。
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为 (产物中只有一种酸根)_________ 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从氧化还原和环境保护的角度分析不用盐酸浸出钴的主要原因____ 。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式_____ 。
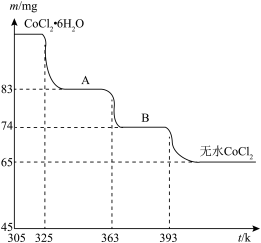
(4)如图是CoCl2.6H2O晶体受热分解时,剩余固体的质量随温度变化的曲线,B物质的化学式是______________ 。

(1)过程Ⅰ中采用NaOH溶液溶出废料中的Al,反应的离子方程式为
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为 (产物中只有一种酸根)
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式
(4)如图是CoCl2.6H2O晶体受热分解时,剩余固体的质量随温度变化的曲线,B物质的化学式是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面:锂混杂于其中。(已知Co2O3的氧化性>Cl2的氧化性)从废料中回收氧化钴(CoO)的工艺流程如下:
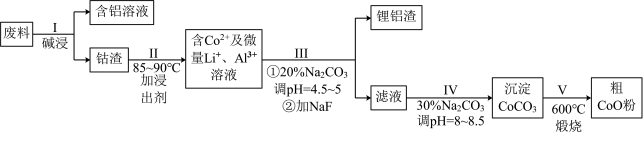
已知:①CoCO3的溶度积为:Ksp=1.0×10-13;
②溶液中离子浓度小于1.0×10-5mol/L时认为该离子沉淀完全。
(1)“碱溶”前通常将废料粉碎,其目的是____________ 。
(2)过程I中采用NaOH溶液溶出废料中的A1,反应的离子方程式为_________________ 。
(3)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出含钻物质的反应化学方程式为 (产物中只有一种酸根)_______________________________________ 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因______________________________________ 。
(4)过程III得到锂铝渣的主要成分是LiF和AI(OH)3,碳酸钠溶液在产生 Al(OH)3时起重要作用,请写出该反应的离子方程式__________________________________ 。
(5)将2.0×10-4 mol/LCoSO4与2.2×10-4mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为__________ ,Co2+是否沉淀完全? __________ (填“是”或“否”)。
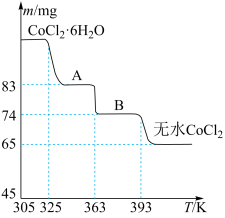
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,物质B的化学式是____________________ 。

已知:①CoCO3的溶度积为:Ksp=1.0×10-13;
②溶液中离子浓度小于1.0×10-5mol/L时认为该离子沉淀完全。
(1)“碱溶”前通常将废料粉碎,其目的是
(2)过程I中采用NaOH溶液溶出废料中的A1,反应的离子方程式为
(3)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出含钻物质的反应化学方程式为 (产物中只有一种酸根)
(4)过程III得到锂铝渣的主要成分是LiF和AI(OH)3,碳酸钠溶液在产生 Al(OH)3时起重要作用,请写出该反应的离子方程式
(5)将2.0×10-4 mol/LCoSO4与2.2×10-4mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,物质B的化学式是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)工业制胆矾时,将粗制 粉末(含
粉末(含 、
、 杂质)慢慢加入适量的稀
杂质)慢慢加入适量的稀 中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。
中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。
已知: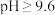 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: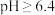 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: 接近4时,
接近4时, 以
以 的形式完全沉淀.回答下列问题:
的形式完全沉淀.回答下列问题:
①为除去 ,可先加入
,可先加入________ ,(填编号)将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为________________ ,后加入适当的________ (填编号)调节溶液的 使
使 沉淀。
沉淀。
A. B.
B. C.
C. D.
D.
②甲同学怀疑调整溶液 接近4是否能达到除去
接近4是否能达到除去 而不损失
而不损失 的目的,已知,常温下
的目的,已知,常温下 的溶度积
的溶度积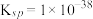 ,
, 的溶度积
的溶度积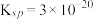 ,设溶液中
,设溶液中 的浓度为
的浓度为 ,则
,则 开始沉淀时溶液的
开始沉淀时溶液的 为
为________ , 完全沉淀时溶液的的
完全沉淀时溶液的的 为
为________ ,通过计算确定上述方案________ (填“可行”或“不可行”).
③ ,
, 溶液中由水电离出的
溶液中由水电离出的 是
是________ 。
(2)SOCl2是一种液态化合物,将其滴入水中,反应剧烈,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
①根据实验现象,写出SOCl2和H2O反应的化学方程式:________________ 。
②利用SOCl2和AlCl3•6H2O混合共热可制备无水AlCl3,试解释原因________________ 。
(1)工业制胆矾时,将粗制
 粉末(含
粉末(含 、
、 杂质)慢慢加入适量的稀
杂质)慢慢加入适量的稀 中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。
中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。已知:
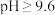 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: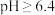 时,
时, 以
以 的形式完全沉淀:
的形式完全沉淀: 接近4时,
接近4时, 以
以 的形式完全沉淀.回答下列问题:
的形式完全沉淀.回答下列问题:①为除去
 ,可先加入
,可先加入 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为 使
使 沉淀。
沉淀。A.
 B.
B. C.
C. D.
D.
②甲同学怀疑调整溶液
 接近4是否能达到除去
接近4是否能达到除去 而不损失
而不损失 的目的,已知,常温下
的目的,已知,常温下 的溶度积
的溶度积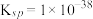 ,
, 的溶度积
的溶度积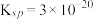 ,设溶液中
,设溶液中 的浓度为
的浓度为 ,则
,则 开始沉淀时溶液的
开始沉淀时溶液的 为
为 完全沉淀时溶液的的
完全沉淀时溶液的的 为
为③
 ,
, 溶液中由水电离出的
溶液中由水电离出的 是
是(2)SOCl2是一种液态化合物,将其滴入水中,反应剧烈,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
①根据实验现象,写出SOCl2和H2O反应的化学方程式:
②利用SOCl2和AlCl3•6H2O混合共热可制备无水AlCl3,试解释原因
您最近一年使用:0次



