下列说法正确的是
A.金刚石、石墨、 互为同位素 互为同位素 |
B.金属钠能置换出 溶液中 溶液中 |
C.催化剂能提高合成氨反应中 的平衡转化率 的平衡转化率 |
D.由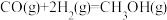 能自发进行可得出 能自发进行可得出 |
更新时间:2021-05-14 15:51:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是( )
| A.金属Na着火时立即用水或泡沫灭火剂来灭火 |
| B.任何金属元素灼烧时都有焰色反应,钾元素的焰色用肉眼直接看到的是紫色。 |
| C.铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 |
| D.除去Na2CO3溶液中的NaHCO3溶液可以用加热的方法除去 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作规范且能达到目的是
| 实验目的 | 实验操作 | |
| A | 称取2.0gNaOH固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
| B | 配制 的 的 溶液 溶液 | 称取 固体1.580g,放入100mL容量瓶中,加水稀释到刻度线 固体1.580g,放入100mL容量瓶中,加水稀释到刻度线 |
| C | 证明Na2O2与水反应放热 | Na2O2用棉花包裹后滴几滴水,棉花燃烧,说明该反应放出热量 |
| D | 比较钠、铁的活泼性 | 把钠块投入FeCl2溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验装置不能达到实验目的是
| A. 验证Na和水反应是否为放热反应 | B. 用 做喷泉实验 做喷泉实验 | C. 观察纯碱的焰色反应 | D. 比较 、 、 的稳定性 的稳定性 |
 | 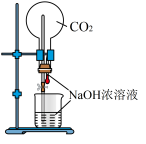 |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】N2O是一种温室气体,易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。在N2O中加入少量碘蒸气反应机理为:
①I2(g)=2I(g)(快反应)
②I(g)+N2O(g)=N2(g)+IO(g)(慢反应)
③2IO(g)+N2O(g)=N2(g)+ O2(g)+I2(g)(快反应)
O2(g)+I2(g)(快反应)
下列叙述错误的是
①I2(g)=2I(g)(快反应)
②I(g)+N2O(g)=N2(g)+IO(g)(慢反应)
③2IO(g)+N2O(g)=N2(g)+
 O2(g)+I2(g)(快反应)
O2(g)+I2(g)(快反应)下列叙述错误的是
| A.升高温度,反应①正向进行程度大 | B.反应②的活化能比反应③大 |
| C.碘蒸气可以提高N2O的分解率 | D.N2O的分解速率由反应②决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定条件下,在体积固定为 的密闭容器中加入
的密闭容器中加入
 发生反应:
发生反应: ,则下图中正确的是(
,则下图中正确的是(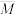 表示混合气体的平均相对分子质量)
表示混合气体的平均相对分子质量)
 的密闭容器中加入
的密闭容器中加入
 发生反应:
发生反应: ,则下图中正确的是(
,则下图中正确的是(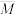 表示混合气体的平均相对分子质量)
表示混合气体的平均相对分子质量)A.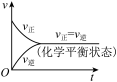 | B.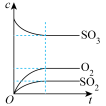 | C. | D.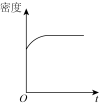 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在某恒容的密闭容器中发生反应: ,在200℃和T℃时,X的浓度(mol/L)随时间变化的有关实验数据见下表,下列有关叙述正确的是
,在200℃和T℃时,X的浓度(mol/L)随时间变化的有关实验数据见下表,下列有关叙述正确的是
 ,在200℃和T℃时,X的浓度(mol/L)随时间变化的有关实验数据见下表,下列有关叙述正确的是
,在200℃和T℃时,X的浓度(mol/L)随时间变化的有关实验数据见下表,下列有关叙述正确的是| 时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 200℃ | 0.80 | 0.55 | 0.35 | 0.20 | 0.15 | 0.15 |
| T℃ | 1.00 | 0.65 | 0.35 | 0.18 | 0.18 | 0.18 |
| A.在200℃下,0~4min内用Y表示的化学反应速率为0.1125 mol•L﹣1•min﹣1 |
| B.根据上表内数据可得出结论,其它条件相同,反应物浓度越大,反应速率越大 |
| C.在T℃下,6min时反应刚好达到平衡状态 |
| D.从表中可知:T<200℃ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
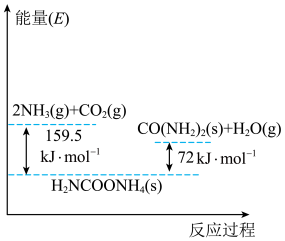
【推荐1】以CO2和NH3为原料合成尿素反应分两步完成,ⅰ. CO2和NH3生成H2NCOONH4;ⅱ. H2NCOONH4分解生成尿素,总反应为: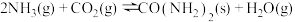 △H。反应过程能量变化如图。下列说法错误的是
△H。反应过程能量变化如图。下列说法错误的是
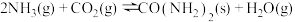 △H。反应过程能量变化如图。下列说法错误的是
△H。反应过程能量变化如图。下列说法错误的是
| A.第一步ΔS<0 |
| B.第二步活化能大于第一步 |
| C.△H =+87.5 kJ∙mol-1 |
| D.升高温度,总反应反应物活化分子百分数增大,反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在工业生产中,对能够发生的化学反应,研究和选择合适的反应条件才有实际意义。恒温恒压下,下列过程一定不能自发进行的是
| A.4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)△H<0 |
| B.CaO(s)+CO2(g)=CaCO3(s)△H<0 |
| C.2N2O5(g)=4NO2(g)+O2(g)△H>0 |
| D.2H2O(1)+O2(g)=2H2O2(aq)△H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
| A.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| B.改变温度对放热反应的影响程度大 |
| C.反应2C(s) + SiO2(s) == Si (s) + 2CO(g) △H > 0 是在高温下的自发反应 |
| D.分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支试管加入少量MnO2,可以研究催化剂对H2O2分解速率的影响 |
您最近一年使用:0次



