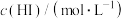某同学设计实验探究镁与铵盐溶液的反应,仔细分析以下记录后,所得结论正确的是
| 实验编号 | ① | ② | ③ | ④ |
| 溶液种类 |   |   |   |  |
m( )/g )/g | 0.48 | 0.48 | 0.48 | 0.48 |
| V(溶液)/mL | 100 | 100 | 100 | 100 |
| 实验现象 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 几乎看不到现象 |
6h时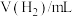 | 433 | 255 | 347 | 12 |
A.实验中产生的气体仅为 ,沉淀为 ,沉淀为 |
B.由实验①②可得,溶液中阴离子的浓度或种类对产生 的速率有影响 的速率有影响 |
C.由实验①③可得,溶液中 越大,反应速率越快 越大,反应速率越快 |
D.由实验①~④可得,溶液的 越小,产生 越小,产生 的速率越快 的速率越快 |
20-21高二下·四川乐山·期末 查看更多[4]
(已下线)第06讲 影响化学反应速率的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)四川省乐山市2020-2021学年高二下学期期末考试化学试题
更新时间:2021-07-06 11:37:32
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】某学习小组同学研究过氧化氢溶液与氢碘酸(HI)反应: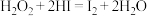 ,室温下的实验数据如下表。已知:该反应的速率方程可表示为
,室温下的实验数据如下表。已知:该反应的速率方程可表示为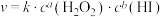 ;
;
下列有关说法不正确 的是
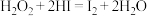 ,室温下的实验数据如下表。已知:该反应的速率方程可表示为
,室温下的实验数据如下表。已知:该反应的速率方程可表示为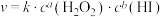 ;
;实验编号 | ① | ② | ③ | ④ | ⑤ |
| 0.1 | 0.1 | 0.1 | 0.2 | 0.3 |
| 0.1 | 0.2 | 0.3 | 0.1 | 0.1 |
从混合至溶液出现棕黄色的时间/s | 13 | 6.5 | 4.3 | 6.5 | 4.3 |
A.实验①进行 后测得 后测得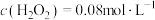 ,则 ,则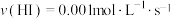 |
B.由编号为①②③的实验数据可知,当 浓度不变时,增大HI浓度,该反应速率加快 浓度不变时,增大HI浓度,该反应速率加快 |
C.对比表中数据, , , |
| D.将实验⑤的温度升高,溶液出现棕黄色时间变长,可能是温度升高使双氧水分解 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验方案设计正确的是
| 编号 | 目的 | 方案设计 |
| A | 检验固体试样中有 | 在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润红色石蕊试纸变蓝的气体,该固体试样中不可能存在 |
| B | 探究S与Cl的金属性强弱 | 向NaHS溶液中滴入稀盐酸,观察是否有生成臭鸡蛋气味气体( )。 )。 |
| C | 探究浓度对化学反应速率的影响 | 向两支试管分别加入 和 和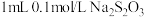 溶液,向盛有 溶液,向盛有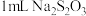 溶液试管中加入 溶液试管中加入 蒸馏水,再同时向两支试管中加 蒸馏水,再同时向两支试管中加 ,收集生成的 ,收集生成的 气体,比较生成气体的多少 气体,比较生成气体的多少 |
| D | 探究 的还原性 的还原性 | 在试管中加入少量酸性 溶液,然后向试管中逐滴加入 溶液,然后向试管中逐滴加入 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
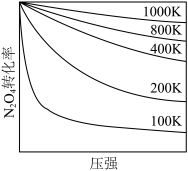
【推荐3】(NH4)2SO3氧化是氨法脱硫的重要过程。某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如图。下列说法不正确的是


| A.60℃之前,氧化速率增大与温度升高化学反应速率加快有关 |
| B.60℃之后,氧化速率降低可能与O2的溶解度下降及(NH4)2SO3受热易分解有关 |
| C.(NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,与SO32-水解程度增大有关 |
| D.(NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,可能与O2的溶解速率有关 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
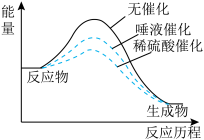
【推荐1】某小组同学探究SO2与Fe3+盐溶液的反应,进行了如下实验:已知:Fe3++HSO3-⇌Fe(HSO3)2+(红棕色)
结合上述实验,下列说法不正确的是
| 实验 | ① | ② | ③ |
| 操作 | 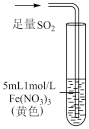 |  | 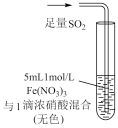 |
| 现象 | 溶液中立即产生大量红棕色物质,无丁达尔现象;5h后溶液变为浅黄色,加入铁氰化钾溶液,产生蓝色沉淀 | 溶液中立即产生大量红棕色物质,无丁达尔现象;5h后溶液几乎无色,加入铁氰化钾溶液,产生大量蓝色沉淀 | 溶液中立即产生大量红棕色物质,无丁达尔现象;5h后溶液变为黄色(比①深),加入铁氰化钾溶液,产生蓝色沉淀 |
| A.产生红棕色物质的反应速率快于SO2与Fe3+氧化还原反应的速率 |
| B.①与②对照,说明阴离子种类对SO2与Fe3+氧化还原反应的速率有影响 |
| C.Fe(NO3)3溶液中加入1滴浓硝酸后变为无色,说明浓硝酸具有漂白性 |
| D.5h后③比①黄色更深不能证明是NO3-浓度的增大减慢了SO2与Fe3+反应的速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】以四甲基氯化铵[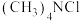 ]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[
]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[ ],下列叙述不正确的是
],下列叙述不正确的是

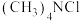 ]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[
]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[ ],下列叙述不正确的是
],下列叙述不正确的是
| A.a极电极发生还原反应 |
B.保持电流恒定,增大NaCl稀溶液浓度,制备 的反应速率增大 的反应速率增大 |
| C.c为阳离子交换膜,d为阴离子交换膜 |
| D.b极收集2.24L(标况)气体时,溶液中有0.4mol离子透过交换膜 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
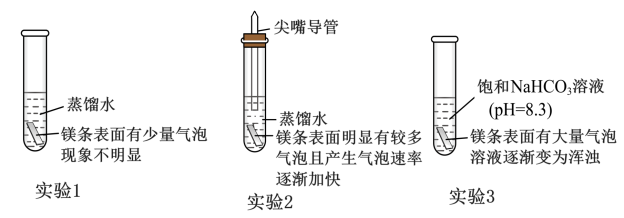
【推荐3】如图表示室温下用砂纸打磨过的镁条与水反应的探究实验,实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验3产生的浑浊物主要为碱式碳酸镁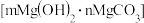 。下列说法错误的是
。下列说法错误的是
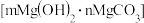 。下列说法错误的是
。下列说法错误的是
A.实验1现象不明显,可能与 Mg 表面生成了难溶的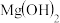 有关 有关 |
| B.实验2比实验1现象更明显,可能是由于玻璃管空间狭小热量不易散失 |
| C.由实验1和实验3可得出“碱性增强有利于加快镁与水反应速率”的结论 |
D.实验3中 破坏了 破坏了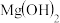 在镁条表面的沉积,增大了镁与水的接触面积 在镁条表面的沉积,增大了镁与水的接触面积 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】100mL2mol·L-1的H2SO4跟过量的锌反应,在一定温度下,为减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的
| A.0.1mol·L-1H2SO4 | B.CH3COOK |
| C.KNO3溶液 | D.K2CO3溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)pC(g)的速率和平衡的影响,图象如下,下列判断正确的是
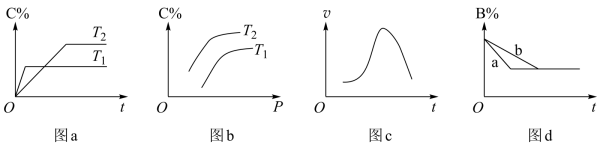

| A.由图a可知,T1>T2,该反应的逆反应为放热反应 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图象,由此说明该反应吸热 |
| D.图d中,曲线a一定增加了催化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.一定条件下,丁烷催化裂化生成1mol乙烯时,消耗丁烷的数目为NA |
| B.常温常压下,0.5molO3与11.2LO2所含的分子数均为0.5NA |
| C.用惰性电极电解CuSO4溶液一段时间后,若加入29.4gCu(OH)2能使溶液复原,则电解过程中转移电子的数目为1.2NA |
| D.25℃时,1LpH=10的NaHCO3溶液中含有H2CO3的数目为10-4NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
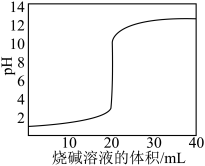
【推荐2】常温下,0.1 mol/L 的某二元酸H2A的溶液中可能存在的含A粒子(H2A、HA-、A2-)的物质的量分数随pH的变化如图所示,下列说法中不正确的是

A.H2A的电离方程式为H2A HA-+H+, HA- HA-+H+, HA- H++A2- H++A2- |
| B.Na2A溶液一定呈碱性,NaHA溶液一定呈酸性 |
| C.常温下,电离常数K(HA-)=10-3 |
| D.W点的溶液中pH=3-lg3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】25 ℃时,几种弱酸的电离常数如下:
下列说法正确的是
弱酸的化学式 | CH3COOH | HCN | H2S |
电离常数(25 ℃) | 1.8×10﹣5 | 4.9×10﹣10 | K1=1.3×10﹣7 K2=7.1×10﹣15 |
| A.等物质的量浓度的各溶液pH关系为pH(CH3COONa)>pH(Na2S)>pH(NaCN) |
| B.a mol•L-1 HCN溶液与b mol•L-1 NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b |
| C.在Na2S和NaHS的混合溶液中,一定存在c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| D.某浓度NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-d mol•L-1 |
您最近一年使用:0次