BiOCl是一种具有珍珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
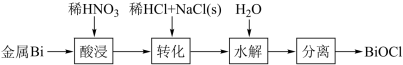
不列说法错误的是

不列说法错误的是
| A.酸浸工序中分次加入稀 HNO3可降低反应剧烈程度 |
| B.酸浸过程中金属Bi被稀HNO3氧化为Bi(NO3)3 |
| C.转化工序中加入稀HCl可抑制生成BiONO3 |
| D.水解工序中加入少量NH4NO3(s)有利于BiOCl的生成 |
更新时间:2021-07-20 19:28:13
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温下,用质量和表面积相同的镁条(已用砂纸打磨),分别探究不同条件下镁与水反应的实验(装置图如下),实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验3产生的浑浊物主要为碱式碳酸镁 [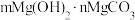 ]。下列说法正确的是
]。下列说法正确的是
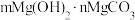 ]。下列说法正确的是
]。下列说法正确的是| 实验1 | 实验2 | 实验3 |
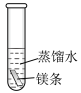 | 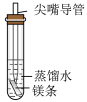 |  |
| 镁条表面有微小气泡产生。且溶液较长时间无明显变化 | 镁条表面有较多气泡且产生气泡的速率逐渐加快,溶液中无明显现象 | 镁条表面有大量气泡产生,溶液逐渐变浑浊 |
| A.实验1说明Mg不活泼,难与水反应 |
| B.实验2说明在空气催化下,Mg与水反应速率加快 |
C.实验3中 破坏了 破坏了 在镁条表面的沉积,加快了反应速率 在镁条表面的沉积,加快了反应速率 |
| D.实验1和实验3对比可得出碱性增强有利于加快镁与水的反应速率的结论 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )


| A.O→a段不产生氢气是因为表面的氧化物隔离了铝和稀盐酸 |
| B.a→b段产生氢气的速率增加较快的主要原因之一是温度升高 |
| C.t=c时刻,反应处于平衡状态 |
| D.t>c,产生氢气的速率降低的主要原因是溶液中H+浓度下降 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】化学是以实验为基础的科学,根据实验目的,下列操作及现象、结论都正确的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 检验某白色粉末中是否含有 | 取少量该粉末溶于足量稀硝酸中,再加入 溶液,溶液出现白色沉淀 溶液,溶液出现白色沉淀 | 该白色粉末中一定含有 |
| B | 探究不同价态硫元素之间的转化 | 向 和 和 混合溶液中加入浓硫酸,溶液中出现淡黄色沉淀 混合溶液中加入浓硫酸,溶液中出现淡黄色沉淀 | +4价和 价硫可反应生成0价硫 价硫可反应生成0价硫 |
| C | 探究反应物浓度对化学反应速率的影响 | 向试管A加入10ml 0.1mol/L 溶液,向试管B加入5mL 0.1mol/L 溶液,向试管B加入5mL 0.1mol/L 溶液和5mL蒸馏水。同时向两支试管加入10mL 0.1mol/L 溶液和5mL蒸馏水。同时向两支试管加入10mL 0.1mol/L 溶液,前者出现浑浊的时间更短 溶液,前者出现浑浊的时间更短 | 增大 浓度,可以加快反应速率 浓度,可以加快反应速率 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
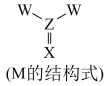
【推荐1】X、Y、Z和W是四种短周期主族元素,原子序数依次增大,Y的单质与冷水不反应,可以在二氧化碳中燃烧,X、Z同主族,X、Z、W可以构成一种易水解的物质M(如图所示),说法正确的是

| A.简单离子半径:W>Z |
| B.气态氢化物沸点:X<Z |
| C.W和第三周期离子半径最小的元素形成共价化合物,属于弱电解质 |
| D.将上述物质M和AlCl3·6H2O混合加热,可得无水氯化铝 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H<0 |
B.加水稀释0.1mol·L-1的CH3COONa溶液后,溶液中 的值增大 的值增大 |
| C.氟元素的非金属性强于溴元素,由此可推出酸性:HF>HBr |
| D.用等物质的量浓度的NaOH溶液中和等体积且pH均为2的盐酸和醋酸溶液,盐酸消耗的NaOH 溶液体积更多 |
您最近半年使用:0次



