I.可逆反应∶mA(g)+nB(g)⇌pC(g)+qD(s) ∆H,试根据图回答∶
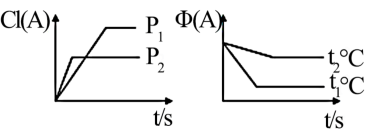
[A的转化率(%)表示为α(A)、A的含量(%)表示为φ(A)]
(1)压强P1_______ P2(填“>”,“<”或“=”下同)
(2)计量数(m+n)_______ (p)
(3)温度t1℃_______ t2℃
(4)ΔH_______ 0
II.反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
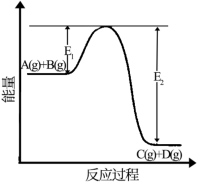
(5)该反应是_______ 反应(填“吸热”,“放热”);
(6)当反应达到平衡时,只升高温度,化学平衡向_______ (填“正反应方向”或“逆反应方向”)移动。
(7)反应体系中加入催化剂该反应的反应热_______ (填增大”“减小”“不变”);

[A的转化率(%)表示为α(A)、A的含量(%)表示为φ(A)]
(1)压强P1
(2)计量数(m+n)
(3)温度t1℃
(4)ΔH
II.反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(5)该反应是
(6)当反应达到平衡时,只升高温度,化学平衡向
(7)反应体系中加入催化剂该反应的反应热
19-20高二上·新疆乌鲁木齐·期中 查看更多[4]
新疆乌鲁木齐市第二十中学2019-2020学年高二上学期期中考试化学试题安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
更新时间:2021-09-15 22:22:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】能量转化是化学变化的主要特征之一,按要求回答下列问题。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主页,岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_________ (填序号)。
A.页岩气属于新能源
B.页岩气和氧气的反应是放热反应
C.甲烷中每个原子的最外层电子排布都达到8电子稳定结构
D.页岩气可以作燃料电池的负极燃料
(2)有关的电池装置如图:
①上述四种电池中,属于二次电池的是____ (填序号,下同),属于一次电池的是____ 。
②a装置中,外电路中电子的流向是______ (填“从Zn流向Cu”或“从Cu流向Zn”)。
③装置中,若电解质改为碱性介质,则负极的电极反应式为___ 。
(3)氧化还原反应一般可以设计成原电池。若将反应Fe+2Fe3+=3Fe2+设计成原电池,则:
①该电池的电解质溶液可以是___ 。
②当外电路中转移1 mol e-时,电解质溶液增加的质量是__ g。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主页,岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是
A.页岩气属于新能源
B.页岩气和氧气的反应是放热反应
C.甲烷中每个原子的最外层电子排布都达到8电子稳定结构
D.页岩气可以作燃料电池的负极燃料
(2)有关的电池装置如图:
| 电池装置 |  |  |  |  |
| 编号 | a | b | c | d |
①上述四种电池中,属于二次电池的是
②a装置中,外电路中电子的流向是
③装置中,若电解质改为碱性介质,则负极的电极反应式为
(3)氧化还原反应一般可以设计成原电池。若将反应Fe+2Fe3+=3Fe2+设计成原电池,则:
①该电池的电解质溶液可以是
②当外电路中转移1 mol e-时,电解质溶液增加的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】人们常常利用化学反应将化学能转化为热能、电能等其他形式的能量,用于生产、生活和科研。请回答下列问题:
(1)下图表示氢气燃烧生成水蒸气的物质及能量变化。已知1mol氢气完全燃烧生成水蒸气时放出热量245kJ。

则图中x为_______ 。
(2)为实现低碳环保的目标,北京冬奥会各赛区推广使用氢氧燃料电池汽车。某种氢氧燃料电池的内部结构示意图如下。

①a处通入_______ ,右侧的电极反应式为_______ 。
②若电路中通过3mol电子,则负极消耗物质的质量为_______ g。
(1)下图表示氢气燃烧生成水蒸气的物质及能量变化。已知1mol氢气完全燃烧生成水蒸气时放出热量245kJ。

则图中x为
(2)为实现低碳环保的目标,北京冬奥会各赛区推广使用氢氧燃料电池汽车。某种氢氧燃料电池的内部结构示意图如下。

①a处通入
②若电路中通过3mol电子,则负极消耗物质的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)已知在高温、高压、催化剂作用下,1 mol石墨转化为金刚石,吸收1.9 kJ的热量。
①石墨和金刚石________ 能量高,________ 更稳定。
②推测石墨与金刚石各1 mol在相同条件下燃烧,________ 放出的热量多。
(2)①司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应为2CrO3(红色)+3C2H5OH+3H2SO4====Cr2(SO4)3(绿色)+3CH3CHO+6H2O。
被检测的气体的成分是_______ ,上述反应中的氧化剂是_______ 。还原剂是_______ 。
②1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列_________ 事实(填入编号)。
a.苯不能使溴的四氯化碳溶液褪色 b.苯能与H2发生加成反应 c.苯没有同分异构体 d.邻二溴苯只有一种
现代化学认为苯分子碳碳之间的键是__________________ 。
①石墨和金刚石
②推测石墨与金刚石各1 mol在相同条件下燃烧,
(2)①司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应为2CrO3(红色)+3C2H5OH+3H2SO4====Cr2(SO4)3(绿色)+3CH3CHO+6H2O。
被检测的气体的成分是
②1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列
a.苯不能使溴的四氯化碳溶液褪色 b.苯能与H2发生加成反应 c.苯没有同分异构体 d.邻二溴苯只有一种
现代化学认为苯分子碳碳之间的键是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】烃基异构化是当前环保的急切要求,正戊烷异构化为异戊烷的热化学方程式是: CH3CH2CH2CH2CH3 CH3CH(CH3)CH2CH3△H=-7.1 kJ·mol-1
CH3CH(CH3)CH2CH3△H=-7.1 kJ·mol-1
(1)正戊烷异构化反应选择的温度条件是____________ 。
(2)由于副反应较为复杂,提高产率的最佳方法是____________ 。
(3)如果提高温度,反应速率___________ ,转化率___________ (填“升高"“不变”或“降低” ),同时还会产生积炭现象,假如在反应物中掺入一定量水,则可以减弱这种现象,理由是___________ (用化学方程式表示)。
(4)在573 K时,正戊烧转化率为54%,则此时平衡常数为___________ (保留两位有效数字)。
 CH3CH(CH3)CH2CH3△H=-7.1 kJ·mol-1
CH3CH(CH3)CH2CH3△H=-7.1 kJ·mol-1(1)正戊烷异构化反应选择的温度条件是
(2)由于副反应较为复杂,提高产率的最佳方法是
(3)如果提高温度,反应速率
(4)在573 K时,正戊烧转化率为54%,则此时平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上常用CO和 合成甲醇,反应方程式为:
合成甲醇,反应方程式为:
 。在
。在 时,体积为2L的恒容容器中充入物质的量之和为3mol的
时,体积为2L的恒容容器中充入物质的量之和为3mol的 和CO,达到平衡时
和CO,达到平衡时 的体积分数(V%)与
的体积分数(V%)与 的关系如图所示。
的关系如图所示。
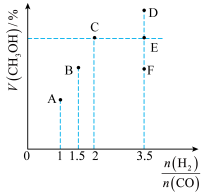
(1)当起始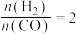 ,经过5min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率
,经过5min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率
___________ 。
(2)B点的平衡常数为_______ (计算结果保留两位小数)。
(3)当起始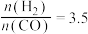 时,达到平衡状态后,
时,达到平衡状态后, 的体积分数可能是图像中的
的体积分数可能是图像中的___________ 点(填“D”“E”或“F”)。
(4)由下图可知:
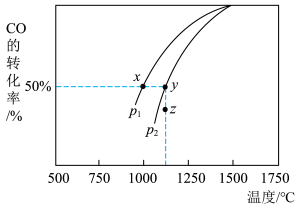
①该反应的
______ 0(填“>”“<”或“=”,下同)。
②相同起始量达到x、y时,容器内气体密度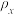
_______  。
。
③当压强为 时,在z点:
时,在z点:
_______  。
。
 合成甲醇,反应方程式为:
合成甲醇,反应方程式为:
 。在
。在 时,体积为2L的恒容容器中充入物质的量之和为3mol的
时,体积为2L的恒容容器中充入物质的量之和为3mol的 和CO,达到平衡时
和CO,达到平衡时 的体积分数(V%)与
的体积分数(V%)与 的关系如图所示。
的关系如图所示。
(1)当起始
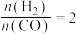 ,经过5min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率
,经过5min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率
(2)B点的平衡常数为
(3)当起始
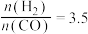 时,达到平衡状态后,
时,达到平衡状态后, 的体积分数可能是图像中的
的体积分数可能是图像中的(4)由下图可知:

①该反应的

②相同起始量达到x、y时,容器内气体密度
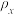
 。
。③当压强为
 时,在z点:
时,在z点:
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】用H2还原CO2可以在一定条件下合成CH3OH(不考虑副反应)
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0
CH3OH(g)+H2O(g) ΔH<0
恒压下,CO2和H2的起始物质的量比为1∶3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。

(1)甲醇平衡产率随温度升高而降低的原因为___________ 。
(2)P点甲醇产率高于T点的原因为___________ 。
(3)根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________ ℃。
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0
CH3OH(g)+H2O(g) ΔH<0恒压下,CO2和H2的起始物质的量比为1∶3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。

(1)甲醇平衡产率随温度升高而降低的原因为
(2)P点甲醇产率高于T点的原因为
(3)根据上图,在此条件下采用该分子筛膜时的最佳反应温度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在容积为1L的恒容密闭容器中,用三种纳米级Cu2O分别进行催化分解水的实验:2H2O(g) 2H2(g)+O2(g) ΔH>0。水蒸气的浓度c随时间t 的变化如下表所示:
2H2(g)+O2(g) ΔH>0。水蒸气的浓度c随时间t 的变化如下表所示:

①对比实验的温度:T2_________ T1(填“>”、“<”或“=”)
②催化剂催化效率:实验①________ 实验②(填“>”或“<”)
③在实验③达到平衡状态后,向该容器中通入水蒸气与氢气各0.1mol,则反应再次达到平衡时,请确定化学反应进行的方向_________________ (填“向正反应反应进行”或“向逆反应方向进行”)。
 2H2(g)+O2(g) ΔH>0。水蒸气的浓度c随时间t 的变化如下表所示:
2H2(g)+O2(g) ΔH>0。水蒸气的浓度c随时间t 的变化如下表所示:
①对比实验的温度:T2
②催化剂催化效率:实验①
③在实验③达到平衡状态后,向该容器中通入水蒸气与氢气各0.1mol,则反应再次达到平衡时,请确定化学反应进行的方向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。已知:3H2(g)+CO2(g)⇌CH3OH(g)+H2O(g) ΔH=-48.9kJ/mol
(1)为提高CH3OH转化率,理论上应采用的条件是________ (填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[ ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
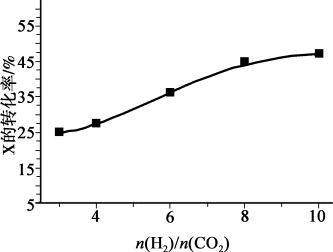
反应物X是_________ (填“CO2”或“H2”),理由是_________ 。
(3)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol,这段时间内H2的平均速率为______ ,化学平衡常数K=___ 。
(1)为提高CH3OH转化率,理论上应采用的条件是
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[
 ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
反应物X是
(3)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol,这段时间内H2的平均速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_____________________ ;
(2)反应开始至2 min,气体Z的平均反应速率为_________ ;
(3)当反应达平衡时后:若X、Y、Z均为气体,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为_____ 反应(填放热或吸热)。

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率为
(3)当反应达平衡时后:若X、Y、Z均为气体,若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
Ⅰ.一定条件下,在容积为 的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
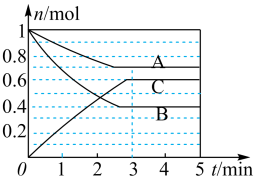
(1)达到平衡后加压,C的含量_______ (填写“变大”“变小”或“不变”)。
(2)该反应的反应速率v随时间t的关系如图所示。
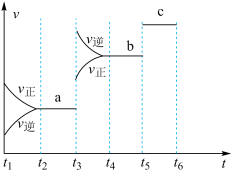
①根据图判断,在 时刻改变的外界条件是
时刻改变的外界条件是_______ 。
②a、b、c对应的平衡状态中,A的转化率最大的是状态_______ 。
Ⅱ.在密闭容器中充入一定量的 ,发生反应
,发生反应
 。如图所示为
。如图所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。

(3)该反应的逆反应是_______ (填“吸热反应”或“放热反应”)。
(4)N点 的体积分数是
的体积分数是_______ 。
(5)M点对应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅰ.一定条件下,在容积为
 的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
的密闭容器中, A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度,A的体积分数减小。
(1)达到平衡后加压,C的含量
(2)该反应的反应速率v随时间t的关系如图所示。

①根据图判断,在
 时刻改变的外界条件是
时刻改变的外界条件是②a、b、c对应的平衡状态中,A的转化率最大的是状态
Ⅱ.在密闭容器中充入一定量的
 ,发生反应
,发生反应
 。如图所示为
。如图所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)该反应的逆反应是
(4)N点
 的体积分数是
的体积分数是(5)M点对应的平衡常数

 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】T℃时,在体积为2L的恒容密闭容器中A气体与B气体反应生成C气体,反应过程中A、B、C物质的量的变化如下图a所示;若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如下图b所示。

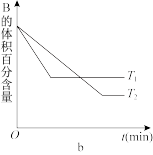
(1)从反应开始到平衡,A的平均反应速率v(A)=_____ mol/(L∙min);
(2)该反应的平衡常数表达式为___ ;为使该反应的平衡常数变大,可以采取的措施是___ 。
(3)上述反应的正反应____ (填“放热”或“吸热”);
(4)在此容器中,判断该反应达到平衡状态的标志是___ 。(填字母)
a.A和B的浓度相等 b.C的百分含量保持不变 c.容器中气体的压强不变 d.C的生成速率与C的消耗速率相等 e.容器中混合气体的密度保持不变
(5)T℃时,若在同一容器中加入2molC,达平衡后体系中各物质的百分含量与图a中的平衡状态相同,则需再加入A、B的物质的量分别为____ 、____ 。


(1)从反应开始到平衡,A的平均反应速率v(A)=
(2)该反应的平衡常数表达式为
(3)上述反应的正反应
(4)在此容器中,判断该反应达到平衡状态的标志是
a.A和B的浓度相等 b.C的百分含量保持不变 c.容器中气体的压强不变 d.C的生成速率与C的消耗速率相等 e.容器中混合气体的密度保持不变
(5)T℃时,若在同一容器中加入2molC,达平衡后体系中各物质的百分含量与图a中的平衡状态相同,则需再加入A、B的物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】T℃时,在一个体积为 2L 的容器中,A 气体与 B 气体反应生成 C 气体,反应过程中 A、B、C 的变化如图所示。
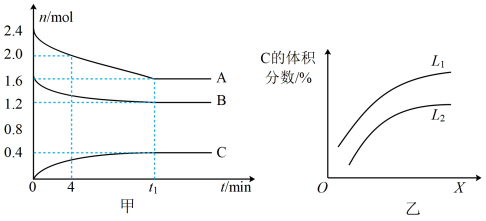
(1)根据甲图,写出反应的化学方程式_______ 。
(2)0~4min 时,A的平均反应速率为_______ 。
(3)已知:K(300℃)>K(350℃),该反应是_______ (填“吸热”或“放热”)反应。
(4)如乙图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中 X 代表的是_______ (填“温度”或“压强”)。判断 L1_______ L2(填“>” 或“<”),理由是_______ 。

(1)根据甲图,写出反应的化学方程式
(2)0~4min 时,A的平均反应速率为
(3)已知:K(300℃)>K(350℃),该反应是
(4)如乙图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中 X 代表的是
您最近一年使用:0次



