X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是
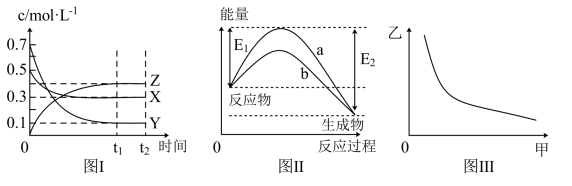

A.该反应的热化学方程式为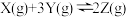 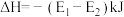 |
B.该温度下,反应的平衡常数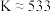 ,且若升高温度,K值减小 ,且若升高温度,K值减小 |
| C.图Ⅱ曲线b表示加入催化剂使反应活化能减小,焓变减小 |
| D.若图Ⅲ中甲表示压强,乙表示Z的含量,则其变化符合图Ⅲ中曲线 |
更新时间:2021-10-14 21:08:36
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】化学反应中常伴随着能量变化,下列有关能量的判断或表示方法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| B.已知C(s,石墨)=C(s,金刚石) △H=+1.9 kJ∙mol−1,则石墨比金刚石更稳定 |
C.已知2SO2(g)+O2(g) 2SO3(g) △H=−Q kJ∙mol−1 (Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量为 2SO3(g) △H=−Q kJ∙mol−1 (Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量为 kJ kJ |
| D.已知H+(aq)+OH-(aq)=H2O(l) △H=−57.3 kJ∙mol−1,则向含0.1 mol∙L−1的盐酸中加入4.0gNaOH固体,放出的热量等于5.73kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列热化学方程式及其有关叙述正确的是
| A.氢气的燃烧热为285.8 kJ·mol-1,则水分解的热化学方程式为2H2O(l)=2H2(g)+O2(g)ΔH=+285.8 kJ·mol-1 |
| B.已知2C(石墨,s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1,则石墨的燃烧热为110.5 kJ·mol-1 |
C.已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应,放出92.4 kJ的热量 2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应,放出92.4 kJ的热量 |
D.已知乙炔的燃烧热为1 299.6 kJ·mol-1,则表示乙炔燃烧热的热化学方程式为C2H2(g)+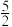 O2(g)=2CO2(g)+H2O(l) ΔH=-1 299.6 kJ·mol-1 O2(g)=2CO2(g)+H2O(l) ΔH=-1 299.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】不管化学反应是一步完成还是分几步完成,该反应的热效应是相同的。在25 ℃ ,105 Pa时,1 mol石墨和1 mol一氧化碳完全燃烧生成二氧化碳时的反应热分别是ΔH=−393.5kJ∙mol−1和ΔH=−283kJ∙mol−1,下列说法或方程式正确的是
| A.在相同条件下:2C(石墨,s)+O2(g)=2CO(g) ΔH=−110.5kJ∙mol−1 |
| B.1 mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0 kJ |
| C.在相同条件下,C(石墨,s)+CO2(g)=2CO(g) ΔH=+172.5kJ∙mol−1 |
| D.已知金刚石不如石墨稳定,则石墨转变为金刚石需要放热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】 可活化
可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:

下列关于活化历程的说法正确的是
 可活化
可活化 放出
放出 ,其反应历程如图所示:
,其反应历程如图所示:
下列关于活化历程的说法正确的是
A.该转化过程 >0 >0 |
B.该反应过程中,最大能垒(活化能)为204.32 |
C.在此反应过程中 的成键数目未发生变化 的成键数目未发生变化 |
| D.整个过程中,Ni是该反应的催化剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】我们把能够发生化学反应的碰撞叫做有效碰撞;发生有效碰撞的分子必须具有足够的能量,这种分子叫做活化分子;活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能。下列说法不正确的是


| A.图甲中曲线Ⅱ可以表示催化剂降低了反应的活化能,反应的转化率不变 |
| B.图乙中HI分子发生了有效碰撞 |
| C.盐酸和氢氧化钠溶液反应速度非常快,反应活化能较小 |
| D.压缩体积增大反应物浓度,单位时间内有效碰撞次数增加 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列方式方法不能用来研究2NO2 N2O4反应快慢的是
N2O4反应快慢的是
 N2O4反应快慢的是
N2O4反应快慢的是| A.恒温恒压下,测容器体积的变化情况 |
| B.恒温恒容下,测混合气体颜色的深浅 |
| C.绝热恒容下,测容器内温度的变化情况 |
| D.恒温恒压下,测量容器内压强变化情况 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】如图表示不同温度(T)和压强(p)对可逆反应 的影响,且
的影响,且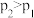 。则图中纵轴表示的意义可能是
。则图中纵轴表示的意义可能是
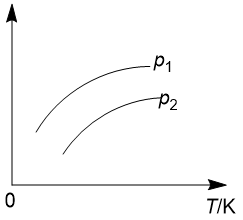
①混合气体的平均摩尔质量
②混合气体中M的百分含量
③混合气体中L的百分含量
④一定条件下L的转化率
 的影响,且
的影响,且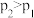 。则图中纵轴表示的意义可能是
。则图中纵轴表示的意义可能是
①混合气体的平均摩尔质量
②混合气体中M的百分含量
③混合气体中L的百分含量
④一定条件下L的转化率
| A.①③ | B.②④ | C.①② | D.②③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】T℃时,向2.0 L恒容密闭容器中充入 ,发生反应
,发生反应
 。经过一段时间后达到平衡,测得反应过程中部分数据如下表所示。
。经过一段时间后达到平衡,测得反应过程中部分数据如下表所示。
下列说法正确的是
 ,发生反应
,发生反应
 。经过一段时间后达到平衡,测得反应过程中部分数据如下表所示。
。经过一段时间后达到平衡,测得反应过程中部分数据如下表所示。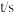 | 0 | 50 | 150 | 250 | 350 |
 | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A.该反应在任何温度下均能自发进行 |
B.前50 s的平均速率 |
| C.T℃时,该反应的平衡常数为0.025 |
D.若开始时充入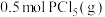 ,则平衡时 ,则平衡时 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在一定温度下,反应X(g)+Y(g) 2Z(g)的平衡常数为0.25,若将10mol的Z(g)通入体积为10L的密闭容器中,在该温度时Z(g)的最大分解率接近于
2Z(g)的平衡常数为0.25,若将10mol的Z(g)通入体积为10L的密闭容器中,在该温度时Z(g)的最大分解率接近于
 2Z(g)的平衡常数为0.25,若将10mol的Z(g)通入体积为10L的密闭容器中,在该温度时Z(g)的最大分解率接近于
2Z(g)的平衡常数为0.25,若将10mol的Z(g)通入体积为10L的密闭容器中,在该温度时Z(g)的最大分解率接近于| A.50% | B.80% |
| C.88% | D.95% |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】在常温下,下列反应的平衡常数的数值如下:2NO(g)  N2(g)+O2(g) K1=1×1030;2H2(g)+O2(g)
N2(g)+O2(g) K1=1×1030;2H2(g)+O2(g) 2H2O(g) K2=2×1081; 2CO2(g)
2H2O(g) K2=2×1081; 2CO2(g) 2CO(g)+O2(g) K3=4×10-92。以下说法正确的是( )
2CO(g)+O2(g) K3=4×10-92。以下说法正确的是( )
 N2(g)+O2(g) K1=1×1030;2H2(g)+O2(g)
N2(g)+O2(g) K1=1×1030;2H2(g)+O2(g) 2H2O(g) K2=2×1081; 2CO2(g)
2H2O(g) K2=2×1081; 2CO2(g) 2CO(g)+O2(g) K3=4×10-92。以下说法正确的是( )
2CO(g)+O2(g) K3=4×10-92。以下说法正确的是( )| A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D.以上说法都不正确 |
您最近一年使用:0次



