下列事实不能用平衡移动原理解释的是
| A.浓硫酸的使用有利于酯化反应 |
| B.夏天打开啤酒瓶,有许多气泡冒出 |
| C.Fe(SCN)3溶液中加入6mol/L NaOH溶液后颜色变浅 |
| D.唾液可以使淀粉水解速率加快 |
更新时间:2021-10-16 11:53:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知mX(g)+nY(g) gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是
gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是
 gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是
gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是| A.升高温度,平衡将正向移动 |
| B.X的正反应速率是Y的逆反应速率的m/n倍 |
| C.降低温度,混合气体的平均相对分子质量变小 |
| D.增加X的物质的量,Y的转化率降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实中,不能 用勒夏特列原理解释的是
① 溶液中加入固体KSCN后颜色变深
溶液中加入固体KSCN后颜色变深
②由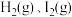 和HI(g)组成的平衡体系加压后颜色变深
和HI(g)组成的平衡体系加压后颜色变深
③实验室常用排饱和食盐水的方法收集氯气
④棕红色 加压后颜色先变深后变浅
加压后颜色先变深后变浅
⑤加催化剂有利于合成氨的反应
①
 溶液中加入固体KSCN后颜色变深
溶液中加入固体KSCN后颜色变深②由
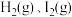 和HI(g)组成的平衡体系加压后颜色变深
和HI(g)组成的平衡体系加压后颜色变深③实验室常用排饱和食盐水的方法收集氯气
④棕红色
 加压后颜色先变深后变浅
加压后颜色先变深后变浅⑤加催化剂有利于合成氨的反应
| A.②⑤ | B.③⑤ | C.①② | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】能使反应 的反应速率增大,且平衡向正反应方向移动的是
的反应速率增大,且平衡向正反应方向移动的是
 的反应速率增大,且平衡向正反应方向移动的是
的反应速率增大,且平衡向正反应方向移动的是A.及时分离出 气体 气体 | B.增大 的浓度 的浓度 |
| C.适当降低温度 | D.选择高效催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,在重铬酸钾( )溶液中存在如下平衡:
)溶液中存在如下平衡: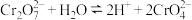 ,若要使溶液呈橙色且酸性增强,下列条件可行的是(已知
,若要使溶液呈橙色且酸性增强,下列条件可行的是(已知 与
与 会产生
会产生 砖红色沉淀)
砖红色沉淀)
 )溶液中存在如下平衡:
)溶液中存在如下平衡: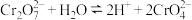 ,若要使溶液呈橙色且酸性增强,下列条件可行的是(已知
,若要使溶液呈橙色且酸性增强,下列条件可行的是(已知 与
与 会产生
会产生 砖红色沉淀)
砖红色沉淀)A.加入 固体 固体 | B.通入 气体 气体 |
C.加入 固体 固体 | D.加入 固体 固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对于平衡体系:aA(g)+bB(g) cC(g)+dD(g) △H<0,下列判断其中不正确的是
cC(g)+dD(g) △H<0,下列判断其中不正确的是
 cC(g)+dD(g) △H<0,下列判断其中不正确的是
cC(g)+dD(g) △H<0,下列判断其中不正确的是| A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,则a+b<c+d |
| B.若从正反应开始,平衡时,A、B的转化率相等,则投入A、B的物质的量之比为a:b |
| C.若平衡体系中共有气体Mmol,再向其中充入bmolB,达到平衡时气体总物质的量为( M+b)mol,则a+b=c+d |
| D.若a+b=c+d,对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】恒温时,在体积为V的密闭容器内,可逆反应:N2 + 3H2 2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为
2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为
 2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为
2NH 3 达平衡时,测得容器内气体的压强为p1 。将容器的体积压缩 V/2 至达到新的平衡时,气体的压强为 p2。则 p1和p 2的关系为| A.p2 < p 1 | B.p1 < p2 < 2p1 | C.p1 > 2p2 | D.2p1 = p2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)⇌4NO2(g)+ O2(g) ΔH>0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
下列说法中不正确的是
2N2O5(g)⇌4NO2(g)+ O2(g) ΔH>0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A.500 s内N2O5分解速率为2.96×10-3mol·L-1·s-1 |
| B.T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50% |
| C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 |
D.达平衡后其他条件不变,将容器的体积压缩到原来的 ,则再次平衡时c(N2O5)> 5.00 mol·L-1 ,则再次平衡时c(N2O5)> 5.00 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
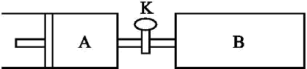
【推荐3】如图,关闭活塞K,向A中充入1 mol X、1 mol Y,向B中充入2 mol X、2 mol Y,起始时A的容积是a L、B的容积是2a L。在相同温度和催化剂存在的条件下,使两容器中均发生反应X(g)+Y(g) 2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容,达到平衡时,A的容积为1.4a L。下列说法错误的是
2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容,达到平衡时,A的容积为1.4a L。下列说法错误的是
 2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容,达到平衡时,A的容积为1.4a L。下列说法错误的是
2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容,达到平衡时,A的容积为1.4a L。下列说法错误的是
| A.反应速率:v(B)>v(A) |
| B.A中X的转化率为80% |
| C.平衡时Y体积分数:A>B |
| D.打开活塞K,反应一段时间后达到平衡,此时A的容积为2.2a L(连通管中气体体积不计) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用化学平衡移动原理解释的是
| A.收集氯气可以用排饱和食盐水的方法 |
| B.在一定条件下,氢气与碘蒸汽反应达平衡后,加压,混合气体颜色变深 |
| C.可用浓氨水和氢氧化钠固体快速制取氨气 |
| D.合成三氧化硫过程中使用过量的氧气,以提高二氧化硫的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列变化不能用平衡移动原理释解的是
| A.工业合成氨的反应,往往需要使用催化剂 |
B.红棕色的 加压后颜色先变深再变浅 加压后颜色先变深再变浅 |
| C.光照新制的氯水,溶液的酸性增强 |
| D.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
您最近一年使用:0次

 催化氧化时,使用催化剂加快化学反应速率
催化氧化时,使用催化剂加快化学反应速率 平衡体系加压,气体颜色变深
平衡体系加压,气体颜色变深 溶液中加入Fe粉,溶液颜色逐渐变浅
溶液中加入Fe粉,溶液颜色逐渐变浅

