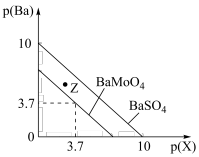
已知:BaMoO4、BaSO4均难溶于水,lg2≈0.3,离子浓度≤10-5mol/L时认为其沉淀完全。T℃时,BaMoO4、BaSO4的沉淀溶解平衡曲线如图所示,其中p(Ba)=-lgc(Ba2+),p(X)=-lgc(MoO )或-lgc(SO
)或-lgc(SO )。下列叙述正确的是
)。下列叙述正确的是
 )或-lgc(SO
)或-lgc(SO )。下列叙述正确的是
)。下列叙述正确的是
| A.T℃时,Z点对应为BaMoO4的不饱和溶液 |
| B.T℃时,向等浓度的Na2SO4和Na2MoO4的混合溶液中加入BaCl2溶液,先析出BaMoO4沉淀 |
| C.T℃时,Ksp(BaMoO4)的数量级为10-7 |
D.T℃时,BaMoO4(s)+SO  BaSO4(s)+MoO BaSO4(s)+MoO 的平衡常数K=200 的平衡常数K=200 |
更新时间:2021-11-14 15:28:49
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
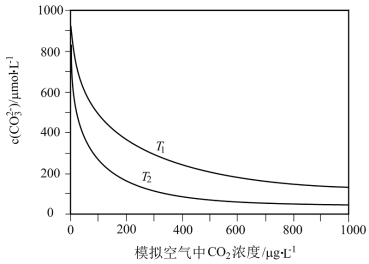
【推荐1】大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO 浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO
浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO (aq)+H2O(aq)
(aq)+H2O(aq)  2HCO
2HCO (aq),下列说法不正确的是
(aq),下列说法不正确的是
 浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO
浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO (aq)+H2O(aq)
(aq)+H2O(aq)  2HCO
2HCO (aq),下列说法不正确的是
(aq),下列说法不正确的是
| A.T1>T2 |
B.海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,CO 浓度降低 浓度降低 |
C.当大气中CO2浓度确定时,海水温度越高,CO 浓度越低 浓度越低 |
| D.大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,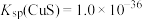 ,
,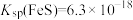 ,下列说法错误的是
,下列说法错误的是
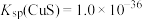 ,
,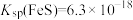 ,下列说法错误的是
,下列说法错误的是A. 在水中的沉淀溶解平衡可表示为: 在水中的沉淀溶解平衡可表示为: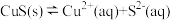 |
B.25℃时,饱和 溶液中 溶液中 的浓度为 的浓度为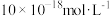 |
C.因为 是强酸,所以反应 是强酸,所以反应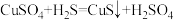 不能发生 不能发生 |
D.除去某溶液中的 ,可加入 ,可加入 作沉淀剂,反应的离子方程式为 作沉淀剂,反应的离子方程式为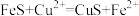 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断正确的是
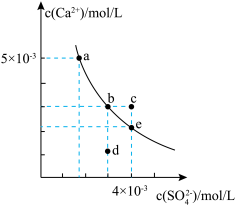

| A.曲线上任意一点的Ksp都相同 |
| B.在CaSO4饱和溶液中加入Na2SO4固体,可使溶液由b点变化到c点 |
| C.蒸发水后,可使溶液由d点变化到b点 |
| D.常温下,CaSO4的Ksp的数量级为10-5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.1000mol/L AgNO3标准溶液(pH≈5)分别滴定20.00 mL 0.1000mol/L的NaCl溶液和NaBr溶液,混合溶液的pAg[定义为pAg= -lgc(Ag+)]与AgNO3溶液体积的变化关系如图所示。下列说法不正确的是
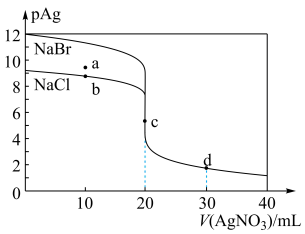

| A.常温时溶度积常数:Ksp(AgCl)>Ksp(AgBr) |
| B.相同实验条件下,若改用10.00 mL 0.2000mol/L NaCl溶液,则b点向a点移动 |
| C.NaBr溶液在c点时:c(Ag+)+c(H+)=c(Br-)+c(OH-) |
D.NaCl溶液在d点时:c( )>c(Na+)>c(Ag+)>c(Cl-)>c(H+) )>c(Na+)>c(Ag+)>c(Cl-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组利用工业废弃的铁铜合金制备碳式碳酸铜的简易流程如图。下列叙述正确的是
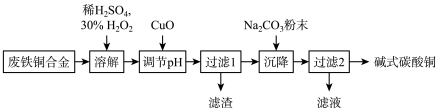

A.“沉降”应中溶液 以不同方式或不同用量比混合不影响产品成分 以不同方式或不同用量比混合不影响产品成分 |
| B.“调节pH”环节可用氨水替代CuO |
| C.“过滤I ”的滤液中c (Cu2+) ·c2 (OH-) ≦Ksp[Cu (OH)2] |
| D.为了加快反应速率,“溶解”应在较高温度下进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 是重要的工业原料。用含镍废料(主要成分为NiO,含有少量
是重要的工业原料。用含镍废料(主要成分为NiO,含有少量 和
和 )制备
)制备 和
和 的流程如图所示。
的流程如图所示。
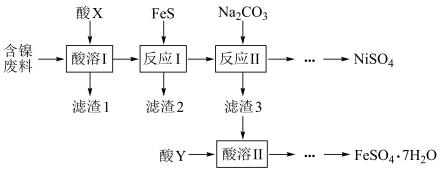
下列说法错误的是
 是重要的工业原料。用含镍废料(主要成分为NiO,含有少量
是重要的工业原料。用含镍废料(主要成分为NiO,含有少量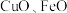 和
和 )制备
)制备 和
和 的流程如图所示。
的流程如图所示。
下列说法错误的是
A.滤渣1为 |
B.反应Ⅰ能自发进行,说明: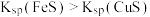 |
| C.X和Y都是硫酸,硫酸浓度越大越能提高酸溶率 |
D.当加入 的浓度过大时,滤渣3为混合物 的浓度过大时,滤渣3为混合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】溶液中除铁时还常用NaClO3作氧化剂,在较小的pH条件下最终生成一种浅黄色的黄铁矾钠 [Na2Fe6(SO4)4(OH)12]沉淀除去。下图是温度-pH与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域。下列说法不正确的是 {已知25℃,Ksp[Fe(OH)3]=2.64×10-39}


| A.工业生产黄铁矾钠,温度控制在85~95℃pH=1.5左右 |
| B.pH=6,温度从80℃升高至150℃体系得到的沉淀被氧化 |
| C.用氯酸钠在酸性条件下氧化Fe2+ 离子方程式为:6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O |
| D.在25℃时溶液经氧化,调节溶液pH=4 ,此时溶液中c(Fe3+)=2.64×10-9 mol·L-1 |
您最近一年使用:0次

 Ca2+(aq)+2OH-(aq)△H<0,下列有关该平衡体系的说法正确的有几个
Ca2+(aq)+2OH-(aq)△H<0,下列有关该平衡体系的说法正确的有几个