实验中学高二化学某班学生甲、乙小组,分别用实验探究溶液中 、
、 的化学性质回答下列问题:
的化学性质回答下列问题:
(1)将硫酸亚铁溶液滴入硫酸酸化的 溶液中,振荡混合后,溶液中含有
溶液中,振荡混合后,溶液中含有 、
、 等。以下请用离子方程式回答:
等。以下请用离子方程式回答:
①25℃时硫酸亚铁溶液 的原因:
的原因:___________ 。
②请写出硫酸亚铁溶液与硫酸酸化的 溶液反应的原理:
溶液反应的原理:___________ 。
(2)甲组同学取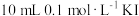 溶液,加入
溶液,加入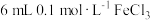 溶液混合。充分反应后,分别取2 mL此溶液于3支试管中进行如下实验:
溶液混合。充分反应后,分别取2 mL此溶液于3支试管中进行如下实验:
①第一支试管中加入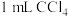 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;
②第二支试管中加入1滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红实验。
②检验的离子是___________ (填离子符号);
实验①和③说明:在 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有___________ (填离子符号),由此可以证明该氧化还原反应为___________ (填可逆反应或不可逆反应)。
(3)乙组同学向盛有 溶液的试管中加入几滴硫酸酸化的硫酸亚铁溶液,溶液变成棕黄色,发生反应的离子方程式为:
溶液的试管中加入几滴硫酸酸化的硫酸亚铁溶液,溶液变成棕黄色,发生反应的离子方程式为:___________ 。一段时间后,溶液中有气泡出现,试管微热,随后有红褐色沉淀生成。产生气泡的原因是___________ 。
 、
、 的化学性质回答下列问题:
的化学性质回答下列问题:(1)将硫酸亚铁溶液滴入硫酸酸化的
 溶液中,振荡混合后,溶液中含有
溶液中,振荡混合后,溶液中含有 、
、 等。以下请用离子方程式回答:
等。以下请用离子方程式回答:①25℃时硫酸亚铁溶液
 的原因:
的原因:②请写出硫酸亚铁溶液与硫酸酸化的
 溶液反应的原理:
溶液反应的原理:(2)甲组同学取
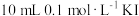 溶液,加入
溶液,加入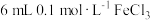 溶液混合。充分反应后,分别取2 mL此溶液于3支试管中进行如下实验:
溶液混合。充分反应后,分别取2 mL此溶液于3支试管中进行如下实验:①第一支试管中加入
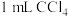 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;②第二支试管中加入1滴
 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入1滴KSCN溶液,溶液变红实验。
②检验的离子是
实验①和③说明:在
 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有(3)乙组同学向盛有
 溶液的试管中加入几滴硫酸酸化的硫酸亚铁溶液,溶液变成棕黄色,发生反应的离子方程式为:
溶液的试管中加入几滴硫酸酸化的硫酸亚铁溶液,溶液变成棕黄色,发生反应的离子方程式为:
更新时间:2021/11/15 15:32:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某废料铁泥主要成分为 、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取
、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:
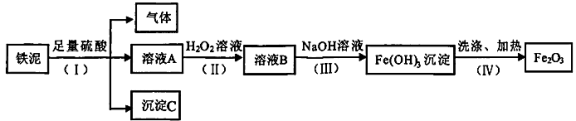
(1)写出步骤(I)中铁单质参与的有关反应的离子方程式___________ ,分离溶液A和沉淀C的操作名称是___________ 。
(2)检验溶液A中含有 应选用的试剂是
应选用的试剂是___________
A.铁粉 B. 溶液 C.酸性
溶液 C.酸性 溶液 D.KSCN溶液
溶液 D.KSCN溶液
(3)步骤(Ⅱ)中加入 溶液,
溶液, 在反应中作
在反应中作___________ (填“氧化剂”或“还原剂”)。
(4)步骤(IV)中生成的 固体的颜色是
固体的颜色是___________ 。
(5)若最终获得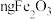 ,则铁泥中铁元素的质量分数为
,则铁泥中铁元素的质量分数为___________ 。
 、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取
、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:
(1)写出步骤(I)中铁单质参与的有关反应的离子方程式
(2)检验溶液A中含有
 应选用的试剂是
应选用的试剂是A.铁粉 B.
 溶液 C.酸性
溶液 C.酸性 溶液 D.KSCN溶液
溶液 D.KSCN溶液(3)步骤(Ⅱ)中加入
 溶液,
溶液, 在反应中作
在反应中作(4)步骤(IV)中生成的
 固体的颜色是
固体的颜色是(5)若最终获得
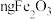 ,则铁泥中铁元素的质量分数为
,则铁泥中铁元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂。
[查阅资料]隔绝空气加热至500 ℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用如图所示部分装置进行实验(夹持装置略)。
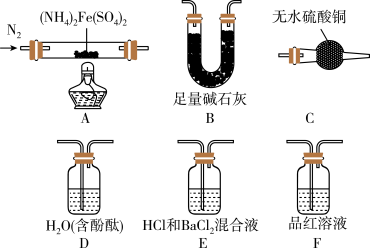
验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
(1)所选用装置的正确连接顺序为________________________ (填装置序号)。
(2)证明有水蒸气生成的实验现象为_______________________ 。
(3)证明有氨气生成的实验现象为_____________________ 。
(4)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含FeO或Fe3O4:______________________ 。
[查阅资料]隔绝空气加热至500 ℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用如图所示部分装置进行实验(夹持装置略)。

验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
(1)所选用装置的正确连接顺序为
(2)证明有水蒸气生成的实验现象为
(3)证明有氨气生成的实验现象为
(4)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含FeO或Fe3O4:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水FeCl3,实验装置如下图所示:
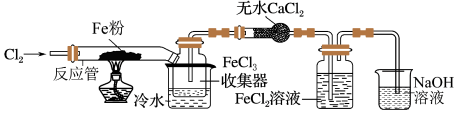
已知:无水FeCl3在空气中易潮解,加热易升华。
⑴通入Cl2和加热反应管这两步操作的先后顺序是_____ ,原因是______ 。
⑵实验后生成的FeCl3大部分进入收集器,少量沉积在反应管的右端。要使沉积得FeCl3进入收集器,可以进行的操作是________ 。
⑶洗气瓶中的FeCl2溶液用于吸收未反应的Cl2。向反应后的洗气瓶中滴加KSCN溶液,结果看到溶液先变红后褪色,溶液褪色的可能原因是_______ 。
⑷洗气瓶中生成的FeCl3溶液可用于吸收H2S气体生成S。写出吸收H2S气体的离子反应方程式:_______ 。为检测反应后溶液中是否存在Fe2+,甲同学提出可用酸性KMnO4溶液,乙同学提出酸性KMnO4溶液褪色不能证明存在Fe2+,理由是________ 。

已知:无水FeCl3在空气中易潮解,加热易升华。
⑴通入Cl2和加热反应管这两步操作的先后顺序是
⑵实验后生成的FeCl3大部分进入收集器,少量沉积在反应管的右端。要使沉积得FeCl3进入收集器,可以进行的操作是
⑶洗气瓶中的FeCl2溶液用于吸收未反应的Cl2。向反应后的洗气瓶中滴加KSCN溶液,结果看到溶液先变红后褪色,溶液褪色的可能原因是
⑷洗气瓶中生成的FeCl3溶液可用于吸收H2S气体生成S。写出吸收H2S气体的离子反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O 的流程如下:
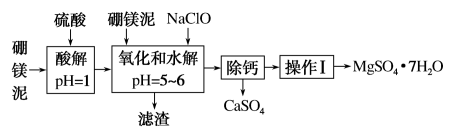
根据题意回答下列问题:
(1)实验中需用1mo/L 的硫酸800mL,若用18.4mol/L 的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为____________
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO 可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-,还 有一种离子也会被NaClO氧化,该反应的离子方程式为_________________ 。
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外还有________________ 。
(4)在“除钙”前,需检验滤波中Fe3+是否被除尽,简述检验方法:______________ 。
(5)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤: “操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,__________ ,便得到了MgSO4·7H2O。
(6)实验中提供的硼镁泥共10g,得到的MgSO4·7H2O 为17.22g,则MgSO4·7H2O的产率为__________________ 。

根据题意回答下列问题:
(1)实验中需用1mo/L 的硫酸800mL,若用18.4mol/L 的浓硫酸来配制,量取浓硫酸时,需使用的量筒的规格为
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO 可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-,还 有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外还有
(4)在“除钙”前,需检验滤波中Fe3+是否被除尽,简述检验方法:
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤: “操作Ⅰ”是将滤液继续蒸发浓缩,冷却结晶,
(6)实验中提供的硼镁泥共10g,得到的MgSO4·7H2O 为17.22g,则MgSO4·7H2O的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】甘氨酸亚铁[(H2NCH2COO)2Fe,摩尔质量204g/mol]是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
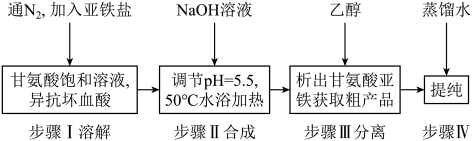
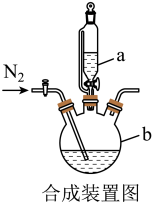
已知:
请回答:
(1)下列说法正确的是___________。
(2)合成过程中,本实验为了防止Fe2+被氧化,采取的措施是___________ 。
(3)合成过程需控制pH=5.5,pH过大或过小都对实验有影响,试说明理由___________ 。
(4)步骤Ⅲ加入无水乙醇的目的是___________ 。
(5)若甘氨酸的投料量为300kg,得到纯品306kg,则产品的产率为___________ 。


已知:
| 甘氨酸H2NCH2COOH | 异抗坏血酸 | 甘氨酸亚铁 | FeSO4·7H2O | FeCl2·4H2O |
| 易溶于水微溶于乙醇 | 易溶于水和乙醇有弱酸性和强环原性 | 易溶于水难溶于乙醇 | 易溶于水难溶于乙醇 | 易溶于水易溶于乙醇 |
(1)下列说法正确的是___________。
| A.滴入液体前,应先打开滴液漏斗a的上口玻璃塞 |
| B.根据题中所给信息,亚铁盐应选用FeSO4·7H2O |
| C.步骤Ⅲ中的分离方法是过滤 |
| D.步骤Ⅳ,提纯操作中的干燥过程最好选用真空干燥 |
(3)合成过程需控制pH=5.5,pH过大或过小都对实验有影响,试说明理由
(4)步骤Ⅲ加入无水乙醇的目的是
(5)若甘氨酸的投料量为300kg,得到纯品306kg,则产品的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫酸亚铁铵晶体[x(NH4)2SO4·yFeSO4·zH2O] [ M=(132x+152y+18z)g·mol-1 ]是常见的补血剂。
已知:①硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
②FeSO4溶液与(NH4)2SO4反应可得到硫酸亚铁铵。
(1)FeSO4溶液的制备。将铁粉、一定量 H2SO4溶液反应制得FeSO4溶液,其中加入的铁粉需过量,除铁粉不纯外,主要原因是_______ (用离子方程式表示)。
(2)制备x(NH4)2SO4·yFeSO4·zH2O。向制备得到的FeSO4溶液中加入一定质量的(NH4)2SO4固体,在70℃~80℃条件下溶解后,趁热倒入50mL乙醇中,析出晶体。乙醇的作用为_______ 。
(3)产品化学式的确定——NH 含量的测定
含量的测定
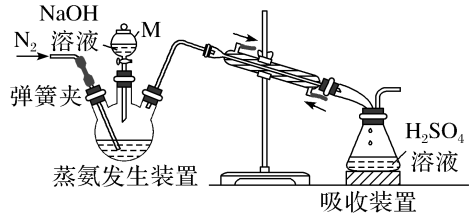
I.准确称取58.80 g晶体,加水溶解后,将溶液注入三颈烧瓶中;
II.准确量取50.00 mL 3.030 mol·L-1 H2SO4溶液于锥形瓶中;
III.向三颈烧瓶中通入氮气,加入足量NaOH浓溶液,加热,蒸氨结束后取下锥形瓶;
IV.用0.120 mol·L-1的NaOH标准溶液滴定锥形瓶中过量的硫酸,滴定终点时消耗25.00 mL NaOH标准溶液。
①装置M的名称为_______ 。
②通入N2的作用为_______ 。
③蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”,“处理”的操作方法是_______ 。
④若步骤IV中,未用NaOH标准溶液润洗滴定管,则n(NH )将
)将_______ (填“偏大”、“偏小”或“不变”)。
(4)产品化学式的确定——SO 含量的测定
含量的测定
I.另准确称取58.80 g晶体于烧杯中,加水溶解,边搅拌边加入过量的BaCl2溶液;
II.将得到的溶液过滤得到沉淀,洗涤沉淀3~4次;
Ⅲ.灼烧沉淀至恒重,称量,得沉淀质量为69.90 g。
结合实验(3)和(4),通过计算得出硫酸亚铁铵晶体的化学式为_______ 。
已知:①硫酸亚铁铵晶体在空气中不易被氧化,易溶于水,不溶于乙醇。
②FeSO4溶液与(NH4)2SO4反应可得到硫酸亚铁铵。
(1)FeSO4溶液的制备。将铁粉、一定量 H2SO4溶液反应制得FeSO4溶液,其中加入的铁粉需过量,除铁粉不纯外,主要原因是
(2)制备x(NH4)2SO4·yFeSO4·zH2O。向制备得到的FeSO4溶液中加入一定质量的(NH4)2SO4固体,在70℃~80℃条件下溶解后,趁热倒入50mL乙醇中,析出晶体。乙醇的作用为
(3)产品化学式的确定——NH
 含量的测定
含量的测定
I.准确称取58.80 g晶体,加水溶解后,将溶液注入三颈烧瓶中;
II.准确量取50.00 mL 3.030 mol·L-1 H2SO4溶液于锥形瓶中;
III.向三颈烧瓶中通入氮气,加入足量NaOH浓溶液,加热,蒸氨结束后取下锥形瓶;
IV.用0.120 mol·L-1的NaOH标准溶液滴定锥形瓶中过量的硫酸,滴定终点时消耗25.00 mL NaOH标准溶液。
①装置M的名称为
②通入N2的作用为
③蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”,“处理”的操作方法是
④若步骤IV中,未用NaOH标准溶液润洗滴定管,则n(NH
 )将
)将(4)产品化学式的确定——SO
 含量的测定
含量的测定I.另准确称取58.80 g晶体于烧杯中,加水溶解,边搅拌边加入过量的BaCl2溶液;
II.将得到的溶液过滤得到沉淀,洗涤沉淀3~4次;
Ⅲ.灼烧沉淀至恒重,称量,得沉淀质量为69.90 g。
结合实验(3)和(4),通过计算得出硫酸亚铁铵晶体的化学式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】在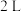 密闭容器中,800℃时反应
密闭容器中,800℃时反应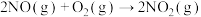 体系中,
体系中,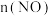 随时间的变化如表:
随时间的变化如表:
(1)上述反应___________ (填“是”或“不是”)可逆反应。
(2)如图所示,表示 变化曲线的是
变化曲线的是______ 。用 表示从
表示从 内该反应的平均速率v=
内该反应的平均速率v=_______ 。
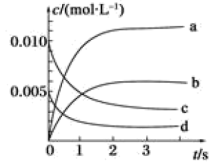
(3)能说明该反应已达到平衡状态的是___________ (填序号)。
a. b.容器内压强保持不变
b.容器内压强保持不变
c.体系颜色不再改变d.容器内密度保持不变
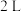 密闭容器中,800℃时反应
密闭容器中,800℃时反应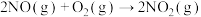 体系中,
体系中,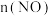 随时间的变化如表:
随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应
(2)如图所示,表示
 变化曲线的是
变化曲线的是 表示从
表示从 内该反应的平均速率v=
内该反应的平均速率v=
(3)能说明该反应已达到平衡状态的是
a.
 b.容器内压强保持不变
b.容器内压强保持不变c.体系颜色不再改变d.容器内密度保持不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I.某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据分析得:(8分钟时A为0.2mol 、B为0.5mol)
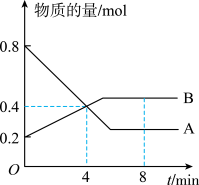
(1)该反应的化学方程式为_________________________ 。
(2)反应开始时至4min时,A的平均反应速率为________ 。
(3)4min时,反应是否达平衡状态?________ (填“是”或“否”), 8min时,V正________ V逆(填“>”“<”或“=”)。
II.在2L密闭容器中,800℃时反应2NO(g)+O2(g) →2NO2(g)体系中,n(NO)随时间的变化如表:
(1)上述反应________ (填“是”或“不是”)可逆反应。
(2)如图所示,表示NO2变化曲线的是________ 。
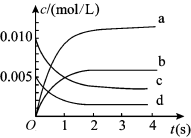
(3)能说明该反应已达到平衡状态的是________ (填序号)。
a. v(NO2)=2v(O2) b.容器内压强保持不变
c. v逆(NO)=2v正(O2) d. 容器内密度保持不变

(1)该反应的化学方程式为
(2)反应开始时至4min时,A的平均反应速率为
(3)4min时,反应是否达平衡状态?
II.在2L密闭容器中,800℃时反应2NO(g)+O2(g) →2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图所示,表示NO2变化曲线的是

(3)能说明该反应已达到平衡状态的是
a. v(NO2)=2v(O2) b.容器内压强保持不变
c. v逆(NO)=2v正(O2) d. 容器内密度保持不变
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】碘化钾是常用的化工原料。某实验小组设计实验探究 的还原性。
的还原性。
I.探究不同条件下空气中氧气氧化 的速率。
的速率。
(1)酸性条件下 能被空气中氧气氧化,发生反应的离子方程式为
能被空气中氧气氧化,发生反应的离子方程式为_______ 。
(2)通过实验组别1和组别2探究温度对氧化速率的影响。其中
_______ ,
_______ 。
(3)设计实验组别3的目的是_______ 。
Ⅱ.探究反应“ ”为可逆反应。
”为可逆反应。
试剂: 溶液,
溶液, 溶液,淀粉溶液,
溶液,淀粉溶液, 溶液,
溶液, 溶液。实验如下:
溶液。实验如下:_______ ;乙同学认为该现象无法证明该反应为可逆反应,原因为_______ 。
(5)请选择上述试剂重新设计实验,证明该反应为可逆反应_______ 。
 的还原性。
的还原性。I.探究不同条件下空气中氧气氧化
 的速率。
的速率。| 组别 | 温度 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | 淀粉溶液 | ||
 | V |  | V | ||||
| 1 |  |  |  |  |  |  | 3滴 |
| 2 | 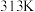 |  | 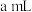 | 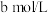 |  |  | 3滴 |
| 3 |  |  |  | 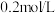 |  |  | 3滴 |
 能被空气中氧气氧化,发生反应的离子方程式为
能被空气中氧气氧化,发生反应的离子方程式为(2)通过实验组别1和组别2探究温度对氧化速率的影响。其中


(3)设计实验组别3的目的是
Ⅱ.探究反应“
 ”为可逆反应。
”为可逆反应。试剂:
 溶液,
溶液, 溶液,淀粉溶液,
溶液,淀粉溶液, 溶液,
溶液, 溶液。实验如下:
溶液。实验如下:
(5)请选择上述试剂重新设计实验,证明该反应为可逆反应
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】六水合硫酸镁铵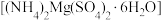 是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。
是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。
实验室制备步骤如下:
Ⅰ.称取 于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。
于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。
Ⅱ.称取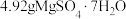 于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。
于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。
Ⅲ.将步骤Ⅰ所得的 溶液倒入步骤Ⅱ的
溶液倒入步骤Ⅱ的 溶液中,搅拌混合充分,冰水浴20min,析出晶体。
溶液中,搅拌混合充分,冰水浴20min,析出晶体。
Ⅳ.减压过滤。用无水乙醇洗涤产品1~2次,抽干后,将晶体转移到蒸发皿里,置于40℃水浴锅中约30min,即可得 晶体。
晶体。
Ⅴ.所得晶体称重为mg。
回答下列问题:
(1)称取固体应采用___________ (填“托盘天平”或“电子天平”)。
(2)步骤Ⅰ所得溶液pH___________ 7(填“>”“<”或“=”),原因是___________ 。
(3)步骤Ⅲ的化学方程式是___________ ,下列关于该反应的说法正确的是___________ (填标号)。
A.发生氧化还原反应
B.物质之间溶解度差异导致反应发生
C.冰水浴有助于晶体充分析出
(4)步骤Ⅱ与步骤Ⅳ中都有“置于40℃水浴锅中”,其目的分别是___________ 。
(5)步骤Ⅳ中用无水乙醇洗涤产品的优点是___________ 。
(6)减压过滤也叫抽滤,可加快过滤速度。如图为减压过滤装置,实验过程中操作顺序是___________ ⑤⑥(填序号)。
①打开抽气泵开关,倒入固液混合物 ②修剪滤纸,使其略小于布氏漏斗,让滤纸与漏斗紧密贴合 ③安装仪器,检查是否漏气 ④开始抽滤 ⑤断开吸滤瓶接管 ⑥关抽气泵。___________ (用含m的代数式表示)。
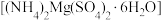 是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。
是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。实验室制备步骤如下:
Ⅰ.称取
 于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。
于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。Ⅱ.称取
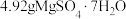 于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。
于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。Ⅲ.将步骤Ⅰ所得的
 溶液倒入步骤Ⅱ的
溶液倒入步骤Ⅱ的 溶液中,搅拌混合充分,冰水浴20min,析出晶体。
溶液中,搅拌混合充分,冰水浴20min,析出晶体。Ⅳ.减压过滤。用无水乙醇洗涤产品1~2次,抽干后,将晶体转移到蒸发皿里,置于40℃水浴锅中约30min,即可得
 晶体。
晶体。Ⅴ.所得晶体称重为mg。
回答下列问题:
(1)称取固体应采用
(2)步骤Ⅰ所得溶液pH
(3)步骤Ⅲ的化学方程式是
A.发生氧化还原反应
B.物质之间溶解度差异导致反应发生
C.冰水浴有助于晶体充分析出
(4)步骤Ⅱ与步骤Ⅳ中都有“置于40℃水浴锅中”,其目的分别是
(5)步骤Ⅳ中用无水乙醇洗涤产品的优点是
(6)减压过滤也叫抽滤,可加快过滤速度。如图为减压过滤装置,实验过程中操作顺序是
①打开抽气泵开关,倒入固液混合物 ②修剪滤纸,使其略小于布氏漏斗,让滤纸与漏斗紧密贴合 ③安装仪器,检查是否漏气 ④开始抽滤 ⑤断开吸滤瓶接管 ⑥关抽气泵。

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】为治理环境,减少雾霾,应采取措施减少氮氧化物(NOx)的排放量。还原法、氧化法、电化学吸收法是减少氮氧化物排放的有效措施。
(1)厌氧氨化法(Anammox) 是一种新型的氨氮去除技术。
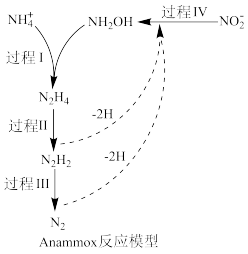
①N元素的原子核外电子排布式为______________ ;联氨(N2H4)中N原子采取_______ 杂化;H、N、O三种元素的电负性由大到小的顺序为_____________ 。
②过程II属于_________ 反应 (填“氧化”或“还原”)。
③该过程的总反应是_______________ 。
④NH2OH (羟胺)是一元弱碱,25℃时, 其电离平衡常数Kb=9.1×10-9,NH3·H2O 的电离平衡常数Kb=1.6×10-5,则1 molNH2OH和NH3·H2O分别与盐酸恰好反应生成的盐pH:前者___________ 后者。(填“大于”或“小于”)
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,其反应原理为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=-1625.5 kJ/mol。
4N2(g)+6H2O(g) △H=-1625.5 kJ/mol。
①该方法应控制反应温度在315~ 400℃之间,反应温度不宜过高的原因是_______________________________ 。
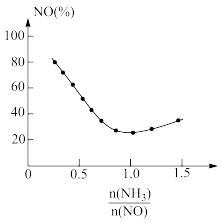
②氨氮比 会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当
会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当 时烟气中NO含量反而增大,主要原因是
时烟气中NO含量反而增大,主要原因是______________________________________ 。
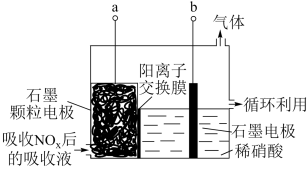
(3)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸,该电池的阳极反应式为______________________ 。
(1)厌氧氨化法(Anammox) 是一种新型的氨氮去除技术。

①N元素的原子核外电子排布式为
②过程II属于
③该过程的总反应是
④NH2OH (羟胺)是一元弱碱,25℃时, 其电离平衡常数Kb=9.1×10-9,NH3·H2O 的电离平衡常数Kb=1.6×10-5,则1 molNH2OH和NH3·H2O分别与盐酸恰好反应生成的盐pH:前者
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,其反应原理为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=-1625.5 kJ/mol。
4N2(g)+6H2O(g) △H=-1625.5 kJ/mol。①该方法应控制反应温度在315~ 400℃之间,反应温度不宜过高的原因是
②氨氮比
 会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当
会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当 时烟气中NO含量反而增大,主要原因是
时烟气中NO含量反而增大,主要原因是
(3)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽使之转化为硝酸,该电池的阳极反应式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】10℃时加热 饱和溶液,测得该溶液的pH发生如下变化:
饱和溶液,测得该溶液的pH发生如下变化:
甲同学认为:该溶液pH升高的原因是 的水解程度增大,碱性增强。
的水解程度增大,碱性增强。
(1)乙同学认为:该溶液pH升高的原因是 受热分解,生成了
受热分解,生成了 ,并推断
,并推断 的水解程度
的水解程度___________ (填“大于”或“小于”) 的水解程度。
的水解程度。
(2)丙同学认为:甲、乙的判断都不充分,还需要进一步补做实验来验证。
①将加热煮沸后的溶液冷却到10℃,若溶液的pH___________ (填“高于”“低于”或“等于”)8.3,则甲的判断正确。
②查阅资料,发现 的分解温度为150℃,丙断言
的分解温度为150℃,丙断言______ (填“甲”或“乙”)的判断是错误的,理由是_________ 。
(3)关于 饱和水溶液的表述正确的是
饱和水溶液的表述正确的是_________ (填字母)。
a.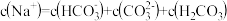
b.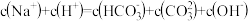
c. 的电离程度大于
的电离程度大于 的水解程度
的水解程度
 饱和溶液,测得该溶液的pH发生如下变化:
饱和溶液,测得该溶液的pH发生如下变化:| 温度 | 10℃ | 20℃ | 30℃ | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
 的水解程度增大,碱性增强。
的水解程度增大,碱性增强。(1)乙同学认为:该溶液pH升高的原因是
 受热分解,生成了
受热分解,生成了 ,并推断
,并推断 的水解程度
的水解程度 的水解程度。
的水解程度。(2)丙同学认为:甲、乙的判断都不充分,还需要进一步补做实验来验证。
①将加热煮沸后的溶液冷却到10℃,若溶液的pH
②查阅资料,发现
 的分解温度为150℃,丙断言
的分解温度为150℃,丙断言(3)关于
 饱和水溶液的表述正确的是
饱和水溶液的表述正确的是a.
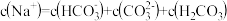
b.
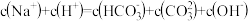
c.
 的电离程度大于
的电离程度大于 的水解程度
的水解程度
您最近一年使用:0次



