某学习小组利用  来探究“外界条件对化学反应速率的影响”。实验时,先分别量取
来探究“外界条件对化学反应速率的影响”。实验时,先分别量取  酸性溶液、
酸性溶液、 溶液,然后倒入大试管中迅速振荡,观察现象。
溶液,然后倒入大试管中迅速振荡,观察现象。
(1)可通过测定_______________ 来判断反应的快慢。
(2)为了观察到明显的现象,如果 与
与  溶液的体积相同,则它们初始物质的量浓度需要满足的关系为:
溶液的体积相同,则它们初始物质的量浓度需要满足的关系为: :
:
______ 。
(3)甲同学设计了如下实验
①探究温度对化学反应速率影响的组合实验编号是______ 。
②实验 测得混合后溶液褪色的时间为
测得混合后溶液褪色的时间为 ,忽略混 合前后体积的微小变化,则这段时间平均反应速率
,忽略混 合前后体积的微小变化,则这段时间平均反应速率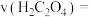
______ 
(4)在实验中,草酸 溶液与
溶液与  酸性溶液反应时,褪色总是先慢后快。
酸性溶液反应时,褪色总是先慢后快。
①乙同学据此提出以下假设:
假设 :反应放热
:反应放热
假设 :生成
:生成_____________ 对反应有催化作用
假设 :生成
:生成 对反应有催化作用
对反应有催化作用
假设 :反应生成的
:反应生成的  或
或 该反应有催化作用
该反应有催化作用
丙同学认为假设 不合理,其理由
不合理,其理由_______________ 。
②丁同学用如下实验证明假设 成立:在
成立:在  和
和  试管中分别加
试管中分别加 
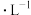 草酸溶液,再在
草酸溶液,再在  试管中加入
试管中加入 
 溶液、
溶液、 试管中加入
试管中加入_____  蒸馏水,然后在两支试管中同时分别加入
蒸馏水,然后在两支试管中同时分别加入 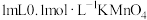 酸性溶液。
酸性溶液。
预期的实验现象是______ 。在  试管中加入蒸馏水的目的是
试管中加入蒸馏水的目的是______ 。
同学们认为不宜用 溶液代替
溶液代替  溶液对该反应进行催化探究,其原因是
溶液对该反应进行催化探究,其原因是 用离子方程式表示
用离子方程式表示
_______________ 。
 来探究“外界条件对化学反应速率的影响”。实验时,先分别量取
来探究“外界条件对化学反应速率的影响”。实验时,先分别量取  酸性溶液、
酸性溶液、 溶液,然后倒入大试管中迅速振荡,观察现象。
溶液,然后倒入大试管中迅速振荡,观察现象。(1)可通过测定
(2)为了观察到明显的现象,如果
 与
与  溶液的体积相同,则它们初始物质的量浓度需要满足的关系为:
溶液的体积相同,则它们初始物质的量浓度需要满足的关系为: :
:
(3)甲同学设计了如下实验
| 实验 编号 |  溶液 溶液 | 酸性 溶液 溶液 | 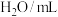 | 温度 | ||
浓度 | 体积 | 浓度 | 体积 | |||
 | 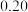 |  |  |  |  | 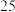 |
 | 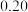 |  |  |  |  | 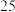 |
 | 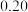 |  |  |  |  |  |
②实验
 测得混合后溶液褪色的时间为
测得混合后溶液褪色的时间为 ,忽略混 合前后体积的微小变化,则这段时间平均反应速率
,忽略混 合前后体积的微小变化,则这段时间平均反应速率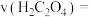

(4)在实验中,草酸
 溶液与
溶液与  酸性溶液反应时,褪色总是先慢后快。
酸性溶液反应时,褪色总是先慢后快。①乙同学据此提出以下假设:
假设
 :反应放热
:反应放热假设
 :生成
:生成假设
 :生成
:生成 对反应有催化作用
对反应有催化作用假设
 :反应生成的
:反应生成的  或
或 该反应有催化作用
该反应有催化作用丙同学认为假设
 不合理,其理由
不合理,其理由②丁同学用如下实验证明假设
 成立:在
成立:在  和
和  试管中分别加
试管中分别加 
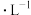 草酸溶液,再在
草酸溶液,再在  试管中加入
试管中加入 
 溶液、
溶液、 试管中加入
试管中加入 蒸馏水,然后在两支试管中同时分别加入
蒸馏水,然后在两支试管中同时分别加入 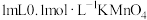 酸性溶液。
酸性溶液。预期的实验现象是
 试管中加入蒸馏水的目的是
试管中加入蒸馏水的目的是同学们认为不宜用
 溶液代替
溶液代替  溶液对该反应进行催化探究,其原因是
溶液对该反应进行催化探究,其原因是 用离子方程式表示
用离子方程式表示
更新时间:2021-11-16 20:55:45
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)我校化学社团做了如下探究实验:利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。实验数据如表所示:
①写出该反应的离子方程式:_______ 。
②通过实验A、B可探究_______ (填外部因素)的改变对反应速率的影响,其中V1=_______ ;通过实验_______ (填实验序号)可探究温度变化对化学反应速率的影响。
③利用实验B中数据计算,用KMnO4溶液的浓度变化表示的反应速率v(KMnO4)=_______ 。
④实验中发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是_______ ,相应的粒子最有可能是_______ 。
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
①表中a=_______ ,b=_______ 。
②能验证温度对化学反应速率影响规律的是实验_______ (填实验编号)。
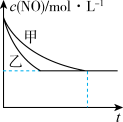
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线_______ (填“甲”或“乙”)。
(1)我校化学社团做了如下探究实验:利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。实验数据如表所示:
| 实验 序号 | 实验温度/K | KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | 溶液颜色褪至无色时所需时间/s | ||
 |  |  |  |  | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 3 |  |
| B | 293 | 2 | 0.02 | 3 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 5 |  |
②通过实验A、B可探究
③利用实验B中数据计算,用KMnO4溶液的浓度变化表示的反应速率v(KMnO4)=
④实验中发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对KMnO4与H2C2O4之间的反应有某种特殊的作用,则该作用是
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO
 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。实验 编号 | t/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 催化剂的比表面积/m2/g |
| I | 280 |  |  | 82 |
| II | 280 |  | b | 124 |
| Ⅲ | 350 | a |  | 82 |
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室可利用甲醇、空气和铜制备甲醛。甲醇和甲醛的沸点和水溶性见下表:
下图是两个学生设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如(甲)和(乙)所示,试回答:
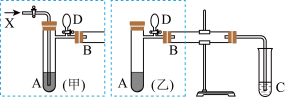
(1)若按(甲)装置进行实验,则通入A管的X是_______ ,B中反应的化学方程式为_______ 。
(2)若按(乙)装置进行实验,则B管中应装_______ 。
(3)C中应装的试剂是_______ ,乙在实验完成时,先打开D处气球的铁夹,再撤去酒精灯,打开铁夹的目的是_______ 。
(4)你认为用甲和乙哪套装置较好,并描述其理由_______ 。
(5)现有两种烯烃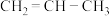 和
和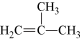 ,它们的混合物在一定条件下发生加聚反应,其产物中可能有
,它们的混合物在一定条件下发生加聚反应,其产物中可能有
①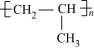 ②
②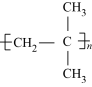 ③
③
④ ⑤
⑤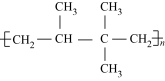 ⑥
⑥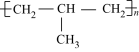
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 混溶 |
| 甲醛 | -21 | 混溶 |

(1)若按(甲)装置进行实验,则通入A管的X是
(2)若按(乙)装置进行实验,则B管中应装
(3)C中应装的试剂是
(4)你认为用甲和乙哪套装置较好,并描述其理由
(5)现有两种烯烃
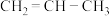 和
和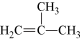 ,它们的混合物在一定条件下发生加聚反应,其产物中可能有
,它们的混合物在一定条件下发生加聚反应,其产物中可能有①
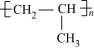 ②
②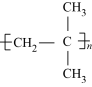 ③
③
④
 ⑤
⑤ ⑥
⑥
| A.全部 | B.只有①②③⑤ | C.只有①②③④ | D.只有③⑤⑥ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】电镀工业会产生大量的电镀污水,处理某酸性电镀废液(主要含Cu2+、Fe3 +)以制备氯化亚铜的工艺流程如图所示:
已知:① 氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。
② 常温下,
请回答下列问题:
(1)加H2SO4的步骤中,下列措施,可提高溶解速率的是_______ (填序号)。
a.加热 b.增大压强 c.延长浸出时间 d.适当提高硫酸的浓度
(2)电镀污泥的主要成分是____ ,产品CuCl晶体要用无水乙醇洗涤、真空干燥、密封包装的目的是______________ 。
(3)加入H2SO4的目的是_________ 。
(4)亚硫酸钠、氯化钠、硫酸铜在溶液中反应生成CuCl的离子方程式为__________ 。
(5)实验探究pH对CuCl产率的影响如图 所示,当pH=2时CuCl 产率最大的原因是_________
(6)以碳棒为电极电解CuCl2溶液也可得到CuCl。写出电解CuCl2溶液阴极的反应方程式:_______

已知:① 氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。
② 常温下,
| 物质 | Fe(OH)3 | Cu(OH)2 |
| Ksp | 4.0×10-38 | 5.0×10-20 |
(1)加H2SO4的步骤中,下列措施,可提高溶解速率的是
a.加热 b.增大压强 c.延长浸出时间 d.适当提高硫酸的浓度
(2)电镀污泥的主要成分是
(3)加入H2SO4的目的是
(4)亚硫酸钠、氯化钠、硫酸铜在溶液中反应生成CuCl的离子方程式为
(5)实验探究pH对CuCl产率的影响如图 所示,当pH=2时CuCl 产率最大的原因是

(6)以碳棒为电极电解CuCl2溶液也可得到CuCl。写出电解CuCl2溶液阴极的反应方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】在一个2L的密闭容器中投入反应物,发生反应2SO3(g) 2SO2(g)+O2(g) ΔH>0,其中SO3的变化如图所示:
2SO2(g)+O2(g) ΔH>0,其中SO3的变化如图所示:___________ 。
(2)8min时反应达平衡状态,下列能说明该反应已达到平衡状态的是___________(填序号)。
(3)升高温度,该反应的K值将___________ (填“增大”、“减小”或“不变”)。
(4)在第12min时,容器压缩到1L,则SO3的变化曲线为___________ (填a、b、c或d)。
(5)若保持容积不变,在第12min时加入SO3(g),则平衡向___________ (填“正”或“逆”)反应方向移动,SO3的体积分数___________ (填“增大”或“减小”)。
 2SO2(g)+O2(g) ΔH>0,其中SO3的变化如图所示:
2SO2(g)+O2(g) ΔH>0,其中SO3的变化如图所示:
(2)8min时反应达平衡状态,下列能说明该反应已达到平衡状态的是___________(填序号)。
| A.n(SO3)∶n(SO2)∶n(O2)=2∶2∶1 |
| B.容器内压强保持不变 |
| C.v(SO2)逆=2v(O2)正 |
| D.容器内密度保持不变 |
(3)升高温度,该反应的K值将
(4)在第12min时,容器压缩到1L,则SO3的变化曲线为
(5)若保持容积不变,在第12min时加入SO3(g),则平衡向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】二氧化碳的重整和综合利用可以有效缓解环境压力,助力尽快实现双碳目标。CO2与H2合成甲醇涉及反应:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.2kJ•mol-1
CO(g)+H2O(g) △H2=+41.2kJ•mol-1
Ⅲ.CO(g)+2H2(g) CH3OH(g) △H3=-90.2kJ•mol-1
CH3OH(g) △H3=-90.2kJ•mol-1
回答下列问题:
(1)△H1=______ 。
(2)若反应II的△S2=+42.1J•mol-1•K-1,则该反应在298K时______ (填“能”或“不能”)自发进行。
(3)T0℃,向10L恒容密闭容器中充入1molCO2和3molH2发生上述反应。10min末达到平衡时测得容器中CO2的转化率为90%,CO的物质的量为0.3mol。
①0~10min内,平均反应速率v(CH3OH)=______ 。
②下列叙述不能作为上述反应达到平衡状态标志的是______ 。
A.H2O的生成速率与CO2的消耗速率相等
B.混合气体的总质量不再变化
C.混合气体的总压强不再变化
D.CO的物质的量不再变化
③T0℃时,H2的平衡转化率为______ ;该温度下,反应Ⅰ的平衡常数Kc=______ (保留三位有效数字)。
(4)我国学者结合实验和计算机模拟结果,提出了CO2电还原制备CH3OH的机理,其部分反应历程如图所示,吸附在催化剂表面的物种用“•”标注。

其中CO2在______ (填“阴极”或“阳极”)上发生反应;下列转化过程中,可能适合在高温条件下进行的是______ (填选项字母)。
A.CO2+6H→•CO2 B.•CO+•OH→•CO+•H2O
C.•OCH•→OCH2 D.•CH3OH→CH3OH
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.2kJ•mol-1
CO(g)+H2O(g) △H2=+41.2kJ•mol-1Ⅲ.CO(g)+2H2(g)
 CH3OH(g) △H3=-90.2kJ•mol-1
CH3OH(g) △H3=-90.2kJ•mol-1回答下列问题:
(1)△H1=
(2)若反应II的△S2=+42.1J•mol-1•K-1,则该反应在298K时
(3)T0℃,向10L恒容密闭容器中充入1molCO2和3molH2发生上述反应。10min末达到平衡时测得容器中CO2的转化率为90%,CO的物质的量为0.3mol。
①0~10min内,平均反应速率v(CH3OH)=
②下列叙述不能作为上述反应达到平衡状态标志的是
A.H2O的生成速率与CO2的消耗速率相等
B.混合气体的总质量不再变化
C.混合气体的总压强不再变化
D.CO的物质的量不再变化
③T0℃时,H2的平衡转化率为
(4)我国学者结合实验和计算机模拟结果,提出了CO2电还原制备CH3OH的机理,其部分反应历程如图所示,吸附在催化剂表面的物种用“•”标注。

其中CO2在
A.CO2+6H→•CO2 B.•CO+•OH→•CO+•H2O
C.•OCH•→OCH2 D.•CH3OH→CH3OH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】I.丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如下图。

(1)丙烷脱氢制丙烯的过程中。恒压时向原料气中掺入高温水蒸气,则K(主反应)_______ (填“增大”、“减小”或不变”,下同),转化率α(C3H8)_______ 。温度升高,副反应更容易发生的主要原因是_______ 。
(2)先以丙烯制丙烯腈,再用丙烯腈在阴极电合成已二腈(弱酸环境),总反应式:2CH2=CH-CN+H2O=NC(CH2)4CN+1/2O2↑,则阳极电极反应式:_______ 。
II.在2.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应:CH4(g)+2NO2(g)⇌CO2(g)+N2(g)+2H2O(g) △H<0,温度为T1和T2下,反应时间(t)与容器内甲烷物质的量数据见下表:
(3)计算T1、0~2min内NO2的平均反应速率v(NO2)=_______ mol·L-1·min-1,温度T2下的平衡常数K=_______ mol·L-1(若提供的数据不足以计算,填“无法确定”)。
(4)在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,不同温度下,NO2的转化率随温度的变化如下图。c点_______ (填“是”或“不是”)反应达平衡的点。


(1)丙烷脱氢制丙烯的过程中。恒压时向原料气中掺入高温水蒸气,则K(主反应)
(2)先以丙烯制丙烯腈,再用丙烯腈在阴极电合成已二腈(弱酸环境),总反应式:2CH2=CH-CN+H2O=NC(CH2)4CN+1/2O2↑,则阳极电极反应式:
II.在2.0L密闭容器中,通入0.10molCH4和0.20molNO2进行反应:CH4(g)+2NO2(g)⇌CO2(g)+N2(g)+2H2O(g) △H<0,温度为T1和T2下,反应时间(t)与容器内甲烷物质的量数据见下表:
| 时间(t/min) | 0 | 2 | 4 | 6 | 10 | 12 |
| T1,甲烷物质的量 | 0.10 | 0.082 | 0.068 | 0.060 | 0.045 | 0.045 |
| T2,甲烷物质的量 | 0.10 | 0.080 | 0.065 | 0.055 | 0.050 | _ |
(4)在一恒容密闭容器中,通入一定量CH4和NO2,测得在相同时间内,不同温度下,NO2的转化率随温度的变化如下图。c点

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究性学习小组利用 与酸性
与酸性 溶液的反应,探究“外界条件对化学反应速率的影响”,实验记录如下表所示:
溶液的反应,探究“外界条件对化学反应速率的影响”,实验记录如下表所示:
查阅资料:酸性 溶液中滴加过量的
溶液中滴加过量的 ,振荡后溶液由紫色变为无色,回答下列问题。
,振荡后溶液由紫色变为无色,回答下列问题。
(1)该反应的离子方程式为:_______ 。
(2)
_______ 。
(3)
_______ ,理由是_______ 。
(4)若探究温度对化学反应速率的影响,可选择实验_______ (填组别),根据实验数据,可以得出的结论是_______ 。
(5)发生反应
 ,该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有_______(填字母序号)。
,该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有_______(填字母序号)。
(6)某反应过程的能量变化如图所示(填入字母)。
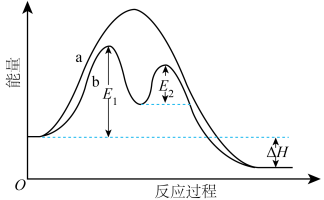
①该反应过程有催化剂参与的是_______ 。
②该反应的活化能为_______ 。
 与酸性
与酸性 溶液的反应,探究“外界条件对化学反应速率的影响”,实验记录如下表所示:
溶液的反应,探究“外界条件对化学反应速率的影响”,实验记录如下表所示:| 实验 组别 | 实验温度/K | 参加反应的物质 | 溶液褪色所需时间/s | ||||
 溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | |||||
| V/mL |  | V/mL |  | V/mL | |||
| A | 293 | 3 | 0.2 | 7 | 1 | 0 | 60 |
| B |  | 3 | 0.2 | 5 | 1 |  | 80 |
| C | 313 | 3 | 0.2 |  | 1 | 2 |  |
 溶液中滴加过量的
溶液中滴加过量的 ,振荡后溶液由紫色变为无色,回答下列问题。
,振荡后溶液由紫色变为无色,回答下列问题。(1)该反应的离子方程式为:
(2)

(3)

(4)若探究温度对化学反应速率的影响,可选择实验
(5)发生反应

 ,该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有_______(填字母序号)。
,该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有_______(填字母序号)。| A.改用高效催化剂 | B.缩小容器的体积 |
| C.升高温度 | D.增加CO的浓度 |

①该反应过程有催化剂参与的是
②该反应的活化能为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】为了探究反应速率的影响因素和反应限度,依据科学研究,对于多因素(变量)问题,常采用只改变某一个因素,控制其他因素不变的研究方法,某实验小组进行如下实验:
I.用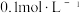 的硫代硫酸钠与
的硫代硫酸钠与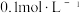 硫酸反应,实验数据如表1:
硫酸反应,实验数据如表1:
表1
(1)表1中V1=_______ ,V3=_______ ,t的取值范围是_______ (填标号)。
a.<15 b.1 5~20 c.>20
Ⅱ.取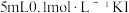 溶液于试管中,并加入5~6滴
溶液于试管中,并加入5~6滴 溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。
溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。
(2)根据上述实验现象,写出KI溶液与FeCl3溶液反应的离子方程式:_______ ;“取出上层清液,滴入2滴KSCN溶液,观察到溶液变红[产生了Fe(SCN)3]”描述中发生反应的离子方程式为_______ 。
Ⅲ.在500℃和101kPa条件下,将一定量的SO2和O2充入含有催化剂的密闭容器中,传感器测得各组分浓度随时间变化如表2:
表2
(3)c1=_______ ,0~40s内, 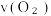 =
= _____ mol·L-1·min-1
(4)反应达到平衡时,SO3的体积分数为_____ (保留3位有效数字)。
I.用
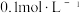 的硫代硫酸钠与
的硫代硫酸钠与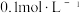 硫酸反应,实验数据如表1:
硫酸反应,实验数据如表1:表1
| 编号 | Na2S2O3体积/mL | 加水的体积/mL | 硫酸体积/mL | 水浴温度/℃ | 出现浑浊用时/s |
| 1 | 2 | 1 | 2 | 25 | 15 |
| 2 | 1 | V1 | 2 | 25 | 20 |
| 3 | 2 | V2 | V3 | 35 | t |
a.<15 b.1 5~20 c.>20
Ⅱ.取
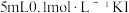 溶液于试管中,并加入5~6滴
溶液于试管中,并加入5~6滴 溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。
溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。(2)根据上述实验现象,写出KI溶液与FeCl3溶液反应的离子方程式:
Ⅲ.在500℃和101kPa条件下,将一定量的SO2和O2充入含有催化剂的密闭容器中,传感器测得各组分浓度随时间变化如表2:
表2
| 反应时间/s | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| c(SO2)/(mol·L-1) | 10 | c1 | 5 | 3.5 | 2.5 | c2 | c2 |
| c(O2)/(mol·L-1) | 5 | 3.5 | 2.5 | 1.75 | c3 | 1 | 1 |
| c(SO3)/(mol·L-1) | 0 | 3 | 5 | 6.5 | 7.5 | 8 | 8 |
 =
= (4)反应达到平衡时,SO3的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
请回答:
(1)表中实验Ⅰ需加入蒸馏水V1=_______ 。验证浓度对反应速率影响的实验是_______ (填实验序号,下同)验证温度对反应速率影响的实验是_______ 。
(2)利用实验Ⅰ中数据计算,忽略混合前后溶液体积的微小变化,若用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=_______ 。
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
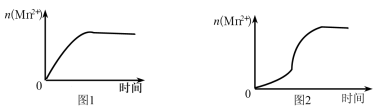
①该小组同学提出的假设是_______ 。
②请你帮助该小组同学完成实验方案Ⅳ。
问题:该反应的催化剂选择MnCl2还是MnSO4_______ (填“MnCl2”或“MnSO4”)。
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/ mL | 试验温度/0C | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol·L-1H2C2O4溶液 | H2O | 3 mol·L-1稀硫酸 | 0.05mol·L-1KMnO4溶液 | |||
| Ⅰ | 3 | V1 | 2 | 3 | 25 | 1.5 |
| Ⅱ | 2 | 3 | 2 | 3 | 25 | 2.7 |
| Ⅲ | 2 | 3 | 2 | 3 | 40 | 1.3 |
(1)表中实验Ⅰ需加入蒸馏水V1=
(2)利用实验Ⅰ中数据计算,忽略混合前后溶液体积的微小变化,若用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是
②请你帮助该小组同学完成实验方案Ⅳ。
| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol·L-1H2C2O4溶液 | H2O | 3 mol·L-1稀硫酸 | 0.05mol·L-1KMnO4溶液 | |||
| Ⅳ | 3.0 | 2.0 | 2.0 | 3.0 | t | |
您最近一年使用:0次



