某同学向50mL0.001
 溶液和50 mL一定浓度的盐溶液中,分别滴加1滴1
溶液和50 mL一定浓度的盐溶液中,分别滴加1滴1  盐酸和1滴1
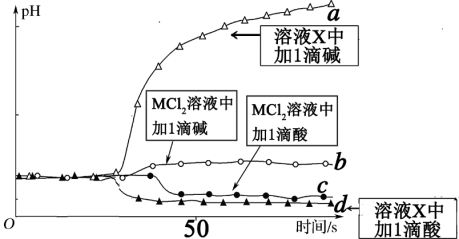
盐酸和1滴1 NaOH溶液,测得溶液pH随时间变化的曲线如图所示。下列说法错误的是
NaOH溶液,测得溶液pH随时间变化的曲线如图所示。下列说法错误的是

 溶液和50 mL一定浓度的盐溶液中,分别滴加1滴1
溶液和50 mL一定浓度的盐溶液中,分别滴加1滴1  盐酸和1滴1
盐酸和1滴1 NaOH溶液,测得溶液pH随时间变化的曲线如图所示。下列说法错误的是
NaOH溶液,测得溶液pH随时间变化的曲线如图所示。下列说法错误的是
A. 是一种弱碱 是一种弱碱 |
B.加酸或碱 水解平衡发生移动 水解平衡发生移动 |
| C.溶液X可能是KCl溶液 |
| D.依据a、d变化可以判断,加碱对X溶液pH影响程度大 |
更新时间:2021-11-17 09:53:55
|
【知识点】 盐类水解规律理解及应用解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关系式错误的是( )
| A.CO2的水溶液:c(H+)>c(HCO3-)>2c(CO32-) |
| B.等浓度的HCN溶液与NaOH溶液等体积混合,所得溶液pH>7,则溶液中离子浓度:c(Na+)>c(CN-) >c(OH-)>c(H+) |
| C.NaHCO3溶液中存在水解平衡:HCO3-+H2O⇌H2CO3+OH- |
D.两种弱酸HX和HY混合后,溶液中的c(H+)为(Ka为电离平衡常数) 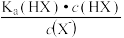 + +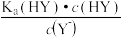 + c(OH-) + c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法错误的是
| A.向醋酸溶液中加水,溶液中所有离子的浓度都减小 |
B.25℃时, 的NaHA的水溶液中: 的NaHA的水溶液中: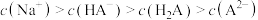 |
| C.盐类水解可看作酸碱中和反应的逆反应 |
D. 溶液呈酸性是由于溶液中 溶液呈酸性是由于溶液中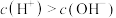 |
您最近一年使用:0次

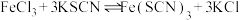 平衡体系中加入KCl固体
平衡体系中加入KCl固体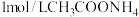 溶液
溶液 溶液对水的电离程度无影响
溶液对水的电离程度无影响 溶液中加入
溶液中加入 固体
固体

