工业制硫酸的一步重要反应是SO2在400~600℃下的催化氧化:2SO2(g)+ O2(g)⇌2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法正确的是
| A.使用催化剂可加快反应速率,提高SO3产率 |
| B.其它条件保持不变,温度越高,速率越快,生产效益越好 |
| C.实际生产中选定400~600℃作为操作温度,其原因是在此温度下催化剂的活性最高 |
| D.增大压强可以提高SO3产率,但高压对动力和设备要求太高,会增加生产成本 |
更新时间:2021-11-17 14:52:42
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液 | B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| B | 取5 mL 0.1 mol·L-1KI溶液,加入1 mL 0.1 mol·L-1FeCl3溶液,萃取分液后,向水层滴入KSCN溶液 | 溶液变成血红色 | Fe3+与I-所发生的反应为可逆反应 |
| C | 向鸡蛋清溶液中滴加饱和Na2SO4溶液 | 有固体析出 | 蛋白质发生变性 |
| D | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液,水浴加热 | 未出现银镜 | 蔗糖未水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定条件下, 和
和 反应生成
反应生成 和
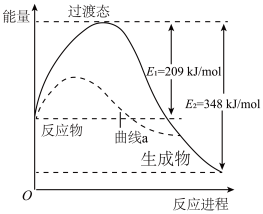
和 的能量变化如图所示,下列说法不正确的是
的能量变化如图所示,下列说法不正确的是
 和
和 反应生成
反应生成 和
和 的能量变化如图所示,下列说法不正确的是
的能量变化如图所示,下列说法不正确的是
A.该反应放出了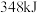 的热量 的热量 |
| B.曲线a可能是反应使用了催化剂 |
| C.断键吸收能量之和小于成键释放能量之和 |
D.该反应热化学方程式为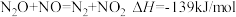 |
您最近一年使用:0次
【推荐3】Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下: ①Cl2(g)  2Cl•(g)快;②CO(g)+Cl•(g)
2Cl•(g)快;②CO(g)+Cl•(g) COCl•(g)快;③COCl•(g)+Cl2(g)
COCl•(g)快;③COCl•(g)+Cl2(g) COCl2(g)+Cl•(g)慢。其中反应②存在v正=k正c(CO) c(C1•)、v逆=k逆c(COCl•)。下列说法正确的是
COCl2(g)+Cl•(g)慢。其中反应②存在v正=k正c(CO) c(C1•)、v逆=k逆c(COCl•)。下列说法正确的是
| A.反应①的活化能大于反应③的活化能 |
B.反应②的平衡常数K=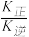 |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.选择合适的催化剂能加快该反应的速率,并提高COCl2的平衡产率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g) CH3OH(g)达到平衡,下列说法正确的是
CH3OH(g)达到平衡,下列说法正确的是
 CH3OH(g)达到平衡,下列说法正确的是
CH3OH(g)达到平衡,下列说法正确的是| 容器 | 温度/K | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0.20 | 0.10 | 0 | 0.025 |
| A.该反应的正反应放热 |
| B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 |
| C.达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍 |
| D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
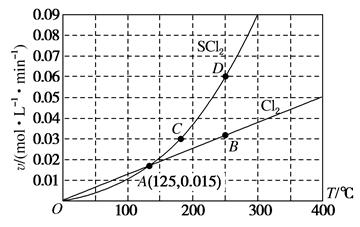
【推荐2】一定压强下,向10L密闭容器中充入1molS2Cl2和1molCl2,发生反应: S2Cl2(g)+Cl2(g) 2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
 2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
| A.正反应的活化能大于逆反应的活化能 |
| B.A、B、C、D四点对应状态下,达到平衡状态的为A点 |
| C.一定温度下,在密闭容器中达到平衡后缩小容器体积,重新达到平衡后,S2Cl2的平衡转化率不变 |
| D.达到平衡后再加热,平衡向逆反应方向移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】在密闭容器中发生如下反应:mA(g)+nB(g) ⇌pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的 ,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
 ,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )
,当达到新平衡时,C的浓度为原来的1.5倍,下列说法正确的是( )A. | B.平衡向逆反应方向移动 |
| C.A的转化率减小 | D.C的体积分数增加 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】在一定温度下的密闭容器中加入一定量的A、B发生反应: ,平衡时测得A的浓度为
,平衡时测得A的浓度为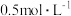 。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为
。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为 。下列有关判断正确的是
。下列有关判断正确的是
 ,平衡时测得A的浓度为
,平衡时测得A的浓度为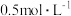 。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为
。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为 。下列有关判断正确的是
。下列有关判断正确的是| A.B的转化率减小 | B.平衡向逆反应方向移动 |
C. | D.C的体积分数增大 |
您最近一年使用:0次

 的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是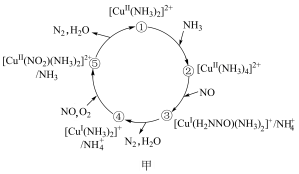
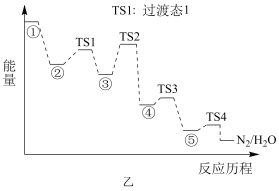
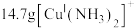 消耗时,状态④到状态⑤的变化过程中转移的电子为
消耗时,状态④到状态⑤的变化过程中转移的电子为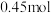
 。选择合适的催化剂,可以得出温度对合成乙醇的影响情况如图所示(选择性
。选择合适的催化剂,可以得出温度对合成乙醇的影响情况如图所示(选择性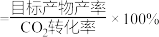 )。下列说法正确的是
)。下列说法正确的是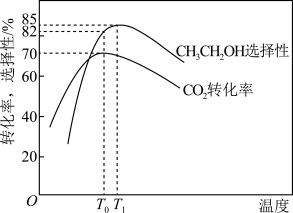

 的转化率
的转化率 时,乙醇的产率为57.4%
时,乙醇的产率为57.4% 时,升高温度,乙醇的产率降低
时,升高温度,乙醇的产率降低

